Antiviraux : un développement souvent difficile (illustration).
Dès le début de l'épidémie COVID-19, une question majeure a été martelée par tous : le traitement, c'est pour quand ? Dix mois plus tard, y a-t-il un traitement ? Non.
Tout juste, et c'est déjà beaucoup, avons-nous vu se préciser l'intérêt de quelques traitements médicamenteux symptomatiques, comme la dexaméthasone, dont l'usage vient d'être validé par l'Agence médicale européenne le 18 septembre 2020 ("Dexamethasone can be considered a treatment option for adults and adolescents with SARS-CoV-2 infection who require supplemental oxygen therapy") et les anticoagulants.
Tout juste, et c'est déjà beaucoup, les réanimateurs ont-ils défini une optimisation progressive de la prise en charge des patients ayant les atteintes les plus graves, avec d'évidents progrès.
Mais, puisqu'il s'agit d'une maladie infectieuse, quand aura-t-on un traitement anti-infectieux ?
Plus de 10 000 antibiotiques identifiés
Le public le moins averti sait que, depuis 80 ans, les antibiotiques ont bouleversé le pronostic des maladies bactériennes, même si, aujourd'hui, des difficultés, dues à l'émergence de résistances bactériennes induites par la défense de la bactérie, la complexité de certains malades et, très souvent, par un mésusage des antibiotiques, subsistent ou réapparaissent.
Le développement de ces médicaments a été fulgurant : quarante ans après la pénicilline, l'essentiel des molécules était inventé, connu, efficace, rentable. À tel point que certains avaient déclaré la fin des maladies infectieuses !
Malheureusement, il n'en était rien et, durant les quarante années suivantes (1980-2020), une dizaine de nouvelles bactéries (mais encore beaucoup plus de virus émergents) sont apparues comme de nouvelles menaces.
Fabriquer un antibactérien (un antibiotique) est relativement facile. Il s'agit "simplement" de trouver une substance qui tue la bactérie, ou au moins inhibe sa croissance (bactériostase).
Si, bien évidemment, dans la vie réelle, rien n'est aussi élémentaire, la saga des antibiotiques fut et reste un énorme succès. Plus de 10 000 molécules antibiotiques ont été identifiées, au moins 400 ont donné lieu à des développements, et plus de 150 ont été commercialisées. Toutes sont efficaces, sous réserve de conditions pharmacodynamiques et pharmacocinétiques favorables et de résoudre quelques problèmes (pas tout à fait annexes) de tolérance et d'interactions. Sans oublier que les cibles d'action sur les bactéries sont nombreuses et varient suivant les antibiotiques : inhibition de la synthèse de la paroi, de l'ADN, de l'ARN ou des protéines du ribosome, principalement.
La longue et laborieuse quête des antiviraux
Les virus sont des parasites qui ne peuvent exister sans les cellules qu'ils infectent pour se reproduire, ce qu'ils ne peuvent faire seuls. Les virus ne sont donc pas tout à fait des organismes vivants, ce qui n'est pas le cas des bactéries qui, quoique procaryotes, peuvent exister de façon autonome, pourvu qu'ils soient à portée des substrats nécessaires.
Contrairement à un antibiotique, un antiviral n'est qu'un médiateur qui va empêcher le virus, soit de pénétrer dans la cellule, soit d'en sortir. Il s'agit d'une molécule perturbant le cycle de réplication d'un ou de plusieurs virus, pouvant ralentir, mais rarement arrêter une infection virale. Un antiviral n'élimine pas les particules virales, mais interfère simplement avec une ou plusieurs des étapes de la réplication virale, contrairement à un antibiotique qui attaque la bactérie elle-même.
La chimiothérapie antivirale connaît depuis toujours un développement lent et laborieux, conséquence de propriétés intrinsèques liées aux virus : parasitisme intracellulaire strict, incapacité à s'autorépliquer, diversité (taille variable, génome simple ou très complexe, virus à ADN et à ARN, etc.).
Depuis les années 1960, l'invention de médicaments antiviraux s'est révélée beaucoup plus difficile et n'a pas du tout permis (en tout cas dans les mêmes conditions) d'obtenir les extraordinaires succès des antibiotiques.
Un antiviral va en effet se heurter à deux obstacles : l'interférence avec le métabolisme cellulaire normal et la variabilité génétique des virus (VIH en particulier). De plus, comme dit plus haut, les antiviraux sont virustatiques (entraînant une inhibition réversible de la réplication virale) : beaucoup sont des inhibiteurs compétitifs des ARN ou ADN polymérases ; il s'agit de promédicaments qui nécessitent une bi ou une tri-phosphorylation intracellulaire afin d'être actifs. Ainsi en est-il des antiviraux des virus herpès. Seuls les antiviraux récents de l'hépatite C chronique permettent d'accéder à l'objectif de l'éradication virale, et donc à la guérison. Ce sont ceux qu'on appelle des antiviraux à action directe, inhibiteurs de protéases, de polymérases. Cependant, les classes pharmacologiques correspondantes doivent être utilisées avec précautions du fait de nombreux effets indésirables et d'interactions médicamenteuses via une induction/inhibition de certains cytochromes.
Le nombre de virus pour lesquels il n'y a aucun traitement antiviral est très élevé
Certes, un virus a été éliminé de l'histoire, celui de la variole (qui pourrait être la sixième plaie d'Égypte) et sa vaccination a pu être supprimée. Avec 40 ans de recul, il s'agit-là d'un grand succès.
L'OMS nous a aussi annoncé, il y a un mois, l'éradication en Afrique des virus sauvages de la poliomyélite. En réalité, on sait (pour diverses raisons - dont la diffusion de virus vaccinaux), qu'on est loin de pouvoir suspendre la vaccination de cette maladie, même si elle a disparu de l'essentiel des pays.
En revanche, le nombre de virus pour lesquels il n'y a aucun traitement antiviral est très élevé : fièvre jaune, maladie à virus Ebola, à virus de Marburg, fièvre de Lassa, infection à Hantavirus et diverses fièvres hémorragiques. On peut y ajouter la rage, certaines encéphalites, ainsi que des maladies qui défrayent régulièrement la chronique : dengue, Chikungunya, infection à virus Zika, sans oublier la poliomyélite et, bien sûr, la rougeole, la rubéole, les oreillons. Citons encore les infections dues à d'autres coronavirus ou au virus respiratoire syncytial. Et la liste est loin d'être close.
Les infections pour lesquelles il existe des traitements antiviraux
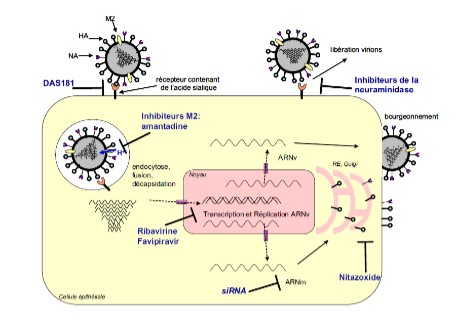
Plusieurs infections virales ont toutefois bénéficié de la mise au point de traitements spécifiques, mais souvent au prix de longues années de recherche dont la complexité est notamment illustrée par le schéma ci-dessous, qui montre les cibles d'action des antiviraux de la grippe (cf. Figure 1).
Figure 1 - Cycle schématique de multiplication du virus grippal et cibles d'action des antiviraux (d'après : Escuret V, Frobert E et Lina B. Grippe et antiviraux. Réanimation 2011 ; 20 : 169-177)
- Le succès peut-être le plus éclatant de la recherche sur les antiviraux est la mise au point du traitement de l'infection à VIH.
Il s'agit-là d'une révolution formidable, mais il s'est passé quinze ans entre la découverte du virus et l'établissement de traitements efficaces. Depuis 1996, un énorme travail a été accompli pour proposer des traitements plus actifs, plus acceptables, mieux tolérés. Plus de 50 antirétroviraux ont fait l'objet de développements. Le rêve reste, bien sûr, de pouvoir arrêter tout médicament, mais, 40 ans après la découverte de la maladie, le traitement qui permettra l'éradication définitive du virus n'est pas encore là.
- De nombreux médicaments sont disponibles pour traiter les hépatites virales,
Dans l'hépatite C, c'est presque le miracle depuis la mise à disposition en 2014 (vingt ans après la découverte du VHC) des antiviraux dits à action directe qui guérissent 95 % des infections chroniques. Il s'agit d'associations fixes de 2, voire de 3 inhibiteurs de protéase et/ou de polymérase.
Ces antiviraux permettent l'éradication du virus et la guérison de l'infection !
Dans l'hépatite B, c'est plus compliqué. Les traitements restent nombreux (interféron, analogues nucléosidiques [entécavir, lamivudine] et nucléotidiques [adéfovir, ténofovir]), mais ils n'entraînent pas la guérison : on cherche la stabilisation de la fibrose, la prévention de la cirrhose et du carcinome hépatocellulaire. En revanche, la vaccination, très efficace, devrait prévenir à l'avenir la survenue d'infection par ce virus.
- Pour la grippe, le bon traitement, c'est la vaccination
Les inhibiteurs de la neuraminidase ont été développés dans les années 1990. Le zanamivir d'abord, puis l'oséltamivir, ont été commercialisés entre 1999 et 2001. Depuis un quart de siècle, le débat sur l'efficacité et l'utilité de ces antiviraux n'est cependant pas clos. L'oséltamivir est indiqué en prophylaxie post-exposition, mais aussi pour le traitement de la grippe. Même si le niveau de preuve de l'efficacité est faible, il paraît suffisant pour justifier la prescription de cet antiviral chez des patients à risque élevé de complications ou lors de formes graves (avis du HCSP du 16 mars 2018). Toutefois, il est à peu près certain que si l'oséltamivir est efficace, ce ne peut-être que lorsque le traitement est débuté très précocement, moins de 48 heures après les premiers symptômes.
Cet antiviral vient toutefois de faire l'objet d'un avis sévère de la Haute Autorité de santé (commission de la transparence du 24 juin 2020), qui pourrait conduire à modifier ces recommandations. Ses conclusions sont :
- En prophylaxie, le service médical rendu (SMR) est faible en situation de pandémie grippale avérée ou potentielle ; il est insuffisant dans les autres situations (prophylaxie lors des épidémies saisonnières de grippe).
- En traitement curatif, le SMR est insuffisant pour justifier d'une prise en charge par la solidarité nationale dans le cadre d'un traitement curatif de la grippe, en cas d'épidémie saisonnière ou de pandémie grippale.
Par ailleurs, le zanamivir n'est plus disponible sous sa forme inhalée. Une forme parentérale existe en ATU nominative depuis 2009 (année de la pandémie H1N1), dénommée DECTOVA : cette forme a fait l'objet d'un avis de la commission de transparence (en date du 1er avril 2020) et un SMR insuffisant lui a été attribué.
Sans pouvoir dire que le débat autour de ces antiviraux est clos, il est certain que leur efficacité et leur utilité ne sont pas évidentes : en un demi-siècle, aucun produit vraiment actif n'a été inventé pour le traitement des virus influenzae de la grippe.
Et même si la vaccination n'est pas efficace à 100 %, c'est elle qui reste l'outil de prévention le plus fiable contre la grippe et les complications associées, notamment dans les populations à risque.
- La ribavirine, un antiviral ancien essayé sur de nombreux virus
- Focus sur les anti-herpesviridae
- Le cytomégalovirus (CMV) est à l'origine de pathologies très variées chez les immunocompétents, mais surtout chez les immunodéprimés
- L'arrivée de l'aciclovir, à la fin des années 1970, fut une vraie révolution pour le traitement des dramatiques encéphalites herpétiques
La précocité du traitement, ainsi que la prise en charge immédiate sont des éléments majeurs du pronostic. L'aciclovir est un antiviral à action directe. Après avoir été phosphorylé en aciclovir triphosphate par une thymidine-kinase virale, présente uniquement dans les cellules infectées par le virus, il agit comme un inhibiteur compétitif sélectif de l'ADN-polymérase virale. L'incorporation de cet analogue nucléosidique stoppe l'élongation de la chaîne d'ADN, interrompant ainsi la synthèse d'ADN viral : la réplication virale est donc bloquée.
- Les autres médicaments de l'herpès
En dehors de l'encéphalite herpétique (heureusement rare - 2 cas/million d'habitants), ces antiviraux sont indiqués dans les différentes manifestations de l'herpès (voir les résumés des caractéristiques du produit [RCP] de chacun de ces antiviraux).
L'aciclovir peut être utilisé en prévention, en cas de récurrence d'herpès génital ou cutanéomuqueux.
- Les infections à virus varicelle-zona (VZV)
Pour le zona, aciclovir, valaciclovir et famciclovir ont des indications décrites dans les RCP, en particulier pour le zona ophtalmique. Un impératif : débuter le traitement le plus tôt possible, dans les 72 premières heures. Chez l'immunodéprimé, et en cas de zona généralisé, le recours à la voie parentérale est nécessaire.
Avec 45 ans de recul, l'aciclovir a été et reste un progrès majeur pour le traitement des infections à HSV et VZV, surtout dans les formes graves, généralisées et chez les immunodéprimés.
Par ailleurs, la prévention de la varicelle par la vaccination (VARILRIX) est recommandée dans une dizaine de situations précisées dans le calendrier vaccinal. La prévention du zona par le vaccin ZOSTAVAX est possible et indiquée chez les sujets de plus de cinquante ans.
Quelles pistes dans la COVID-19 ?
Dès la pandémie COVID-19 identifiée, des centaines de recherches ont été lancées pour trouver LE traitement antiviral.
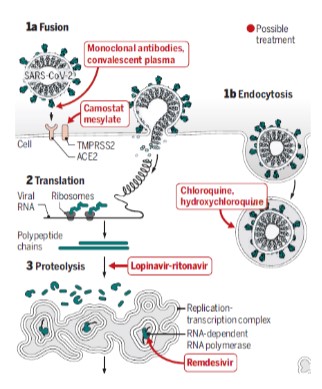
Les cibles possibles sont nombreuses comme le montre le schéma ci-dessous (Figure 2).
Figure 2 - Experimental treatment strategies attempt to interfere with different steps in the coronavirus replication cycle (Science 2020 Vol. 367, p. 1412)
Le 27 février 2020, l'"International Journal of Infectious Diseases" citait 31 médicaments apparaissant comme des candidats possibles pour la prophylaxie et le traitement des infections à SARS-CoV-2. Tous étaient des molécules anciennes, ayant déjà démontré qu'elles étaient sûres chez l'homme et qui constitueraient donc, dans l'attente de nouvelles molécules, de bonnes options pour le traitement de la COVID-19.
On peut citer : le baricitinib, le lopinavir, le darunavir, le favipiravir, le remdésivir, la ribavirine, le galidésivir, la chloroquine, et beaucoup d'autres, y compris des antibiotiques comme la téicoplanine, l'oritavancine, la dalbavancine, l'azitromycine.
Pour l'instant, y a-t-il un médicament qui ait fait la preuve indubitable de son efficacité : NON.
Pourtant, deux substances ont été très médiatisées :
- la chloroquine (ou plus exactement l'hydroxychloroquine). Or, il n'existe à ce jour aucune preuve de son efficacité ;
- le remdésivir a été au centre d'une saga qui aboutit aujourd'hui à un avis de la CT française en date du 16 septembre 2020, contenant des phrases sévères : "Ces données ne permettent pas de conclure de manière robuste sur l'efficacité selon le stade de la maladie ni sur la durée optimale de traitement [...] La Commission regrette et s'étonne que l'activité antivirale du remdésivir n'ait pas été évaluée dans les études fournies, en dehors de l'étude chinoise dans laquelle il n'a pas été mis en évidence d'activité du remdésivir sur la charge virale".
La CT considère que le service médical rendu (SMR) par le remdésivir est :
- faible dans la prise en charge des patients avec une pneumonie nécessitant une oxygénothérapie à faible débit ;
- insuffisant dans la prise en charge par la solidarité nationale chez les patients avec une pneumonie nécessitant une oxygénothérapie à haut débit, ou une oxygénothérapie lors de la ventilation assistée non invasive ou invasive ou une oxygénothérapie par membrane extracorporelle (ECMO).
Rien n'est terminé, mais au 23 septembre 2020 il ne s'agit pas d'un succès franc et massif.
Les résultats d'un premier essai japonais viennent d'être publiés au Japon concernant le favipiravir. La réduction de quelques jours de l'évolution ne permet à ce jour aucune conclusion supérieure à celle du remdésivir.
On ne peut terminer cette présentation sur les difficultés d'inventer des médicaments antiviraux, sans rappeler qu'on dispose aujourd'hui de 16 vaccins contre des virus. Quatorze sont recommandés par le calendrier vaccinal ou lors de voyages ; deux sont en instance : celui de la dengue (DENGVAXIA) qui pose encore pas mal de problèmes, et celui, très récent, contre le virus Ebola (ERVEBO), dont on ne sait pas encore exactement la place qu'il occupera.
Le vaccin espéré pour l'infection à SARS-CoV-2 sera peut-être la solution, ...
Un peu (beaucoup) de patience...
Copyright©vidal.fr
Pour en savoir plus
- Trémolières F. Le naufrage des « essais cliniques » ! Ou comment les méfaits d'un virus ont pu mettre à mal la rigueur et compromettre la réponse à l'urgence. Med Mal Infect 2020 ; 50 (6) : 461-465.
- Escuret V, Frobert E et Lina B. Grippe et antiviraux. Réanimation 2011 ; 20 : 169-177.
- Kai Kupferschmidt, Jon Cohen. Race to find COVID-19 treatments accelerates. Science 2020 ; 367 (6485) : 1412-1413.
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 12 minutes
12 minutes 11 commentaires
11 commentaires 






Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.