Représentation en 3D d'une plaque de cholestérol dans les parois d'une artère (illustration).
Résumé :
La gamme de l'anticorps monoclonal PRALUENT (alirocumab), indiqué dans la prise en charge de certaines hypercholestérolémies, s'enrichit d'un nouveau dosage : PRALUENT 300 mg solution injectable en stylo prérempli.
Chez les patients pour qui ce dosage est adapté, le schéma posologique est réduit à 1 injection mensuelle, au lieu de 1 injection tous les 15 jours avec le dosage à 150 mg déjà existant.
PRALUENT 300 mg est conditionné en boîte unitaire dont le prix public s'élève à 472,20 euros TTC. Il est agréé aux collectivités et remboursable à 65 % selon la procédure des médicaments d'exception et après demande d'accord préalable auprès de l'Assurance maladie.
Comme pour les autres dosages de PRALUENT (75 mg et 150 mg), le périmètre de remboursement de PRALUENT 300 mg est restreint par rapport aux indications prévues par l'autorisation de mise sur le marché (AMM).
Une nouvelle spécialité PRALUENT, dosée à 300 mg d'alirocumab, est mise à disposition en ville et à l'hôpital, PRALUENT 300 mg solution injectable en stylo prérempli, en complément de PRALUENT 75 mg et PRALUENT 150 mg solutions injectables en stylo prérempli, avec lesquels il partage les mêmes indications (cf. Encadré 1).La gamme de l'anticorps monoclonal PRALUENT (alirocumab), indiqué dans la prise en charge de certaines hypercholestérolémies, s'enrichit d'un nouveau dosage : PRALUENT 300 mg solution injectable en stylo prérempli.
Chez les patients pour qui ce dosage est adapté, le schéma posologique est réduit à 1 injection mensuelle, au lieu de 1 injection tous les 15 jours avec le dosage à 150 mg déjà existant.
PRALUENT 300 mg est conditionné en boîte unitaire dont le prix public s'élève à 472,20 euros TTC. Il est agréé aux collectivités et remboursable à 65 % selon la procédure des médicaments d'exception et après demande d'accord préalable auprès de l'Assurance maladie.
Comme pour les autres dosages de PRALUENT (75 mg et 150 mg), le périmètre de remboursement de PRALUENT 300 mg est restreint par rapport aux indications prévues par l'autorisation de mise sur le marché (AMM).
Ce nouveau dosage à 300 mg se distingue par un schéma posologique réduit à 1 injection mensuelle (1 fois toutes les 4 semaines), au lieu de 1 injection tous les 15 jours avec les deux autres dosages de PRALUENT (75 mg et 150 mg).
Encadré 1 - Indications thérapeutiques de PRALUENT
Hypercholestérolémie primaire (hétérozygote familiale et non familiale) ou une dyslipidémie mixte de l'adulte, en complément d'un régime alimentaire (cf. VIDAL Reco "Dyslipidémies") :
|
Évaluation médico-économique de PRALUENT 300 mg
Dans un avis du 3 février 2021, la Commission de la Transparence a évalué PRALUENT 300 mg et son schéma posologique mensuel sur la base notamment de l'étude CHOICE I de 48 semaines, multicentrique, en double insu, contrôlée versus placebo (cf. Monographie VIDAL de PRALUENT 300 mg - Rubrique Pharmacodynamie).
Sur la base des données disponibles et comme pour les autres dosages (75 mg et 150 mg), les conclusions de la CT sur PRALUENT 300 mg diffèrent selon l'indication thérapeutique et la population cible :
- dans l'hypercholestérolémie familiale hétérozygote :
- le service médical rendu (SMR) attribué est important en association à un traitement hypolipémiant optimisé chez les patients adultes ayant une hypercholestérolémie familiale hétérozygote, insuffisamment contrôlée et nécessitant un traitement par LDL-aphérèse ;
- le SMR est jugé insuffisant dans les autres populations de l'autorisation de mise sur le marché (AMM) ;
- dans la maladie cardiovasculaire athéroscléreuse établie :
- le SMR est considéré comme important uniquement en association à un traitement hypolipémiant optimisé chez les patients adultes ayant une maladie cardiovasculaire athéroscléreuse établie par un antécédent de SCA récent (prévention secondaire) et qui ne sont pas contrôlés (LDL-c > 0,7 g/L) malgré un traitement hypolipémiant optimisé comprenant au moins une statine à la dose maximale tolérée ;
- le SMR est jugé insuffisant dans les autres populations de l'indication, incluant notamment PRALUENT (alirocumab) en monothérapie ou en association avec d'autres thérapies hypolipémiantes chez :
- les patients intolérants aux statines ou chez qui les statines sont contre-indiquées,
- ou les patients avec une maladie cardiovasculaire athéroscléreuse établie autre qu'un antécédent de SCA récent,
- ou les patients qui n'ont pas d'hypercholestérolémie associée,
- ou les patients ne recevant pas un traitement optimisé par au moins une statine à la dose maximale tolérée.
PRALUENT 300 mg en pratique
Le schéma posologique de PRALUENT 300 mg est de 1 injection sous-cutanée (SC) toutes les 4 semaines.
Pour rappel, avec les autres dosages de PRALUENT (75 mg et 150 mg), le schéma posologique comporte 1 injection toutes les 2 semaines (soit 2 injections par mois).
Selon les recommandations du résumé des caractéristiques du produit (RCP) de PRALUENT, la dose initiale habituelle d'alirocumab est de 75 mg toutes les 2 semaines.
Les patients qui nécessitent une diminution plus importante du taux de LDL-C (> 60 %) peuvent démarrer le traitement à la dose de 150 mg toutes les 2 semaines ou 300 mg 1 fois par mois (cf. Monographie VIDAL de PRALUENT 300 mg - Rubrique Posologie).
Le stylo prérempli
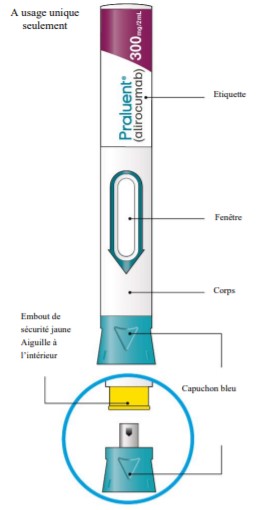 PRALUENT 300 mg solution injectable se présente en stylo prérempli (2 mL) prêt à l'emploi, à usage unique.
PRALUENT 300 mg solution injectable se présente en stylo prérempli (2 mL) prêt à l'emploi, à usage unique. Ce stylo est conçu pour réaliser une injection sous cutanée (SC) dans la cuisse, l'abdomen ou le haut du bras. Il est recommandé d'alterner les sites d'injection à chaque injection.
Pour déclencher l'injection, le stylo doit être appuyé fermement contre la peau et maintenu enfoncé. Une fenêtre de contrôle permet de suivre l'injection.
Avant utilisation, le stylo doit être sorti du réfrigérateur pour amener la solution à température ambiante.
Identité administrative
- Liste I
- Prescription initiale annuelle réservée aux spécialistes en cardiologie, en endocrinologie-diabétologie-nutrition ou en médecine interne
- Renouvellement non restreint
- Boîte de 1 stylo pré-rempli de 2 mL, CIP 3400930215616
- Remboursable à 65 % selon la procédure des médicaments d'exception (Fiche d'information thérapeutiques publiée au Journal officiel du 8 juillet 2021, texte 14) et selon la procédure d'accord préalable (Journal officiel du 8 juillet 2021, texte 16)
- Prix public TTC = 472,20 euros
- Agrément aux collectivités (Journal officiel du 8 juillet 2021, texte 15)
- Laboratoire sanofi-aventis France
Encadré 2 - Périmètre et modalités de prise en charge de PRALUENT 300 mg
PRALUENT 300 mg est remboursable et agréé aux collectivités uniquement :
Depuis le 15 décembre 2020, la prise en charge par l'Assurance maladie de toute prescription (initiale et renouvellement) d'un traitement par PRALUENT est subordonnée à l'accord préalable du service du contrôle médical. La demande d'accord préalable est applicable à toutes les indications thérapeutiques susceptibles d'ouvrir droit à une prise en charge. |
Pour aller plus loin
Avis de la Commission de la Transparence - PRALUENT (HAS, 3 février 2021)
Sur VIDAL.fr
REPATHA ET PRALUENT : PRISE EN CHARGE SOUMISE À UNE DEMANDE D'ACCORD PRÉALABLE DÈS LE 15 DÉCEMBRE 2020 (10 décembre 2020)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.