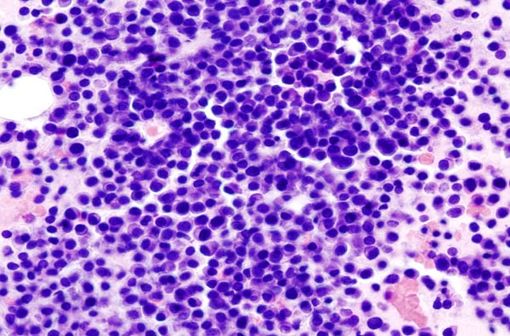
Image histopathologique d'un myélome multiple (extrait de la moelle osseuse). Coloration à l'hématoxyline et à l'éosine (illustration @Wikimedia).
La prise en charge de DARZALEX (daratumumab) dans le cadre de son agrément aux collectivités est étendue à l'indication suivante :
- en association avec le bortézomib, le thalidomide et la dexaméthasone pour le traitement des patients adultes atteints d'un myélome multiple nouvellement diagnostiqué et éligibles à une autogreffe de cellules souches.
Cette extension de prise en charge s'applique aux deux spécialités DARZALEX actuellement commercialisées en France :
- DARZALEX 1 800 mg (120 mg/mL) solution injectable pour administration sous-cutanée (SC), en flacon de 15 mL (CIP 3400930212202) ;
- DARZALEX 20 mg/mL solution à diluer pour perfusion intraveineuse (IV) en flacon de 20 mL (CIP 3400955021810) et de 5 mL (CIP 3400955021803).
Encadré 1 - Indications thérapeutiques de DARZALEX
DARZALEX est indiqué dans le traitement du myélome multiple (cf. VIDAL Reco "Myélome multiple"), selon plusieurs combinaisons :
|
Un SMR important en raison de la supériorité de l'association daratumumab, bortézomib, thalidomide et dexaméthasone
DARZALEX en association avec le bortézomib, le thalidomide et la dexaméthasone a fait l'objet d'une évaluation médico-économique par la Commission de la Transparence (CT) au premier trimestre 2020, à l'issue de laquelle la CT a attribué :
- un service médical rendu (SMR) important ;
- une amélioration du service médical rendu mineure (ASMR IV) par rapport au protocole VTd* dans le traitement des patients adultes atteints d'un myélome multiple nouvellement diagnostiqué et éligibles à une autogreffe de cellules souches.
Dans le cadre de cette évaluation, la CT a pris en compte les données de l'étude de phase 3 CASSIOPEIA (cf. Encadré 2) qui démontrent la supériorité de l'ajout de DARZALEX (D) au bortézomib, au thalidomide et à la dexaméthasone (protocole D-VTd) par rapport au protocole VTd administré seul, à l'issue de 4 cycles d'induction suivis de 2 cycles de consolidation, en termes de survie sans progression (HR = 0,47, IC95 % [0,33 – 0,67], gain médian non quantifiable à ce jour).
Encadré 2 - L'étude CASSIOPEIA en synthèse
| L'étude CASSIOPEIA* est une étude de phase 3, randomisée, comparative, en ouvert. Cette étude a inclus 1 085 patients ayant un myélome multiple nouvellement diagnostiqué, éligibles à une chimiothérapie intensive associée à une autogreffe de cellules souches périphériques L'étude comporte 2 phases :
*Moreau P, Attal M, Hulin C et al. Bortezomib, thalidomide, and dexamethasone with or without daratumumab before and after autologous stem-cell transplantation for newly diagnosed multiple myeloma (CASSIOPEIA): a randomised, open- label, phase 3 study. 2019 |
En pratique : utilisation de DARZALEX en association avec le bortézomib, le thalidomide et la dexaméthasone
La posologie de DARZALEX en association avec le bortézomib, le thalidomide et la dexaméthasone est différente des autres schémas d'administration de DARZALEX.
Dans cette indication en effet, DARZALEX est administré selon un schéma séquencé induction/autogreffe de cellules souches/consolidation.
La dose de DARZALEX recommandée est de :
- 16 mg/kg de masse corporelle, administrée en perfusion IV selon le calendrier d'administration suivant (cf. Tableau I) ;
- ou 1 800 mg en solution injectable par voie sous-cutanée, administrée pendant environ 3 à 5 minutes, également selon le calendrier d'administration suivant (cf. Tableau I).
Tableau I - Calendrier d'administration de DARZALEX en association avec le bortézomib, le thalidomide et la dexaméthasone, par cycles de 4 semaines
| Phase de traitement | Semaines | Fréquence d'administration |
| Induction | Semaines 1 à 8 | Hebdomadaire (8 doses au total) |
| Semaines 9 à 16(a) | Toutes les 2 semaines (4 doses au total) |
|
| Interruption dans le but de démarrer la chimiothérapie haute dose suivie de l'autogreffe de cellules souches | ||
| Consolidation | Semaines 1 à 8 (b) | Toutes les 2 semaines (4 doses au total) |
(b) La première dose selon le calendrier d'administration toutes les 2 semaines est administrée en semaine 1, lors de la reprise du traitement consécutive à une autogreffe de cellules souches.
Pour aller plus loin
Arrêté du 7 avril 2021 modifiant la liste des spécialités pharmaceutiques agréées à l'usage des collectivités et divers services publics - DARZALEX (Journal officiel du 14 avril 2021 - texte 29)
Avis de la Commission de la Transparence - DARZALEX 20 mg/mL - Nouvelle indication (HAS, 22 avril 2020)
Avis de la Commission de la Transparence - DARZALEX 1 800 mg (HAS, 22 avril 2020)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.