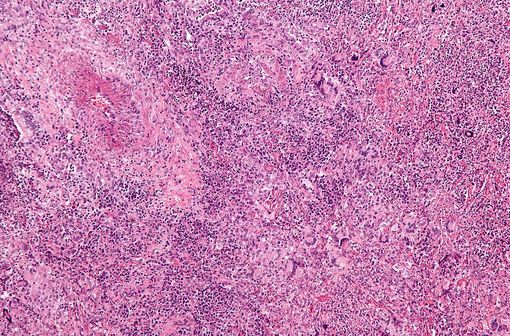
Coupe histologique caractéristique d’une granulomatose de Wegener : vascularite et granulomes accompagnés de cellules géantes polynucléées. Coloration H&E (illustration @Nephron sur Wikimedia).
Résumé :
La prise en charge (agrément aux collectivités et rétrocession) en population pédiatrique des spécialités biosimilaires hospitalières RIXATHON et TRUXIMA 100 mg et 500 mg solution à diluer pour perfusion (rituximab) est alignée sur celle de leur spécialité de référence MABTHERA, dans les indications suivantes :
La prise en charge (agrément aux collectivités et rétrocession) en population pédiatrique des spécialités biosimilaires hospitalières RIXATHON et TRUXIMA 100 mg et 500 mg solution à diluer pour perfusion (rituximab) est alignée sur celle de leur spécialité de référence MABTHERA, dans les indications suivantes :
- Granulomatose avec polyangéite (GPA, ou maladie de Wegener) et polyangéite microscopique (PMA) : traitement de première intention, en association aux glucocorticoïdes, pour l'induction de la rémission chez les patients pédiatriques âgés de 2 ans ou plus à < 18 ans.
- Lymphomes non hodgkiniens (LNH) : traitement de première intention en association à la chimiothérapie dans le traitement des patients pédiatriques âgés de 6 mois ou plus à < 18 ans, présentant un lymphome diffus à grandes cellules B (LDGCB) CD20 positif, un lymphome de Burkitt (LB)/une leucémie de Burkitt (leucémie aiguë à cellules B matures ou LA-B) ou un lymphome Burkitt-like (LB-like).
Les spécialités biosimilaires hospitalières à base de rituximab RIXATHON et TRUXIMA 100 mg et 500 mg solution à diluer pour perfusion (cf. Encadrés 1 et 2) bénéficient d'une extension de prise en charge en pédiatrie, dans le cadre de l'agrément aux collectivités et de la rétrocession :
- Granulomatose avec polyangéite (GPA, ou maladie de Wegener) et polyangéite microscopique (PMA) : la prise en charge est étendue au traitement de première intention, en association aux glucocorticoïdes, pour l'induction de la rémission chez les patients pédiatriques âgés de 2 ans et plus à < 18 ans.
- Lymphomes non hodgkiniens (LNH) : la prise en charge est étendue au traitement de première intention en association à la chimiothérapie des patients pédiatriques âgés de 6 mois et plus à < 18 ans, non précédemment traités présentant à un stade avancé : un lymphome diffus à grandes cellules B (LDGCB) CD20 positif, un lymphome de Burkitt (LB)/une leucémie de Burkitt (leucémie aiguë à cellules B matures ou LA-B) ou un lymphome Burkitt-like (LB-like).
Encadré 1 - Spécialités RIXATHON et TRUXIMA bénéficiant d'une extension de prise en charge en pédiatrie
|
Alignement du périmètre de prise en charge sur celui de MABTHERA
La prise en charge dans ces diverses indications pédiatriques est alignée sur celle de la spécialité référente MABTHERA.
Ces extensions de prise en charge ont fait l'objet d'une évaluation médico-économique par la Commission de la Transparence (CT), et deux avis ont été émis :
- Avis du 2 décembre 2020 pour MABTHERA dans le traitement de la GPA et PAM en population pédiatrique (cette extension d'indication a été octroyée en mars 2020) ;
- Avis du 6 janvier 2021 pour MABTHERA dans le traitement des LDGCB/LB/LA-B/LB-like pédiatriques.
Dans ces indications pédiatriques, le service médical rendu (SMR) attribué à MABTHERA est jugé important.
La CT a également attribué une amélioration du service médical rendu (ASMR) mineure à MABTHERA pour l'ensemble de ces indications en pédiatrie.
Avec cette extension de prise en charge, RIXATHON est désormais agréé aux collectivités et inscrit sur la liste de rétrocession dans toutes ses indications (cf. Encadré 2). Il en est de même pour TRUXIMA au titre de la rétrocession, mais pas de l'agrément aux collectivités qui est restreint dans le pemphigus vulgaris (cf. Rubrique Prescription/Délivrance/Prise en charge dans les monographies VIDAL de TRUXIMA 100 mg solution à diluer pour perfusion et de TRUXIMA 500 mg solution à diluer pour perfusion.
Encadré 2 - Rappel des indications thérapeutiques de RIXATHON et TRUXIMA
Lymphomes non hodgkiniens (LNH) :
Leucémie lymphoïde chronique (LLC) :
Polyarthrite rhumatoïde (cf. VIDAL Reco "Polyarthrite rhumatoïde") :
Granulomatose avec polyangéite (GPA) et polyangéite microscopique (PAM) :
Pemphigus vulgaris :
|
Utilisation du rituximab dans ses indications pédiatriques
Les posologies de RIXATHON/TRUXIMA en population pédiatrique sont décrites dans les monographies VIDAL (cf. Encadré 1).
Pour rappel, chez les patients pédiatriques atteints de GPA ou de PAM, avant la première perfusion IV de rituximab, il faut administrer de la méthylprednisolone à raison d'une dose quotidienne de 30 mg/kg/jour (sans dépasser 1 g/jour) par voie intraveineuse (IV) pendant 3 jours pour traiter les symptômes sévères de vascularite. Jusqu'à trois doses quotidiennes supplémentaires de 30 mg/kg de méthylprednisolone par voie IV peuvent être administrées avant la première perfusion de rituximab.
Une fois l'administration de la méthylprednisolone par voie IV terminée, les patients doivent recevoir de la prednisone orale à la dose de 1 mg/kg/jour (sans dépasser 60 mg/jour), avec réduction progressive de la dose aussi rapidement que possible en fonction de la clinique.
Pour aller plus loin
Arrêté du 27 avril 2021 modifiant la liste des spécialités pharmaceutiques agréées à l'usage des collectivités et divers services publics - RIXATHON et TRUXIMA (Journal officiel du 30 avril 2021, texte 78)
Arrêté du 27 avril 2021 relatif aux conditions de prise en charge de spécialités pharmaceutiques disposant d'une autorisation de mise sur le marché inscrites sur la liste de rétrocession - RIXATHON et TRUXIMA (Journal officiel du 30 avril 2021, texte 79)
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.