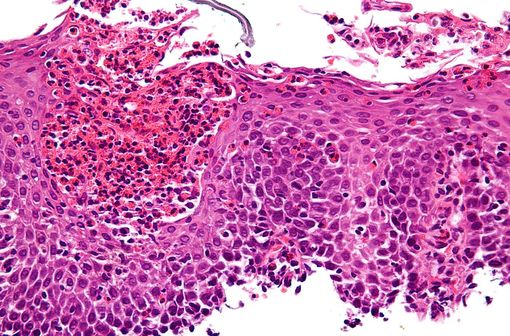
Micrographie à très fort grossissement d'une œsophagite à éosinophiles (illustration @Nephron sur Wikimedia).
Résumé
JORVEZA 1 mg comprimé orodispersible est une spécialité à base de budésonide per os, la première spécialité à disposer d'une autorisation de mise sur le marché (AMM) dans le traitement de l'œsophagite à éosinophiles (OeE) de l'adulte.
JORVEZA se présente en comprimé orodispersible, à laisser se désagréger dans la bouche au contact de la salive. Ce comprimé doit être pris après un repas, sans eau et sans nourriture.
Le schéma posologique comporte 2 prises par jour (matin et soir).
On distingue la posologie d'induction de la rémission (de 6 à 12 semaines selon la réponse au traitement) et la posologie d'entretien de la rémission (durée déterminée par le médecin traitant).
En raison d'interactions pouvant dégrader le profil de tolérance du budésonide, l'administration concomitante de JORVEZA et d'inhibiteurs puissants du CYP3A (dont le jus de pamplemousse) doit être évitée.
JORVEZA est agréé aux collectivités et remboursable à 65 %, uniquement chez les patients adultes non répondeurs aux inhibiteurs de la pompe à protons (utilisés hors AMM). Son prix public s'élève à 396,68 euros (une plaquette de 90 comprimés).
La prescription initiale annuelle est réservée aux spécialistes en hépato-gastro-entérologie. Le renouvellement n'est pas restreint.
JORVEZA 1 mg comprimé orodispersible est une spécialité à base de budésonide per os, la première spécialité à disposer d'une autorisation de mise sur le marché (AMM) dans le traitement de l'œsophagite à éosinophiles (OeE) de l'adulte.
JORVEZA se présente en comprimé orodispersible, à laisser se désagréger dans la bouche au contact de la salive. Ce comprimé doit être pris après un repas, sans eau et sans nourriture.
Le schéma posologique comporte 2 prises par jour (matin et soir).
On distingue la posologie d'induction de la rémission (de 6 à 12 semaines selon la réponse au traitement) et la posologie d'entretien de la rémission (durée déterminée par le médecin traitant).
En raison d'interactions pouvant dégrader le profil de tolérance du budésonide, l'administration concomitante de JORVEZA et d'inhibiteurs puissants du CYP3A (dont le jus de pamplemousse) doit être évitée.
JORVEZA est agréé aux collectivités et remboursable à 65 %, uniquement chez les patients adultes non répondeurs aux inhibiteurs de la pompe à protons (utilisés hors AMM). Son prix public s'élève à 396,68 euros (une plaquette de 90 comprimés).
La prescription initiale annuelle est réservée aux spécialistes en hépato-gastro-entérologie. Le renouvellement n'est pas restreint.
La spécialité JORVEZA 1 mg comprimé orodispersible (budésonide) est indiquée dans le traitement de l'œsophagite à éosinophiles (OeE) chez les adultes (âgés de plus de 18 ans).
Le budésonide per os en allergologie/immunologie
Le budésonide est un glucocorticoïde à visée anti-inflammatoire.
La plupart des spécialités à base de budésonide commercialisées en France sont administrées par voie respiratoire, en inhalation, dans le traitement de l'asthme et de la bronchopneumopathie chronique obstructive (BPCO).
Le budésonide par voie orale existe déjà dans le domaine de la gastro-entérologie, notamment dans le traitement de la maladie de Crohn (MIKICORT granulé gastrorésistant ou gélule gastrorésistante, ENTOCORT gélule) et de la rectocolite hémorragique (CORTIMENT 9 mg comprimé LP).
JORVEZA correspond à la première spécialité à base de budésonide per os disposant d'une autorisation de mise sur le marché (AMM) dans le traitement de l'œsophagite à éosinophiles (cf. Encadré 1).
Il s'agit d'un médicament orphelin, en raison de la faible prévalence de cette maladie (de 1 à 5 pour 10 000).
Encadré 1 - Œsophagite à éosinophiles : physiopathologie et traitement [1]
| L'œsophagite à éosinophiles est une pathologie œsophagienne chronique d'origine allergique et dysimmunitaire caractérisée par une réaction inflammatoire locale au sein de laquelle prédominent les éosinophiles. Il s'agit d'une forme d'allergie alimentaire, la plupart des allergènes responsables provenant de l'alimentation. Les patients relevant d'un traitement médicamenteux sont actuellement pris en charge par des traitements prescrits hors AMM (inhibiteurs de la pompe à protons et corticoïdes topiques à déglutir, dont le budésonide). |
JORVEZA : un traitement de seconde intention, après les IPP selon la CT
Dans son avis du 9 septembre 2020 [1], la Commission de la transparence (CT) a évalué JORVEZA sur la base principalement de deux études cliniques de phase III de supériorité conduites versus placebo chez des patients atteints d'OeE et non répondeurs aux inhibiteurs de la pompe à protons (IPP).
Des résultats en faveur de la supériorité de JORVEZA par rapport au placebo
Selon les résultats de ces études, la supériorité de JORVEZA a été démontrée versus placebo sur le taux de rémission histologique et clinique (critère de jugement principal) à 6 semaines, et le maintien de cette rémission à 48 semaines :
- étude BUL-1/EEA [2] : taux de rémission clinico-pathologique à 6 semaines de l'ordre de 57,6 % dans le groupe budésonide versus 0 % dans le groupe placebo, soit une différence absolue de 55,6% IC95% [26,97%; 73,57%], p<0,001 ;
- l'étude BUL-2/EER (48 semaines), réalisée avec 2 posologies de budésonide (0,5 mg ou 1 mg 2 fois par jour) :
- taux de patients en rechute histologique de 13,2 % (budésonide 0,5 mg) et 10,3 % (budésonide 1 mg) contre 89,7 % dans le groupe placebo ;
- modification du pic d'éosinophiles/mm2 CFG (champ à fort grossissement) depuis l'inclusion : respectivement +38 (budésonide 0,5 mg), +21 (budésonide 1 mg) et +262 (placebo),
- taux de patients en rechute clinique, ayant subi une impaction alimentaire nécessitant une intervention endoscopique ou nécessitant une dilatation endoscopique : respectivement 10,3 % (budésonide 0,5 mg), 7,4 % (budésonide 1 mg) et 60,3 % (placebo) ;
- taux de patients avec un score EEsAI-PRO (Eosinophilic Esophagitis Activity Index - Patient - Reported Outcome) hebdomadaire total < 20 : respectivement 72,1 % (budésonide 0,5 mg), 73,5 % (budésonide 1 mg) et 20,6 % (placebo) ;
- taux de patients en rémission profonde de la maladie : respectivement 39,7 % (budésonide 0,5 mg), 52,9 % (budésonide 1 mg) et 0,0 % (placebo).
Un périmètre de prise en charge restreint par rapport à l'AMM
Au terme de son évaluation, la CT a attribué à JORVEZA un service médical rendu (SMR) important uniquement chez les patients non répondeurs aux IPP.
Dans cette indication restreinte, une amélioration du service médical rendu mineure (ASMR IV) a été attribuée du fait que JORVEZA apporte une réponse partielle au besoin médical identifié couvert (jusqu'à présent, par des médicaments utilisés hors AMM et par des protocoles d'éviction/réintroduction alimentaire).
Faute de données disponibles, le SMR est jugé insuffisant chez les patients répondeurs aux IPP, au regard des alternatives disponibles. Par conséquent, le périmètre de prise en charge de JORVEZA est limité aux patients souffrant d'OeE, en seconde intention chez les non-répondeurs aux IPP (cf. Encadré 2).
JORVEZA en pratique : posologie et consignes de bon usage
Le traitement par JORVEZA doit être instauré par un médecin expérimenté en matière de diagnostic et de traitement de l'OeE.
Posologie : induction ou entretien de la rémission
En induction de la rémission, la dose journalière recommandée est de 2 mg de budésonide en 2 prises, soit :
- 1 comprimé de 1 mg le matin et 1 comprimé de 1 mg le soir.
En entretien de la rémission, la dose journalière recommandée est définie selon les besoins cliniques du patient :
- 1 mg de budésonide en 2 prises, soit 1 comprimé de 0,5 mg le matin et 1 comprimé de 0,5 mg le soir (dosage non commercialisé au 16 mai 2022),
- ou 2 mg de budésonide en 2 prises, soit 1 comprimé de 1 mg le matin et 1 comprimé de 1 mg le soir.
La durée du traitement d'entretien est déterminée par le médecin traitant.
Consignes d'administration du comprimé orodispersible
JORVEZA se présente en comprimé orodispersible. Celui-ci doit se désagréger dans la bouche, en au moins 2 minutes, et jusqu'à 20 minutes. Au fur et à mesure que le comprimé se désagrège, le patient doit déglutir. Le comprimé orodispersible ne doit être ni mâché ni avalé avant d'avoir été dissous, afin d'assurer une exposition optimale de la muqueuse œsophagienne à la substance active.
Les consignes d'administration de JORVEZA sont les suivantes :
- prendre le comprimé immédiatement après son retrait de la plaquette ;
- prendre le comprimé après un repas, sans liquide et sans nourriture ;
- placer le comprimé sur le bout de la langue et le presser légèrement contre le palais pour qu'il se désagrège ;
- après l'administration de JORVEZA, attendre au moins 30 minutes avant de manger, boire, se laver les dents, ou d'administrer d'autres médicaments formulés en solution buvable, pulvérisation ou comprimé à mâcher.
Attention au pamplemousse et à certains médicaments
L'utilisation concomitante de JORVEZA doit être évitée avec les inhibiteurs puissants du CYP3A (évaluer le rapport bénéfice-risque) :
- les médicaments : kétoconazole, ritonavir, itraconazole, clarithromycine, cobicistat ;
- le jus de pamplemousse.
Identité administrative
Liste I
Prescription initiale annuelle réservée aux spécialistes en hépato-gastro-entérologie
Renouvellement non restreint
JORVEZA 1 mg, boîte de 90, CIP 3400930200193
Remboursable à 65 % (cf. Encadré 2 - Journal officiel du 12 avril 2022 - texte 19)
Prix public TTC = 396,68 euros
Agrément aux collectivités (cf. Encadré 2 - Journal officiel du 12 avril 2022 - texte 20)
Laboratoire Dr Falk Pharma
Encadré 2 - Périmètre de prise en charge de JORVEZA
| Traitement de l'œsophagite à éosinophiles (OeE) chez les adultes (âgés de plus de 18 ans) uniquement chez les patients non répondeurs aux IPP. |
Pour aller plus loin
[1] Avis de la Commission de la transparence - JORVEZA (HAS, 9 septembre 2020)
[2] Lucendo AJ, Miehlke S, Schlag C et al. Efficacy of Budesonide Orodispersible Tablets as Induction Therapy for Eosinophilic Esophagitis in a Randomized Placebo-Controlled Trial. Gastroenterology, 2019 Jul;157(1):74-86.e15
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.