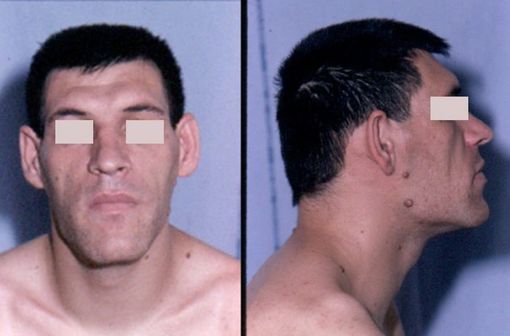
Visage d'un patient souffrant d'acromégalie (illustration @Philippe Chanson and Sylvie Salenave - Acromegaly. Orphanet Journal of Rare Diseases 2008, 3:17, sur Wikimedia).
Résumé
La commercialisation de SOMATULINE LP 30 mg poudre et solvant pour suspension injectable LP (lanréotide) sera arrêtée à partir du 30 septembre 2022.
Au-delà de cette date, seules les spécialités SOMATULINE LP solution injectable en seringue préremplie (dosages à 60 mg, 90 mg et 120 mg) seront maintenues sur le marché. Elles représentent une alternative thérapeutique dans les indications suivantes, en tenant compte des différentes voies d'injection (intramusculaire pour SOMATULINE LP 30 mg, sous-cutanée profonde pour les autres) :
La commercialisation de SOMATULINE LP 30 mg poudre et solvant pour suspension injectable LP (lanréotide) sera arrêtée à partir du 30 septembre 2022.
Au-delà de cette date, seules les spécialités SOMATULINE LP solution injectable en seringue préremplie (dosages à 60 mg, 90 mg et 120 mg) seront maintenues sur le marché. Elles représentent une alternative thérapeutique dans les indications suivantes, en tenant compte des différentes voies d'injection (intramusculaire pour SOMATULINE LP 30 mg, sous-cutanée profonde pour les autres) :
- traitement de l'acromégalie ;
- traitement des symptômes cliniques des tumeurs carcinoïdes.
L'arrêt de commercialisation de SOMATULINE LP 30 mg poudre et solvant pour suspension injectable à libération prolongée (LP) (lanréotide) est programmé au 30 septembre 2022 [1].
Cette spécialité antihormone de croissance, la seule de la gamme SOMATULINE présentée en poudre et solvant à reconstituer (cf. Encadrés 1 et 2) pour voie intramusculaire (IM), est commercialisée depuis 1995 (source ANSM).
Elle est indiquée dans le traitement :
- de l'acromégalie : lorsque les taux circulants d'hormone de croissance (GH) et d'IGF-1 ne sont pas normalisés après chirurgie et/ou radiothérapie ou lorsque la chirurgie et/ou la radiothérapie ne peuvent pas être envisagées ;
- des symptômes cliniques des tumeurs carcinoïdes ;
- des adénomes thyréotropes primitifs responsables d'une hyperthyroïdie : en préparation ou en complément de la chirurgie et/ou de la radiothérapie, ou lorsque ces thérapeutiques ne sont pas appropriées.
Encadré 1 - Gamme SOMATULINE (juin 2022) : quatre dosages, deux formes pharmaceutiques
Forme à reconstituer avant emploi (voie intramusculaire) :
Forme prête à l'emploi (voie sous-cutanée profonde) :
|
Encadré 2 - Indications thérapeutiques de SOMATULINE LP solution injectable en seringue préremplie
Acromégalie :
Tumeurs neuroendocrines :
|
Alternatives à SOMATULINE LP 30 mg indication par indication
Pour pallier la disparition de SOMATULINE LP 30 mg, des alternatives existent en fonction des indications thérapeutiques.
Acromégalie, tumeurs carcinoïdes : report vers les autres spécialités de SOMATULINE
Les autres dosages de SOMATULINE (60 mg, 90 mg et 120 mg) restent disponibles, et représentent une alternative à SOMATULINE LP 30 mg dans :
- le traitement de l'acromégalie (cf. Encadré 3) ;
- le traitement des symptômes cliniques des tumeurs carcinoïdes : la dose initiale recommandée est de 90 mg tous les 28 jours (4 semaines) pendant 2 mois.
Il faut tenir compte des différences en termes de voie d'injection entre SOMATULINE LP 30 mg poudre et solvant pour suspension injectable et SOMATULINE LP solution injectable en seringue préremplie :
- SOMATULINE LP 30 mg poudre et solvant pour suspension injectable : injection de la suspension reconstituée par voie intramusculaire (IM) ;
- SOMATULINE LP solution injectable en seringue préremplie : injection par voie sous-cutanée (SC) profonde.
Encadré 3 - Traitement de l'acromégalie : relais de SOMATULINE LP 30 mg à un autre dosage de SOMATULINE LP
La posologie recommandée varie de 60 à 120 mg tous les 28 jours :
Les seringues préremplies SOMATULINE sont conçues pour une injection sous-cutanée profonde. |
Traitement des adénomes thyréotropes primitifs
Les spécialités SOMATULINE LP solution injectable en seringue préremplie ne disposent pas de l'indication dans le traitement des adénomes thyréotropes primitifs.
Pour remplacer SOMATULINE LP 30 mg dans cette indication, les alternatives sont les spécialités d'octréotide enregistrées dans cette indication.
Pour aller plus loin
[1] Lettre du laboratoire aux professionnels de santé (Ipsen, 16 février 2022)
Pour aller plus loin
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.