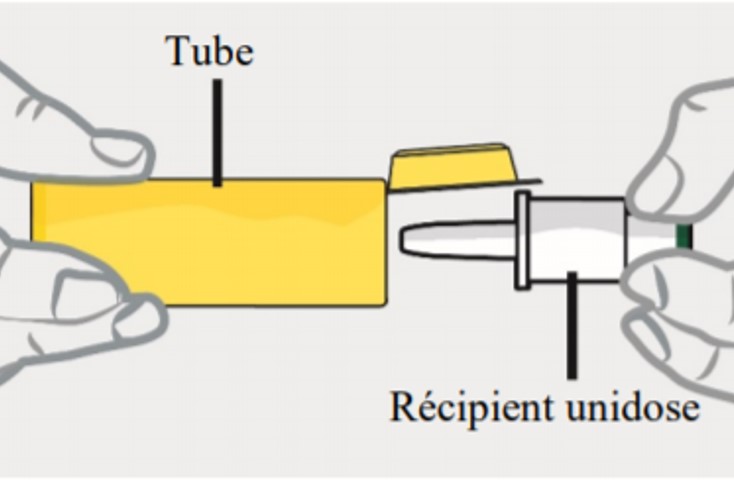
Représentation schématique du récipient unidose de BAQSIMI et du tube le contenant (illustration).
Une nouvelle spécialité à base de glucagon est désormais disponible, BAQSIMI 3 mg poudre nasale, la première à être administrée par voie nasale (cf. Encadré 1).
BAQSIMI est indiqué dans le traitement de l'hypoglycémie sévère chez les adultes, les adolescents et les enfants âgés de 4 ans et plus ayant un diabète (cf. VIDAL Reco "Diabète de type 1").
Encadré 1 - Spécialités de glucagon commercialisées en France
Jusqu'à présent, seules des spécialités à base de glucagon (sous forme chlorhydrate) sous forme injectable étaient commercialisées en France :
|
BAQSIMI en pratique
BAQSIMI est une poudre nasale blanche dosée à 3 mg de glucagon.
La poudre est contenue dans un récipient unidose (cf. Encadré 2) prêt à l'emploi, lui-même disposé dans un tube jaune/orangé scellé.
La durée de conservation de BAQSIMI est de 2 ans (à moins de 30 °C et dans le tube scellé, à l'abri de l'humidité).
Encadré 2 - Description du récipient unidose de BAQSIMI
Le récipient unidose est composé :
|
BAQSIMI peut être utilisé chez l'adulte, l'adolescent et l'enfant à partir de 4 ans.
Il doit être administré par voie nasale uniquement (cf. Encadré 3). Le glucagon est absorbé passivement à travers la muqueuse nasale. Il n'est pas nécessaire d'inhaler, ni d'inspirer profondément après l'administration.
La dose recommandée est de 3 mg de glucagon (dose contenue dans 1 récipient unidose), administrée dans une narine.
Le genre et le poids corporel n'ont pas eu d'effet cliniquement pertinent sur la pharmacodynamie du glucagon en poudre nasale. Après administration de 3 mg de glucagon en poudre nasale chez des adultes et des enfants (diabète de type 1), la glycémie a commencé à augmenter après seulement 5 minutes.
Encadré 3 - Instructions pour l'administration du glucagon en poudre nasale
(cf. Monographie Vidal de BAQSIMI - Rubrique Posologie et mode d'administration)
BAQSIMI est à usage unique et ne délivre qu'une dose de glucagon (3 mg). Aucun test ni manipulation d'amorçage n'est nécessaire avant l'utilisation.
|
- Liste I
- Non remboursable et non agréé aux collectivités (demandes à l'étude)
- Boîte de 1 récipient unidose, CIP 3400930195291
- Laboratoire Lilly
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.