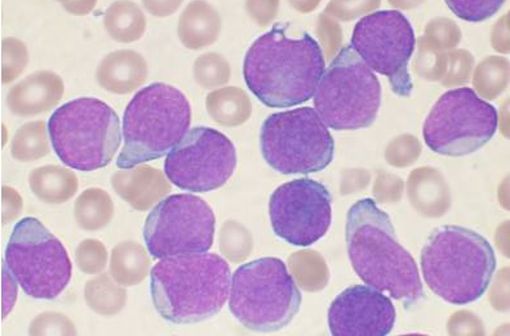
Frottis d'aspiration de moelle osseuse coloré par le test de Wright d'un patient atteint de leucémie lymphoblastique aiguë à cellules B précurseurs (illustration @VashiDonsk sur Wikimédia).
Résumé
L'agrément aux collectivités et la prise en charge en sus des GHS de BLINCYTO 38,5 µg injectable (blinatumomab) sont étendus au traitement des enfants de 1 an et plus, présentant une leucémie aiguë lymphoblastique (LAL) à précurseurs B (CD19+ et Ph-) en première rechute à haut risque, dans le cadre du traitement de consolidation.
Il s'agit de la deuxième indication pédiatrique remboursable pour BLINCYTO, pour laquelle la Commission de la transparence a attribué un service médical rendu (SMR) important et une amélioration du service médical rendu modérée (ASMR III).
Dans cette population, la posologie est définie en fonction du poids du patient :
L'agrément aux collectivités et la prise en charge en sus des GHS de BLINCYTO 38,5 µg injectable (blinatumomab) sont étendus au traitement des enfants de 1 an et plus, présentant une leucémie aiguë lymphoblastique (LAL) à précurseurs B (CD19+ et Ph-) en première rechute à haut risque, dans le cadre du traitement de consolidation.
Il s'agit de la deuxième indication pédiatrique remboursable pour BLINCYTO, pour laquelle la Commission de la transparence a attribué un service médical rendu (SMR) important et une amélioration du service médical rendu modérée (ASMR III).
Dans cette population, la posologie est définie en fonction du poids du patient :
- pour un poids de 45 kg ou plus : dose fixe de 28 µg/jour ;
- pour un poids inférieur à 45 kg : dose calculée à partir de la surface corporelle.
L'anticorps monoclonal à base de blinatumomab, BLINCYTO 38,5 µg poudre pour solution à diluer et solution pour solution pour perfusion bénéficie d'une extension de son agrément aux collectivités [1] et de sa prise en charge en sus de la GHS [2] chez les enfants, dans l'indication suivante :
- en monothérapie dans le traitement des patients pédiatriques à partir de l'âge de 1 an, présentant une leucémie aiguë lymphoblastique (LAL) à précurseurs B exprimant le CD19 avec chromosome Philadelphie négatif en première rechute à haut risque dans le cadre du traitement de consolidation.
Cette indication pédiatrique a été validée en mai 2021. Il s'agit de la seconde indication de BLINCYTO autorisée et prise en charge chez l'enfant (cf. Encadré ci-dessous).
Encadré - Indications thérapeutiques de BLINCYTO
Chez le patient adulte (cf. VIDAL Reco « Leucémies aiguës de l'adulte ») :
Chez le patient pédiatrique :
|
Évaluation médico-économique de BLINCYTO en traitement de consolidation
Dans un avis du 15 décembre 2021 [3], la Commission de la transparence (CT) a évalué l'efficacité de BLINCYTO dans cette indication pédiatrique sur la base de l'étude 20120215 de phase III, randomisée, en ouvert, contrôlée versus le 3e bloc de chimiothérapie intensive conventionnelle de consolidation (HC3) chez des enfants ou adolescents (âgés de 1 mois à 17 ans) atteints de LAL à précurseurs B Ph- après une 1re rechute à haut risque (cf. Figure ci-dessous).
La survie sans événement comme critère de jugement principal
- rechute de la maladie ;
- décès toute cause ;
- non atteinte d'une rémission complète (RC) à la fin du traitement à l'étude moelle de stade M2 après atteinte d'une RC ;
- diagnostic d'une tumeur secondaire.
Des résultats en faveur du blinatumomab
Les résultats de cette étude ont été en faveur de la supériorité du blinatumomab après un suivi médian de 22 mois (HR=0,36 ; IC95% [0,19 ; 0,66] ; p<0,001).
En outre, ils suggèrent un profil de tolérance favorable du blinatumomab, marqué par une plus faible hématotoxicité en comparaison à la chimiothérapie malgré des troubles généraux et neurologiques plus fréquents.
Un SMR important et une ASMR III
Sur la base des données disponibles au moment de cette évaluation, la CT a attribué à BLINCYTO dans le traitement pédiatrique de la LAL en première rechute à haut risque, dans le cadre d'un traitement de consolidation :
- un service médical rendu (SMR) important ;
- une amélioration du service médical rendu modérée (ASMR III).
En conclusion de son avis, la CT considère que la place de BLINCYTO dans la stratégie thérapeutique est celle d'un traitement à privilégier par rapport à la chimiothérapie conventionnelle en troisième bloc de consolidation pour le traitement des enfants ou adolescents à partir de l'âge de 1 an ayant une LAL à précurseurs B exprimant le CD19 en l'absence de chromosome Philadelphie, et ayant obtenu une rémission complète après une première rechute à haut risque.
BLINCYTO en traitement de consolidation chez l'enfant : en pratique
Pour les patients pédiatriques présentant une LAL à précurseurs B en première rechute à haut risque, l'hospitalisation est recommandée au moins pendant les 3 premiers jours du cycle.
Ces patients peuvent recevoir 1 cycle de traitement par BLINCYTO après l'induction et 2 blocs de chimiothérapie de consolidation. Un cycle de traitement est constitué de 28 jours (4 semaines) de perfusion continue.
Dose recommandée : en fonction du poids de l'enfant
La dose recommandée pour les patients pédiatriques en cycle de consolidation tient compte du poids de l'enfant :
- poids supérieur ou égal à 45 kg : dose fixe de 28 µg/jour ;
- poids inférieur à 45 kg : la dose est calculée selon la surface corporelle : 15 microgrammes/m2/jour (sans dépasser 28 microgrammes/jour).
BLINCYTO est un médicament réservé à l'usage hospitalier.
La prescription est réservée aux spécialistes en hématologie, ou aux médecins compétents en maladies du sang.
Une surveillance particulière doit être mise en place pendant le traitement.
Pour aller plus loin
[1] Arrêté du 7 mars 2022 modifiant la liste des spécialités pharmaceutiques agréées à l'usage des collectivités et divers services publics - BLINCYTO (Journal officiel du 12 mai 2022, texte 17)
[2] Arrêté du 30 mars 2022 modifiant la liste des spécialités pharmaceutiques prises en charge en sus des prestations d'hospitalisation mentionnée à l'article L. 162-22-7 du code de la sécurité sociale - BLINCYTO (Journal officiel du 12 mai 2022, texte 18)
[3]Avis de la Commission de la transparence - BLINCYTO (HAS, 15 décembre 2021)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.