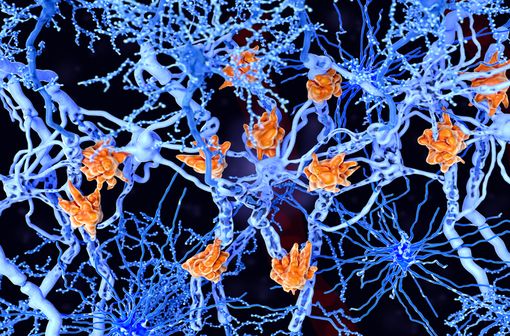
La SEP est une maladie inflammatoire et dégénérative du cerveau et de la moelle épinière qui entraîne la destruction de la gaine de myéline isolante autour des axones des neurones et la perte de la fonction nerveuse (illustration).
Comme TYSABRI 300 mg, TYSABRI 150 mg est indiqué en traitement de fond des formes très actives de sclérose en plaques rémittente-récurrente.
En revanche, cette nouvelle spécialité se distingue par :
- sa voie d'administration SC,
- son dosage à 150 mg,
- sa présentation en seringue préremplie prête à l'emploi.
TYSABRI 150 mg est réservé à l'usage hospitalier ; l'injection doit être réalisée par un professionnel de santé.
Le schéma posologique est de 300 mg toutes les 4 semaines, soit 2 injections de TYSABRI 150 mg toutes les 4 semaines. TYSABRI 150 mg est conditionné en boîte de 2 seringues préremplies.
Des mesures additionnelles de réduction du risque validées par l'ANSM sont diffusées par le laboratoire Biogen, parmi lesquelles un guide de prescription pour les professionnels de santé concernés, ainsi qu'une carte et une brochure à remettre au patient lors de l'instauration de TYSABRI, afin qu'il soit informé sur les principales consignes à respecter pendant le traitement et sur les signes évocateurs des principaux effets indésirables associés à ce médicament (LEMP).
La prescription de TYSABRI 150 mg est restreinte aux neurologues.
TYSABRI 150 mg est agréé aux collectivités.
L'arsenal thérapeutique de la sclérose en plaques rémittente-récurrente (cf. Encadré 1) compte une nouvelle spécialité à base de natalizumab, TYSABRI 150 mg solution injectable en seringue préremplie, en complément de TYSABRI 300 mg solution à diluer pour perfusion déjà disponible.
TYSABRI 150 mg versus TYSABRI 300 mg
TYSABRI 150 mg partage les mêmes indications que TYSABRI 300 mg (cf. Encadré 1), et le même schéma posologique :
- 300 mg de natalizumab 1 fois toutes les 4 semaines
Comme le dosage à 300 mg, TYSABRY 150 mg est réservé à l'usage hospitalier et sa prescription est restreinte aux spécialistes en neurologie. Les modalités de surveillance sont identiques.
Encadré 1 - Indications thérapeutiques de TYSABRI 150 mg et 300 mg
En monothérapie, traitement de fond chez les adultes présentant des formes très actives de sclérose en plaques rémittente-récurrente (SEP-RR) pour les groupes de patients suivants (cf. VIDAL Reco "Sclérose en plaques") :
|
En revanche, cette nouvelle spécialité de la gamme TYSABRI se distingue par sa voie d'administration, son dosage et sa présentation :
- solution injectable administrée par voie sous-cutanée (SC),
- dosée à 150 mg de natalizumab,
- en seringue préremplie prête à l'emploi.
Sécurité, tolérance et efficacité de la forme SC
La forme TYSABRI par voie SC a été évaluée dans 2 études :
- Étude clinique de phase II (REFINE) randomisée, en aveugle et menée en groupes parallèles, ayant exploré la sécurité, la tolérance et l'efficacité de plusieurs schémas thérapeutiques du natalizumab (300 mg IV toutes les 4 semaines, 300 mg SC toutes les 4 semaines, 300 mg IV toutes les 12 semaines, 300 mg SC toutes les 12 semaines, 150 mg IV toutes les 12 semaines et 150 mg SC toutes les 12 semaines) chez des patients déjà traités par natalizumab en perfusion IV :
- le critère d'évaluation principal était le nombre cumulé de lésions IRM actives uniques combinées (somme des nouvelles lésions Gd+ à l'IRM cérébrale et des nouvelles lésions hyperintenses en T2 ou de celles qui ont récemment augmenté de volume et qui ne sont pas associées au Gd+ à l'examen pondéré en T1) ;
- la moyenne des lésions uniques combinées pour le groupe 300 mg par voie SC toutes les 4 semaines a été faible (0,02) et comparable à celle du groupe 300 mg par voie IV toutes les 4 semaines (0,23) ; le nombre de lésions uniques combinées dans les groupes de traitement toutes les 12 semaines était significativement plus élevé que dans les groupes de traitement toutes les 4 semaines, ce qui a entraîné l'arrêt prématuré des groupes de traitement toutes les 12 semaines.
- Étude clinique de phase I, DELIVER, randomisée, en ouvert, avec détermination de la dose, ayant évalué l'efficacité et la sécurité du natalizumab administré par voie SC :
- l'objectif principal de l'étude était de comparer, dans une population de patients atteints de SEP et naïfs de natalizumab, la pharmacocinétique et la pharmacodynamie de doses uniques de 300 mg de natalizumab, administrées par voie SC ou intramusculaire (IM), avec celles des doses de 300 mg de natalizumab administrées en perfusion IV ;
- aucun des patients traités par natalizumab n'a présenté de lésions Gd+ après l'inclusion, quel que soit le stade de la maladie (SEP-RR ou SEP secondaire progressive), la voie d'administration choisie ou la présence de lésions Gd+ à l'inclusion. Parmi les populations de patients atteints de SEP-RR (n = 12) et de SEP secondairement progressive (n = 14), 2 patients du groupe natalizumab 300 mg sous-cutané ont présenté des poussées comparativement à 3 patients du groupe natalizumab 300 mg en perfusion intraveineuse.
En termes de tolérance, le profil de sécurité observé pour le natalizumab administré par voie sous-cutanée a été conforme au profil de sécurité connu du natalizumab administré par voie intraveineuse, à l'exception de la douleur au site d'injection. La fréquence globale de la douleur au site d'injection a été de 4 % (3/71) pour les patients recevant 300 mg de natalizumab toutes les 4 semaines par administration sous-cutanée.
Surveillance des patients : un guide pour rappeler les éléments de vigilance
Le traitement par TYSABRI 150 mg SC doit être instauré et surveillé en continu par des médecins spécialistes, ayant l'expérience du diagnostic et du traitement des affections neurologiques, avec un accès à l'IRM dans un délai approprié.
Comme pour TYSABRI 300 mg, des mesures additionnelles de réduction du risque, validées par l'ANSM et diffusées par le laboratoire exploitant Biogen, accompagnent les médecins et les patients :
- pour les médecins : un guide de prescription (cf. Encadré 2) pour la prise en charge des patients est disponible. Il précise notamment les principaux risques associés à TYSABRI (notamment le risque de leucoencéphalopathie multifocale progressive, LEMP - cf. notre article du 17 février 2016) et la démarche à suivre en cas de suspicion d'effets indésirables ; ont été ajoutés en date du 25 octobre 2021 :
- pour les patients : une carte patient qui contient d'importantes informations sur la sécurité d'utilisation de TYSABRI, notamment sur certains signes et symptômes évocateurs d'effets indésirables graves (cf. Encadré 3), ainsi qu'une brochure patient décrivant l'essentiel des informations à connaître sur le traitement par TYSABRI.
Encadré 2 - Guide de prescription de TYSABRI pour la prise en charge des patients (extrait du RCP)
|
Encadré 3 - Carte patient accompagnant la prescription de TYSABRI
|
TYSABRI 150 mg SC en pratique
La dose recommandée pour une administration SC est de 300 mg toutes les 4 semaines, soit 2 injections de TYSABRI 150 mg en seringue préremplie. La seconde injection doit être administrée :
- immédiatement ou au plus tard 30 minutes après la première,
- et à plus de 3 cm du premier site d'injection.
L'injection SC doit être réalisée par un professionnel de santé. Les sites recommandés sont la cuisse, l'abdomen ou la face postérieure de la partie supérieure du bras.
Tout changement de voie d'administration du médicament doit être effectué 4 semaines après la dose précédente.
La poursuite du traitement devra être reconsidérée soigneusement chez les patients ne présentant aucun signe de bénéfice thérapeutique au-delà de 6 mois.
Consignes d'utilisation de TYSABRI 150 mg SC en seringue préremplie
La seringue préremplie de TYSABRI 150 mg est prête à l'emploi (cf. Figure 1) :
- seringue à usage unique, contenant 1 mL de solution (soit 150 mg de natalizumab),
- aiguille de 27 Gauge préfixée.
Figure 1 - Représentation schématique de la seringue préremplie de TYSABRI 150 mg
Les seringues sont à conserver au réfrigérateur entre 2 et 8 °C dans l'emballage extérieur à l'abri de la lumière. Une conservation à température ambiante (jusqu'à 25 °C) est tolérée pendant 24 heures. Dans ce cas, les seringues préremplies ne doivent pas être remises au réfrigérateur.
Avant l'injection, il est recommandé de faire revenir la solution injectable à température ambiante pendant 30 minutes.
Surveillance du patient après l'injection
Pour les 6 premières doses, les patients doivent rester en observation pendant les injections SC et pendant 1 heure après, afin de détecter les signes et symptômes de réactions à l'injection, y compris l'hypersensibilité.
Au-delà des 6 premières doses, le temps d'observation d'une heure après l'injection peut être réduit ou supprimé selon l'appréciation clinique si les patients n'ont présenté aucune réaction à l'injection.
Identité administrative
- Liste I
- Prescription réservée aux spécialistes en neurologie
- Médicament réservé à l'usage hospitalier
- Boîte de 2 seringues préremplies de 1 mL de solution, CIP 3400955080381
- Agrément aux collectivités (Journal officiel du 8 octobre 2021 - texte 34)
- Inscrit sur la liste en sus des GHS - UCD 3400890012997 (Journal officiel du 8 octobre 2021 - texte 38) [cf. Encadré 3]
- Laboratoire Biogen France
Encadré 3 - TYSABRI 150 mg : périmètre de prise en charge en sus des GHS
|
Pour aller plus loin
Mesures additionnelles de réduction du risque validées par l'ANSM et diffusées par le laboratoire exploitant le médicament TYSABRI :
- Guide de prescription (19/08/2021)
- Brochure patients (19/08/2021)
- Carte patients (19/08/2021)
- Formulaire d'instauration de traitement (25/10/2021)
- Formulaire de poursuite du traitement après 2 ans (25/10/2021)
- Formulaire d'arrêt de traitement (25/10/2021)

 9 minutes
9 minutes Ajouter un commentaire
Ajouter un commentaire



