Le traitement pharmacologique de la BPCO se fait par paliers, en fonction de la sévérité, des symptômes prédominants (dyspnée, exacerbations) et de la réponse au traitement (illustration).
Résumé :
L'arsenal thérapeutique de la bronchopneumopathie obstructive chronique (BPCO) modérée à sévère compte une nouvelle spécialité, TRIXEO AEROSPHERE 5 µg/7,2 µg/160 µg suspension pour inhalation en flacon pressurisé.
Il s'agit d'une triple association (formotérol, glycopyrronium et budésonide), à envisager lorsqu'une bithérapie (corticostéroïde inhalé + bêta-agoniste de longue durée d'action ou bêta-agoniste de longue durée d'action + antagoniste muscarinique de longue durée d'action) ne permet pas de traiter de façon satisfaisante un patient.
La posologie maximale recommandée est de 2 inhalations 2 fois par jour.
Les consignes appropriées doivent être rappelées aux patients pour coordonner l'inspiration et le déclenchement de la dose, et garantir le bon usage de TRIXEO.
TRIXEO AEROSPHERE est agréé aux collectivités et remboursable à 30 %, dans une indication restreinte (uniquement la BPCO sévère) par rapport à celle de l'autorisation de mise sur le marché. Son prix public (hors honoraires de dispensation) s'élève à 53,79 euros (1 aérosol doseur de 120 doses). La prise en charge est subordonnée à la prescription initiale par un pneumologue.
La spécialité TRIXEO AEROSPHERE 5 µg/7,2 µg/160 µg suspension pour inhalation en flacon pressurisé est une nouvelle alternative dans le traitement de la bronchopneumopathie chronique obstructive (BPCO - cf. VIDAL Reco "BPCO").L'arsenal thérapeutique de la bronchopneumopathie obstructive chronique (BPCO) modérée à sévère compte une nouvelle spécialité, TRIXEO AEROSPHERE 5 µg/7,2 µg/160 µg suspension pour inhalation en flacon pressurisé.
Il s'agit d'une triple association (formotérol, glycopyrronium et budésonide), à envisager lorsqu'une bithérapie (corticostéroïde inhalé + bêta-agoniste de longue durée d'action ou bêta-agoniste de longue durée d'action + antagoniste muscarinique de longue durée d'action) ne permet pas de traiter de façon satisfaisante un patient.
La posologie maximale recommandée est de 2 inhalations 2 fois par jour.
Les consignes appropriées doivent être rappelées aux patients pour coordonner l'inspiration et le déclenchement de la dose, et garantir le bon usage de TRIXEO.
TRIXEO AEROSPHERE est agréé aux collectivités et remboursable à 30 %, dans une indication restreinte (uniquement la BPCO sévère) par rapport à celle de l'autorisation de mise sur le marché. Son prix public (hors honoraires de dispensation) s'élève à 53,79 euros (1 aérosol doseur de 120 doses). La prise en charge est subordonnée à la prescription initiale par un pneumologue.
Plus précisément, TRIXEO AEROSPHERE est indiqué dans le traitement continu de la BPCO modérée à sévère chez les adultes non traités de façon satisfaisante par l'association d'un corticostéroïde inhalé (CSI) et d'un bronchodilatateur bêta-2-agoniste de longue durée d'action (LABA), ou l'association d'un LABA et d'un bronchodilatateur antagoniste muscarinique de longue durée d'action (LAMA).
TRIXEO, pour TRIthérapie
Comme suggéré par son nom, TRIXEO associe 3 principes actifs :
- un LABA : le formotérol (fumarate),
- un LAMA : le glycopyrronium (bromure),
- un CSI : le budésonide.
Chaque dose délivrée (mesurée à la sortie de l'embout buccal) contient :
- 5 µg de formotérol ;
- 9 µg de bromure de glycopyrronium équivalant à 7,2 µg de glycopyrronium ;
- 160 µg de budésonide.
Association LABA + LAMA + CSI : ce que disent les recommandations
La prise en charge thérapeutique de la BPCO a fait l'objet de recommandations internationales GOLD en 2021 (Global initiative for chronic Obstructive Lung Disease).
En France, un "Guide du parcours de soins – Bronchopneumopathie chronique obstructive" a été rédigé conjointement par la Haute Autorité de Santé (HAS) et l'Assurance maladie pour accompagner les professionnels de santé.
Selon ces recommandations, le traitement pharmacologique de la BPCO se fait par paliers et tient compte des éléments suivants :
- sévérité des symptômes,
- prédominance de symptôme (dyspnée, exacerbations),
- réponse au traitement.
De la mono à la trithérapie : stratégie thérapeutique
Les LABA et LAMA représentent le principal traitement symptomatique de la BPCO chez les patients ayant une dyspnée quotidienne et/ou des exacerbations.
En cas d'échec d'une monothérapie, une bithérapie associant ces deux types de bronchodilatateurs (LABA + LAMA) est envisagée.
La trithérapie LABA + LAMA + CSI est indiquée en cas de persistance d'exacerbations malgré une bithérapie (LABA + LAMA) bien conduite.
Selon les récentes recommandations internationales, le choix d'ajouter un CSI à une monothérapie (LABA ou LAMA) ou à une bithérapie LABA + LAMA doit tenir compte du seuil d'éosinophiles (> 150 cellules/µL).
Deux études pivots de phase III menées avec la trithérapie TRIXEO
Dans son avis du 10 mars 2021, la Commission de la Transparence (CT) a évalué l'efficacité et la tolérance de TRIXEO AEROSPHERE principalement sur la base de 2 études de phase III :
- ETHOS (1), randomisée, en double aveugle, en groupes parallèles dont l'objectif principal était d'évaluer l'efficacité et la tolérance pendant 52 semaines de TRIXEO AEROSPHERE (BGF 320 MDI) par rapport à chacune des deux associations fixes doubles glycopyrronium 7,2 µg /formotérol 4,8 µg (GF MDI) et budésonide 160 µg /formotérol 4,8 µg (BF MDI) chez 8 573 patients ayant une BPCO modérée à très sévère avec des antécédents d'exacerbation ;
- et KRONOS (2), randomisée, en double aveugle partiel (le CSI était administré en ouvert), en groupes parallèles, ayant pour objectif d'évaluer pendant 24 semaines l'efficacité et la tolérance de TRIXEO AEROSPHERE (BGF 320 MDI, LABA/LAMA/CSI) par rapport aux associations doubles glycopyrronium 7,2 µg /formotérol 4,8 µg (LAMA/LABA, GF MDI) et budésonide 160 µg /formotérol 4,8 µg (CSI/LABA, BF MDI), et de l'association double BF MDI par rapport à l'association double BF poudre pour inhalation (SYMBICORT Turbuhaler, budésonide/formotérol, CSI/LABA) chez 1 902 patients ayant une BPCO modérée à très sévère, symptomatiques.
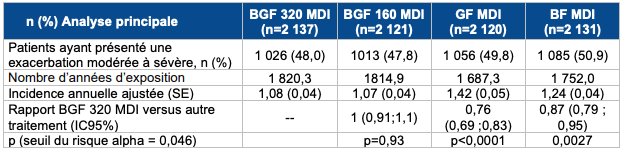
Selon les résultats de l'étude ETHOS, une réduction statistiquement significative du taux d'exacerbations modérées à sévères à 52 semaines (critère de jugement principal) en faveur de BGF 320 MDI a été démontrée par rapport au groupe GF MDI (ratio = 0,76 ; IC95 % [0,69 ; 0,83]) et par rapport au groupe BF MDI (ratio = 0,87 ; IC95 % [0,79 ; 0,95]), avec toutefois des différences absolues de faible ampleur (cf. Tableau I).
Tableau I - Critère de jugement principal - analyse principale - étude ETHOS (population mITT2)
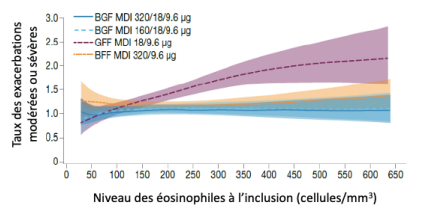
La CT précise qu'"une analyse exploratoire (analyse en sous-groupe sur le critère de jugement principal) suggère que la réduction d'exacerbations modérées à sévères de la triple thérapie comportant un CSI, comparé au LAMA/LABA apparaît dans le sous-groupe de patients présentant un taux d'éosinophiles sanguin > 150 cellules/µL et pas dans le sous-groupe de patients avec un taux d'éosinophiles sanguin < 150 cellules/µL" (cf. Figure 1 extraite de la publication de l'étude).
Figure 1 - Taux des exacerbations en fonction du taux d'éosinophiles dans chaque groupe
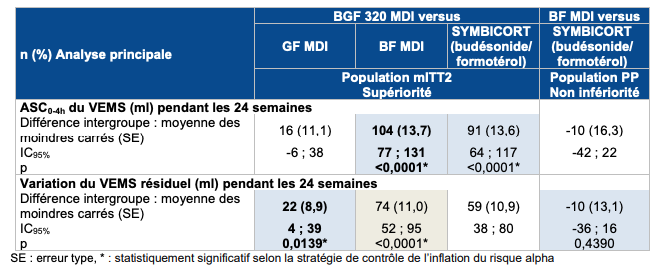
S'agissant des résultats de l'étude KRONOS, une différence statistiquement significative en faveur de BGF 320 MDI a été démontrée (cf. Tableau II) en termes de :
- variation de l'ASC0-4h du VEMS en faveur du groupe BGF 320MDI par rapport au groupe BF MDI (différence de 104 mL, [77 ; 131], p < 0,0001) et par rapport au group SYMBICORT (budésonide/formotérol) (différence de 91 mL, [64 ; 117], p < 0,0001) ;
- variation du VEMS résiduel pré-dose matinal du groupe BGF 320 MDI par rapport au GF MDI (différence de 22 mL, [4 ; 39], p = 0,0139) ; la CT précise que "ces valeurs sont à mettre en perspective avec la différence minimale cliniquement pertinente qui est de 100 ml".
Tableau II - Critères de jugement principaux de l'étude KRONOS selon une approche avec prise en compte uniquement des données disponibles avant l'arrêt du traitement de l'étude (en bleu : analyses avec contrôle de l'inflation du risque alpha, en blanc : analyses sans contrôle de l'inflation du risque alpha, en gris : critère secondaire)
SMR : de modéré à insuffisant selon l'indication
Sur la base des données disponibles, la CT a attribué à TRIXEO AEROSPHERE :
- un service médical rendu (SMR) modéré dans le traitement continu de la BPCO sévère non traités de façon satisfaisante par l'association d'un CSI et d'un LABA ou par l'association d'un LABA et d'un LAMA ;
- un SMR insuffisant dans le traitement de la BPCO modérée, au regard des alternatives disponibles.
TRIXEO AEROSPHERE en pratique
La dose maximale recommandée de TRIXEO AEROSPHERE est de 2 inhalations 2 fois par jour (2 inhalations le matin et 2 inhalations le soir).
À propos de l'inhalateur
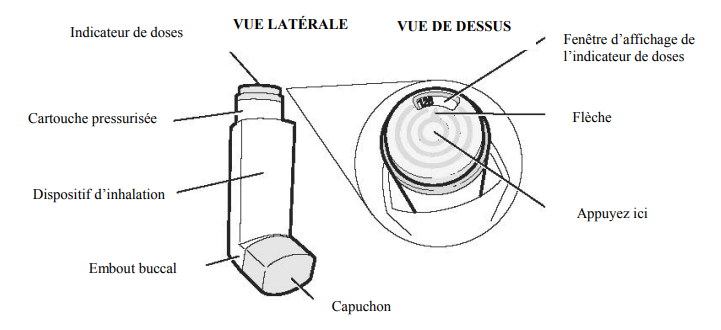
TRIXEO AEROSPHERE se compose d'une cartouche pressurisée insérée dans un inhalateur avec embout (cf. Figure 2).
La cartouche est munie d'un indicateur de dose (le nombre de doses restantes est indiqué par une flèche).
Une cartouche contient 120 doses, soit la quantité suffisante de doses (4 par jour) pour 30 jours de traitement.
Figure 2 - Différentes parties de l'inhalateur TRIXEO AEROSPHERE
Avant d'utiliser l'inhalateur, il est nécessaire de l'amorcer en l'agitant et l'actionnant 4 fois dans l'air ambiant avant la première utilisation ou 2 fois lorsque l'inhalateur n'a pas été utilisé pendant plus de 7 jours, après un lavage hebdomadaire ou lorsqu'il est tombé.
Expirer, déclencher, inspirer
L'inhalation de TRIXEO AEROSPHERE se déroule en 3 étapes principales :
- le patient doit expirer le plus possible,
- le patient place l'embout dans sa bouche,
- le patient appuie sur la cartouche tout en inspirant lentement et profondément, puis retient sa respiration le plus longtemps possible, jusqu'à 10 secondes.
Il est également recommandé de nettoyer l'inhalateur 1 fois par semaine.
Les patients qui présentent des difficultés à coordonner le déclenchement du dispositif d'inhalation avec l'inspiration peuvent utiliser TRIXEO AEROSPHERE avec une chambre d'inhalation. La compatibilité avec la chambre d'inhalation Aerochamber Plus Flow-Vu a été démontrée.
Identité administrative
Liste I
Flacon de 120 doses, CIP 3400930219300
Remboursable à 30 % (Journal officiel du 6 août 2021, texte 23, rectifié par le Journal officiel du 2 septembre, texte 30 - cf. Encadré 2)
Prix public TTC = 53,79 euros
Agrément aux collectivités (Journal officiel du 6 août 2021, texte 24, rectifié par le Journal officiel du 2 septembre 2021, texte 31 - cf. Encadré 2)
Laboratoire AstraZeneca
Encadré 2 - Condition et périmètre de prise en charge de TRIXEO AEROSPHERE
La prise en charge de la TRIXEO AEROSPHERE dans l'indication ci-après est subordonnée à la prescription initiale par un médecin pneumologue :
|
Pour aller plus loin
Avis de la Commission de la Transparence - TRIXEO AEROSPHERE (HAS, 10 mars 2021)
Les études pivots relatives à TRIXEO AEROSPHERE
- Étude ETHOS : Rabe KF, Martinez FJ, Ferguson GT et al ; ETHOS investigators. Inhaled Triple Therapy at Two Glucocorticoid Doses in Moderate-to-Very Severe COPD. NEJM 2020; published on June 24, 2020
- Étude KRONOS : Ferguson GT, Rabe KF, Martinez F et col. Triple therapy with budesonide/glycopyrrolate/formoterol fumarate with co- suspension delivery technology versus dual therapies in chronic obstructive pulmonary disease (KRONOS): a double- blind, parallel-group, multicentre, phase 3 randomised controlled trial. Lancet Respir Med 2018; 6(10) : 747-758
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.