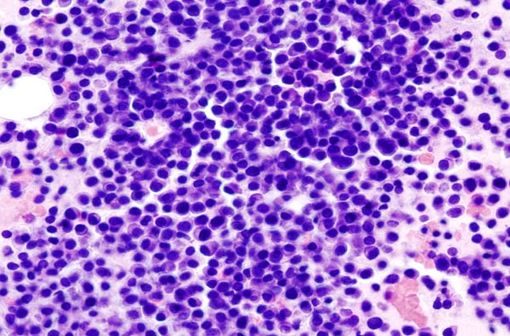
Image histopathologique d'un myélome multiple (extrait de la moelle osseuse). Coloration à l'hématoxyline et à l'éosine (illustration @KGH sur Wikimedia)..
Résumé :
BLENREP 100 mg poudre pour solution à diluer pour perfusion est un nouveau médicament, à base de bélantamab mafodotine, indiqué en monothérapie chez les patients adultes atteints d'un myélome multiple (MM) en rechute ou réfractaire, ayant reçu au moins 4 traitements antérieurs et dont la maladie est réfractaire à au moins un inhibiteur du protéasome (IP), un agent immunomodulateur (IMID) et un anticorps monoclonal anti-CD38, et dont la maladie a progressé lors du dernier traitement.
Pour la Commission de la Transparence (CT), BLENREP est un traitement de recours du myélome multiple lorsque toutes les options thérapeutiques ont été épuisées, sur avis d'une réunion de concertation pluridisciplinaire.
En pratique, BLENREP est administré en perfusion intraveineuse 1 fois toutes les 3 semaines, à la dose de 2,5 mg/kg.
La solution à injecter doit être reconstituée et diluée avant administration.
Le profil de tolérance de BLENREP est marqué par une toxicité cornéenne, à l'origine de kératopathies. Avant l'instauration et pendant le traitement, les patients doivent être soumis à un examen ophtalmologique. Pour limiter les symptômes cornéens, l'utilisation de larmes artificielles sans conservateur est recommandée en soins de support.
BLENREP est un médicament réservé à l'usage hospitalier et soumis à prescription restreinte. Le conditionnement en flacon unitaire de poudre est agréé aux collectivités.
L'arsenal thérapeutique du myélome multiple compte une nouvelle spécialité hospitalière, BLENREP 100 mg poudre pour solution à diluer pour perfusion (bélantamab mafodotine), indiquée en monothérapie dans le traitement des patients adultes atteints de myélome multiple (cf. VIDAL Reco "Myélome multiple") :
BLENREP 100 mg poudre pour solution à diluer pour perfusion est un nouveau médicament, à base de bélantamab mafodotine, indiqué en monothérapie chez les patients adultes atteints d'un myélome multiple (MM) en rechute ou réfractaire, ayant reçu au moins 4 traitements antérieurs et dont la maladie est réfractaire à au moins un inhibiteur du protéasome (IP), un agent immunomodulateur (IMID) et un anticorps monoclonal anti-CD38, et dont la maladie a progressé lors du dernier traitement.
Pour la Commission de la Transparence (CT), BLENREP est un traitement de recours du myélome multiple lorsque toutes les options thérapeutiques ont été épuisées, sur avis d'une réunion de concertation pluridisciplinaire.
En pratique, BLENREP est administré en perfusion intraveineuse 1 fois toutes les 3 semaines, à la dose de 2,5 mg/kg.
La solution à injecter doit être reconstituée et diluée avant administration.
Le profil de tolérance de BLENREP est marqué par une toxicité cornéenne, à l'origine de kératopathies. Avant l'instauration et pendant le traitement, les patients doivent être soumis à un examen ophtalmologique. Pour limiter les symptômes cornéens, l'utilisation de larmes artificielles sans conservateur est recommandée en soins de support.
BLENREP est un médicament réservé à l'usage hospitalier et soumis à prescription restreinte. Le conditionnement en flacon unitaire de poudre est agréé aux collectivités.
- ayant reçu au moins 4 traitements antérieurs,
- et dont la maladie est réfractaire à au moins un inhibiteur du protéasome, un agent immunomodulateur et un anticorps monoclonal anti-CD38,
- et dont la maladie a progressé lors du dernier traitement.
BLENREP fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
Une AMM conditionnelle après une mise à disposition en ATU
Le principe actif de BLENREP, belantamab mafodotin, est un anticorps monoclonal humain IgG1k, conjugué à un agent cytotoxique inhibiteur des microtubules, le maléimidocaproyl monométhyl auristatine F (mcMMAF). Cette combinaison présente une activité antitumorale par ciblage du récepteur B-cell maturation antigen (BCMA) exprimé à la surface des cellules B au stade avancé de maturation et à la surface des plasmocytes tumoraux.
En France, le bélantamab mafodotine a été mis à disposition des patients dès 2019 grâce au dispositif d'autorisation temporaire d'utilisation (ATU nominative puis de cohorte).
En août 2020, BLENREP a reçu une autorisation de mise sur le marché (AMM) européenne conditionnelle. Le comité européen des médicaments à usage humain (CHMP) a conditionné le maintien de cette AMM à des résultats complémentaires d'efficacité (résultats finaux de l'étude pivot DREAMM-2 - cf. Infra - et résultats de l'étude de supériorité de phase 3 DREAMM-3 comparant BLENREP en monothérapie à l'association pomalidomide/dexaméthasone).
Évaluation médico-économique du belantamab mafodotin
Les résultats de l'étude DREAMM-2
L'efficacité et la tolérance du bélantamab mafodotine ont été étudiées dans l'essai clinique de phase II DREAMM-2 (1), randomisé, ouvert, non contrôlé, en groupes parallèles, sous deux posologies : 2,5 mg/kg (posologie recommandée dans l'AMM) et 3,4 mg/kg. La population de l'étude (n = 196) correspondait à des patients ayant un myélome multiple en rechute après au moins 3 lignes de traitement antérieures, dont un anticorps monoclonal anti-CD38 et réfractaires à au moins un agent immunomodulateur (IMiD) et un inhibiteur du protéasome (IP).
Le critère de jugement principal était le taux de réponse globale (TRG), évalué par un comité de revue indépendant (CRI) et défini par la proportion de patients ayant une réponse partielle confirmée (RP) ou meilleure, c'est-à-dire une très bonne réponse partielle (TBRP), une réponse complète (RC) ou une réponse complète stringente (RCs), selon les critères de réponse de 2016 du groupe de travail international sur le myélome multiple (IMWG). L'évaluation a également porté sur 8 critères de jugement secondaires dont la survie sans progression (SSP) et la durée de la réponse globale.
Au terme d'un suivi médian de 13 mois, le TRG évalué par le CRI (population ITT) a été de :
- 32 % (IC97,5 % [21,7 ; 43,6]) dans le groupe bélantamab mafodotine à la posologie de 2,5 mg/kg (n = 97), avec une durée médiane de la réponse de 11 mois ;
- 35 % (IC97,5 % [24,8 ; 47,0]) dans le groupe bélantamab mafodotine à la posologie de 3,4 mg/kg (n = 99).
Dans le même temps, la médiane de survie sans progression évaluée par le CRI (population ITT) a été de 2, 8 mois dans le groupe 2,5 mg/kg (IC95 % [1,6 ; 3,6]) et de 3,9 mois dans le groupe 3,4 mg/kg (IC95 % [2,0 ; 5,8]).
En termes de tolérance, le profil de BLENREP a été marqué par des effets indésirables oculaires fréquents, notamment des kératopathies de grade 3 ou 4 rapportées chez 30 % des patients dans le groupe 2,5 mg/kg.
SMR important, ASMR V
Sur la base des données disponibles au moment de son évaluation, la Commission de la Transparence (CT) a attribué à BLENREP (avis du 16 décembre 2021) :
- un service médical rendu (SMR) important ;
- sans amélioration du SMR (ASMR V).
La CT note l'intérêt de disposer "d'un médicament ayant été évalué après échec d'un anticorps anti-CD38 dans un contexte de besoin médical non couvert" et "d'un nouveau mécanisme d'action ciblant le récepteur BCMA dans les situations de recours", mais pointent le recul extrêmement limité (13 mois environ) et les incertitudes qui en découlent sur l'efficacité et son maintien.
La CT estime que la place de BLENREP dans la stratégie thérapeutique, est celle d'un traitement de dernier recours chez les patients en situation d'impasse thérapeutique après au moins 4 traitements antérieurs, et dont la maladie est réfractaire à au moins un inhibiteur du protéasome, un immunomodulateur et un anticorps monoclonal anti-CD38 comme daratumumab (DARZALEX).
La CT recommande que le choix du bélantamab mafodotine repose sur une concertation pluridisciplinaire.
BLENREP en pratique
Le traitement par BLENREP doit être instauré et supervisé par des médecins expérimentés dans le traitement du myélome multiple.
BLENREP se présente en flacon de poudre, contenant 100 mg de bélantamab mafodotin. Après reconstitution avec de l'eau pour préparation injectable (non fournie avec le flacon de poudre), on obtient une solution concentrée à 50 mg/mL.
La solution reconstituée doit être diluée pour l'administration intraveineuse. Plus précisément, le volume de solution reconstituée correspondant à la dose à administrer doit être dilué dans 250 mL de chlorure de sodium injectable à 0,9 %.
Les instructions pour la reconstitution et la dilution sont décrites dans la monographie VIDAL de BLENREP - Rubrique Modalités Manipulation/ Élimination.
Perfusion intraveineuse toutes les 3 semaines
La dose recommandée de BLENREP est de 2,5 mg/kg administrés par perfusion intraveineuse (IV) 1 fois toutes les 3 semaines.
La durée de perfusion doit être de 30 minutes minimum. Les instructions pour l'administration sont décrites dans la monographie VIDAL de BLENREP - Rubrique Modalités Manipulation/ Élimination.
Le traitement doit être poursuivi jusqu'à progression de la maladie ou l'apparition d'une toxicité inacceptable.
La posologie doit être adaptée en fonction de la tolérance du traitement, en cas de survenue d'effets indésirables cornéens ou d'autres effets indésirables (cf. Tableaux 1 et 2 - monographie VIDAL).
Toxicité cornéenne associée à BLENREP : mesures à appliquer
Le profil de tolérance de BLENREP est marqué par des effets indésirables cornéens (kératopathies, modification de l'acuité visuelle, ulcère cornéen).
Les patients doivent bénéficier d'un examen ophtalmologique (incluant une évaluation de l'acuité visuelle et un examen à la lampe à fente) par un ophtalmologue :
- avant l'instauration du traitement,
- avant la réalisation des 3 cycles suivants,
- puis tout au long du traitement comme cliniquement indiqué.
Pendant le traitement, l'examen ophtalmologique permet d'évaluer la sévérité des effets indésirables cornéens (léger, modéré, sévère) et la démarche posologique à adopter.
Des soins de support sont également recommandés pour réduire les symptômes cornéens :
- administration de larmes artificielles sans conservateur, au moins 4 fois par jour, à partir du premier jour de perfusion et jusqu'à la fin du traitement.
Autres éléments de surveillance et points de vigilance
Le traitement par BLENREP expose également à un risque de thrombopénie. La surveillance doit en prendre compte et une numération formule sanguine complète doit être :
- réalisée au moment de l'instauration du traitement,
- puis contrôlée tout au long du traitement comme cliniquement indiqué.
- pour les femmes en âge de procréer, utiliser une contraception efficace pendant le traitement et pendant 4 mois après l'administration de la dernière dose ;
- pour les hommes dont les partenaires féminines sont en âge de procréer, utiliser une contraception efficace pendant le traitement et pendant 6 mois après l'administration de la dernière dose.
Identité administrative
- Liste I
- Réservé à l'usage hospitalier
- Prescription réservée aux spécialistes en oncologie ou en hématologie, ou aux médecins compétents en cancérologie ou en maladies du sang
- Surveillance particulière au cours du traitement
- Flacon unitaire, CIP 3400955075622
- Agrément aux collectivités (Journal officiel du 17 septembre 2021 - texte 20)
- Laboratoire GSK (GlaxoSmithKline)
Pour aller plus loin
Avis de la Commission de la Transparence - BLENREP (HAS, 16 décembre 2020)
L'étude pivot
(1) Lonial S et al. Belantamab Mafodotin for Relapsed or Refractory Multiple Myeloma (DREAMM-2): A Two-Arm, Randomised, Open-Label, Phase 2 Study. Lancet Oncol 2020 ; 21(2) : 207-221.
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.