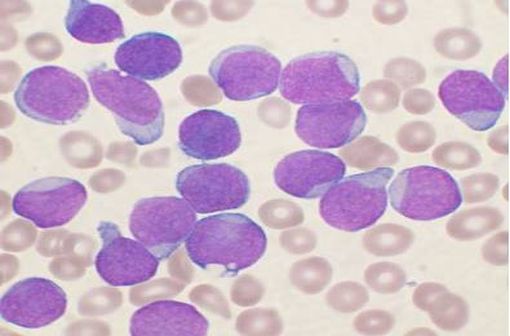
Frottis de moelle osseuse d'un patient atteint d'une leucémie lymphoblastique aiguë à cellules B (illustration @VashiDonsk sur Wikipédia anglais).
Depuis plusieurs années, la spécialité à base de crisantaspase ERWINASE est sous tension d'approvisionnement. Ces difficultés sont compensées partiellement par la mise à disposition régulières d'unités d'ERWINASE initialement destinées au marché britannique (cf. notre dernier article sur ERWINASE du 1er octobre 2020).
Selon les dernières informations communiquées par l'ANSM (Agence nationale de sécurité du médicament et des produits de santé), une indisponibilité totale d'ERWINASE est prévue à partir de la fin de l'année 2020.
En outre, un arrêt de commercialisation de la spécialité KIDROLASE est attendu au cours du deuxième trimestre 2021.
Modification du niveau 3 de priorisation
Dans ce contexte, les préconisations de traitement de la leucémie aiguë lymphoblastique (LAL) chez l'enfant et l'adulte élaborées par l'INCa (Institut national du cancer) en 2017 ont été actualisées (cf. VIDAL Reco "Leucémies aiguës de l'adulte").
Les points de mise à jour concernent le niveau de priorité 3, celui correspondant à une indisponibilité totale d'ERWINASE ; les niveaux de priorité 1 et 2 tels que précisés dans la version 2017 restent valables (cf. Encadré 1).
Concernant le niveau 3, dans la version initiale de 2017, il était recommandé de prioriser uniquement les traitements par ERWINASE déjà débutés chez les enfants.
Dans la version actualisée en octobre 2020, les experts :
- ajoutent à cette population prioritaire pédiatrique celle des adultes atteints de LAL de type T (LAL-T) ;
- suppriment la notion de traitement par ERWINASE ayant déjà débuté.
Encadré 1 - Utilisation d'ERWINASE en période de tension d'approvisionnement : niveaux de priorisation 1, 2 et 3 (version actualisée - octobre 2020)
|
Stratégies de prophylaxie primaire ou secondaire : recommandations d'utilisation des autres asparaginases
L'avis d'experts actualisé identifie également, dans le cadre du traitement de la leucémie aiguë lymphoblastique de l'enfant et de l'adulte, les stratégies de prophylaxies primaire et secondaire des réactions d'hypersensibilité/allergies aux asparaginases (cf. Encadré 2), susceptibles d'être utilisées pour minimiser le recours à ERWINASE.
Ces préconisations visant à sécuriser l'utilisation des asparaginases précisent :
- les modalités d'administration,
- la nécessité ou non d'une prémédication,
- les modalités de surveillance du patient.
Encadré 2 - Spécialités à base d'asparaginase commercialisées en France - octobre 2020
|
Pour aller plus loin
Leucémie aiguë lymphoblastique : actualisation partielle des préconisations de traitement de l'enfant et de l'adulte dans un contexte de tensions d'approvisionnement en Erwinase - Point d'information (ANSM, 30 octobre 2020)
Nouvelles préconisations pour le traitement de la leucémie aiguë lymphoblastique - Actualisation selon l'avis d'experts du 28 octobre 2020
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.