Une éradication aujourd'hui envisageable grâce au dépistage et au traitement (illustration).
Tout commence au début des années 1970, grâce à la mise en place du dépistage sérologique des deux virus A (1) et B (2) déjà connus. Les travaux d'Harvey Alter (3) et d'autres montrent qu'environ 75 % des hépatites post-transfusionnelles ne sont pas liées à la présence du virus B, en cause dans 25 % des cas, et jamais au virus A. Des analyses sérologiques rétrospectives ultérieures vont confirmer cette prévalence de 70 % à 90 % d'hépatites non-A non-B.
Le caractère majoritairement chronique et la possible évolution cirrhogène de ces hépatites silencieuses sont aussi mis en évidence et font suspecter l'existence d'un autre virus transmissible, dont la réalité est démontrée, en 1979, par des études sur le chimpanzé (4).
Une bataille de plus de 10 ans
Il va falloir plus de dix années de travaux jusqu'aux publications, en 1989, par l'équipe de Michael Houghton (5 et 6) qui a identifié le génome du virus et effectué son séquençage, permettant son classement parmi les flavivirus et un dépistage sérologique, initialement par tests Elisa, réduisant spectaculairement le risque transfusionnel dès 1989 (7).
Six génotypes vont être identifiés, numérotés de 1 à 6, avec plusieurs dizaines de sous-types. En France, dès le début des années 2000, le principe de précaution va faire remplacer le dépistage Elisa par la PCR, pour faire diminuer le faible risque transfusionnel résiduel (8).
Des progrès thérapeutiques pas à pas
Les tentatives thérapeutiques débutées à ce moment commencent par l'utilisation de l'interféron alpha-2a, mais avec des résultats très insuffisants après une durée de traitement de 6 ou 12 mois, ce qui va justifier, au milieu des années 1990, son association à la ribavirine, puis son remplacement par l'interféron pégylé au début des années 2000, amenant à un taux de guérison de 55 % en 2010 (cf. Figure 1).
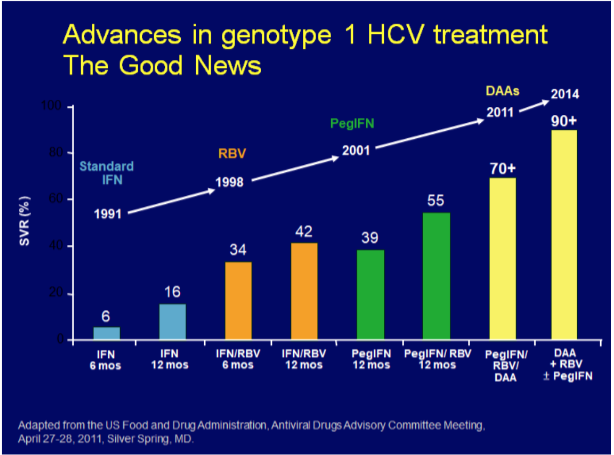
IFN : interféron ; RBV : ribavirine ; PEgIFN : interféron pégylé ; DAA : antiviraux d'action directe ; SVR : réponse virologique soutenue (le virus n'est pas détecté dans le sang 12 semaines ou plus après la fin du traitement).
Grâce aux patients travaux de l'équipe de Charles Rice (9) sur l'analyse des séquences, des fonctionnalités du génome et du cycle de réplication grâce à l'apport des cultures cellulaires et du système des réplicons, c'est-à-dire le transfert de l'ARN viral dans une lignée cellulaire cancéreuse permettant la réplication in vitro du génome viral (10), de nouvelles cibles et stratégies thérapeutiques vont permettre le développement rapide de molécules agissant directement sur la réplication virale (cf. Figures 1 et 2).
Figure 2 - Cycle de vie du virus de l'hépatite C et cibles des antiviraux directs
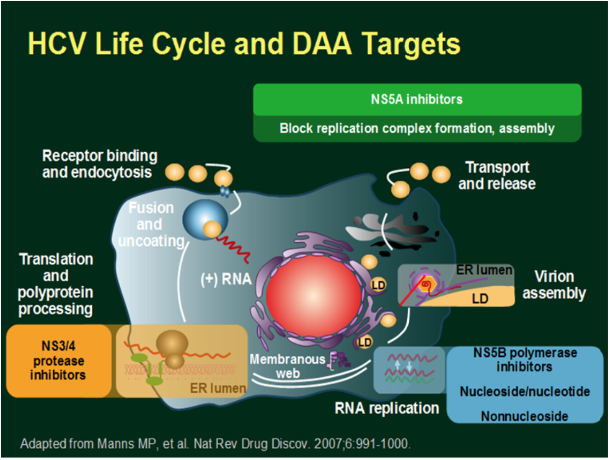
NS5A inhibitors : inhibiteurs de la protéase NS5A ; NS3/4 inhibitors : inhibiteurs de la protéase NS3/4 ; NS5B polymerase inhibitors : inhibiteurs de la polymérase NS5B.
Aujourd'hui, des taux de guérison de plus de 95 %
Les deux premiers antiviraux d'action directe, le bocéprévir et le télaprévir, anti-protéases de première génération, associées à la ribavirine et à l'interféron pégylé, font progresser, dès 2011, le taux de guérison qui atteint plus de 90 % en 2014, mais au prix d'un traitement long et générateur de nombreux effets secondaires.
Le développement d'autres agents antiviraux directs, agissant sur d'autres cibles que la protéase virale et utilisables par voie orale avec des durées de traitement beaucoup plus courtes et une tolérance remarquable, aboutit, à partir de 2014, à des taux de guérison de plus de 95 %, après 12, voire 6 semaines de traitement.
Cette remarquable amélioration des possibilités thérapeutiques, notamment pour certaines populations de patients et pour certaines structures de soins, ainsi que l'important allègement du suivi clinicobiologique ont radicalement transformé l‘offre de soins et la prise en charge de ce problème de santé publique mondial, entretenu essentiellement par les toxicomanies à risque, permettant d'envisager à long terme l'éradication de cette pathologie.
À ce jour, 5 associations d'antiviraux d'action directe sont disponibles en France (cf. Encadrés 1 et 2).
Encadré 2 - L'hépatite C en pratique
|
©vidal.fr
Pour en savoir plus
1 - Feinstone S.M, Kapikian A.Z, Purceli R.H. Hepatitis A: detection by immune electron microscopy of a viruslike antigen associated with acute illness. Science. 1973 ; 182 : 1026-1028.
2 - Blumberg B.S, Alter H.J, Visnich S. A “new” antigen in leukemia sera. JAMA. 1965 ; 191 : 541-546.
3 - Alter H.J, Holland P.V, Purcell R.H et al. Post-transfusion hepatitis after exclusion of commercial and hepatitis B surface antigen positive donors. Ann Intern Med. 1972 ; 77 : 691-699.
4 - Tabor E, Gerety R.J, Drucker J.A et al. Transmission of non-A, non-B hepatitis from man to chimpanzee. Lancet. 1978 ; 1 : 463-466.
5 - Choo Q.L, Kuo G, Weiner A.J et al. Isolation of cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome. Science. 1989 ; 244 : 359-362.
6 - Kuo G, Choo Q.L, Alter H.J et al. An assay for circulating antibodies to a major etiologic virus of human non-A, non-B viral hepatitis genome. Science. 1989 ; 244 : 362-364.
7 - Alter H.J. Discovery of non-A, non-B hepatitis and identification of its etiology. Science. 1989 ; 244 : 359-362.
8 - Brun-Vezinet F, Barin F, Costagliola D, Hervé P. Rapport du Groupe d'experts sur l'intérêt de la détection des acides nucléiques des virus VIH, VHB et VHC en matière de transfusion sanguine et de greffes. Paris : Direction Générale de la Santé,1999.
9 - Moradpour D, Penin F, Rice C.M. Replication of hepatitis C virus. Nat Rev Microbiol. 2007 ; 5 : 453-463.
10 - Bartenschlager R. Hepatitis C virus replicons: potential role for drug development. Nat Rev Drug Discov. 2002; 1 : 911-916. 10.1038/nrd942

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.