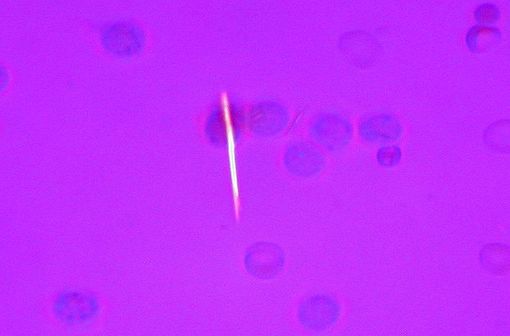
Cristal d'urate dans du liquide synovial (illustration @Ed Uthman sur Wikimedia).
Une nouvelle spécialité à base de probénécide est désormais commercialisée en France sous le nom de SANTURIL 500 mg comprimé sécable.
SANTURIL a obtenu une AMM nationale en avril 2019, sur la base d'un usage médical bien établi.
Retour du probénécide en France
Depuis l'arrêt de commercialisation de BENEMIDE 500 mg comprimé sécable en 2016, le marché français était approvisionné en probénécide via le dispositif d'importation d'une spécialité en provenance d'Allemagne, PROBENECID BIOKANOL 500 mg comprimé sécable, réservé à la rétrocession hospitalière.
La commercialisation de SANTURIL permet une mise à disposition pérenne de ce principe actif en France, en ville et à l'hôpital.
Traitement de seconde intention de l'hyperuricémie
SANTURIL est indiqué dans le traitement de l'hyperuricémie symptomatique (arthrite goutteuse) chez les patients présentant une résistance ou une intolérance aux inhibiteurs de la xanthine oxydase (allopurinol, fébuxostat) [cf. VIDAL Reco "Goutte"].
Une utilisation en monothérapie ou en association avec un inhibiteur de la xanthine oxydase (sauf en cas d'intolérance) est envisageable.
SANTURIL en pratique
Chez l'adulte, la dose quotidienne de probénécide est instaurée selon le schéma suivant :
- 0,5 comprimé (250 mg) 2 fois par jour pendant 1 semaine en début de traitement (une barre de cassure permet de diviser le comprimé en 2 doses égales) ;
- 1 comprimé (500 mg) 2 fois par jour. Le traitement doit être poursuivi à cette dose quotidienne jusqu'à ce que l'uricémie se normalise et que les dépôts d'urate dans les tissus aient été détruits.
L'augmentation progressive de la posologie se justifie par une excrétion importante d'acide urique observée en début de traitement.
Par la suite, une réduction progressive de la dose est possible.
- Prévoir un apport liquidien suffisant
Les comprimés sécables doivent être avalés avec une grande quantité de liquide au cours des repas.
- Une utilisation à écarter dans certaines situations
- une altération de la fonction rénale (clairance de la créatinine inférieure à 50 mL/min) ;
- les enfants âgés de moins de 15 ans ;
- la crise de goutte aiguë.
Pour aller plus loin
- Liste II
- Boîte de 30, CIP 3400930176948
- Remboursable à 30 % (Journal officiel du 21 juillet 2020 - texte 22)
- Prix public TTC = 17,16 euros
- Agrément aux collectivités (Journal officiel du 21 juillet 2020 - texte 23)
- Laboratoire Lipomed GmbH
Pour aller plus loin
Avis de la Commission de la Transparence - SANTURIL (HAS, 5 février 2020)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.