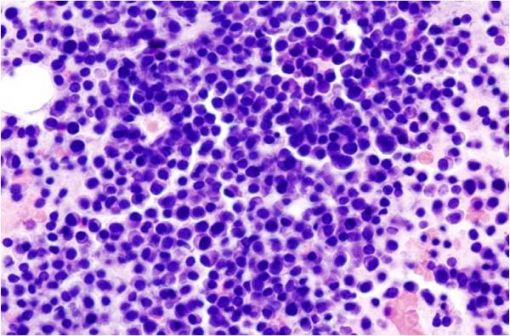
Image histopathologique d'un myélome multiple (extrait de la moelle osseuse), coloration à l'hématoxyline et à l'éosine (illustration @Wikimedia).
Anticorps monoclonal humain de type IgG1K, DARZALEX 20 mg/mL solution à diluer pour perfusion (daratumumab) est le premier représentant de la classe des anticorps monoclonaux ciblant le récepteur transmembranaire CD38, exprimé en grande quantité à la surface des cellules tumorales du myélome multiple.
En France, il a bénéficié d'une ATU nominative, puis d'une ATU de cohorte en 2016, avant d'obtenir son AMM (autorisation de mise sur le marché) européenne la même année.
Il bénéficie du statut de médicament orphelin.
DARZALEX dispose de 3 indications dans le traitement du myélome multiple (Cf. VIDAL Reco "Myélome multiple") :
- en monothérapie, dans le traitement des patients adultes atteints d'un myélome multiple en rechute et réfractaire, pour lesquels les traitements antérieurs incluaient un inhibiteur du protéasome et un agent immunomodulateur et dont la maladie a progressé lors du dernier traitement ;
- en association avec le lénalidomide et la dexaméthasone, ou le bortézomib et la dexaméthasone, dans le traitement des patients adultes atteints d'un myélome multiple ayant reçu au moins un traitement antérieur ;
- en association avec le bortézomib, le melphalan et la prednisone, dans le traitement des patients adultes atteints d'un myélome multiple nouvellement diagnostiqué et non éligibles à une autogreffe de cellules souches (indication obtenue en 2018).
DARZALEX a fait l'objet de trois avis da la Commission de la Transparence (CT), chacun relatif à l'une de ses indications.
- 2017 : évaluation de DARZALEX en monothérapie
Selon la Commission, la place de DARZALEX en monothérapie reste à définir, faute de comparaison au pomalidomide en 3e ligne.
- 2018 : évaluation de DARZALEX en association à une bithérapie
Considérant les données de ces études, la Commission estime que l'efficacité de ces associations est fondée principalement sur des résultats de survie sans progression et de taux de réponse, toutefois sans gain démontré sur la survie globale et la qualité de vie.
Dans l'attente de résultats en termes de survie globale, la Commission estime que DARZALEX en association à une bithérapie par lénalidomide/dexaméthasone ou par bortézomib/dexaméthasone apporte un SMR important et un progrès thérapeutique mineur (ASMR IV) par rapport à chacune des bithérapies utilisées seules, dans le traitement du myélome multiple après au moins un traitement antérieur.
- 2019 : évaluation de DARZALEX en association à une trithérapie
Selon les résultats de cette étude, la supériorité de l'ajout de DARZALEX (daratumumab) au protocole MPV (D-MPV) a été démontrée par rapport au protocole MPV administré seul en termes de survie sans progression, toutefois sans gain démontré sur la survie globale et la qualité de vie à la date de l'analyse.
La fréquence d'événements indésirables graves a été plus élevée avec l'association D-MPV (41,6 % versus 32,5%), avec notamment davantage de pneumonies graves (10,1% versus 3,1%).
Considérant ces données, la CT estime que DARZALEX en association au bortézomib, au melphalan et à la prednisone (protocole MPV) apporte un SMR important et une amélioration du SMR mineure (ASMR IV) par rapport au protocole MPV administré seul dans le traitement des patients adultes atteints d'un myélome multiple nouvellement diagnostiqué et non éligibles à une autogreffe de cellules souches.
Dans cette indication, la place de DARZALEX est celle d'un traitement de 1re intention.
En l'absence de données comparatives, la place de DARZALEX vis-à-vis du protocole Rd (lénalidomide/dexaméthasone), l'autre association admise en première ligne chez les patients inéligibles à une autogreffe de cellules souches, n'est pas connue. Une étude comparant D-Rd au protocole Rd est en cours.
DARZALEX en pratique
DARZALEX doit être administré par un professionnel de santé dans un environnement où l'ensemble des moyens de réanimation est disponible.
DARZALEX peut causer des réactions liées à la perfusion (RLP) graves, y compris des réactions anaphylactiques.
Une médication pré-perfusion (antihistaminiques, antipyrétiques et corticoïdes) et post-perfusion (corticoïdes oraux) doit être administrée afin de réduire ce risque.
La dose recommandée de DARZALEX est de 16 mg/kg de masse corporelle, administrée en perfusion intraveineuse selon un calendrier d'administration tenant compte de l'indication soit dans le myélome multiple nouvellement diagnostiqué (Cf. Tableau I), soit dans le myélome multiple en rechute/réfractaire (Cf. Tableau II).
| Tableau I - Calendrier d'administration de DARZALEX en association avec le bortézomib, le melphalan et la prednisone [MPV] (traitement par cycles de 6 semaines) |
|
| Semaines | Fréquence d'administration |
| Semaines 1 à 6 | Hebdomadaire (6 doses au total) |
| Semaines 7 à 54a | Toutes les 3 semaines (16 doses au total) |
| À partir de la semaine 55, jusqu'à progression de la maladieb |
Toutes les 4 semaines |
b La première dose selon le calendrier d'administration toutes les 4 semaines est administrée en Semaine 55.
| Tableau II - Calendrier d'administration de DARZALEX en monothérapie et en association avec le lénalidomide (traitement par cycles de 4 semaines) |
|
| Semaines | Fréquence d'administration |
| Semaines 1 à 8 | Hebdomadaire (8 doses au total) |
| Semaines 9 à 24a | Toutes les 2 semaines (8 doses au total) |
| À partir de la semaine 25, jusqu'à progression de la maladieb |
Toutes les 4 semaines |
b La première dose selon le calendrier d'administration toutes les 4 semaines est administrée en Semaine 25.
Tous les patients doivent être surveillés tout au long de la perfusion pour détecter une RLP.
En cas de RLP, quels qu'en soient le grade ou la sévérité, la perfusion de DARZALEX sera immédiatement interrompue et les symptômes pris en charge. La surveillance du patient devra continuer après la perfusion jusqu'à la résolution des symptômes.
En cas de RLP, quels qu'en soient le grade ou la sévérité, la perfusion de DARZALEX sera immédiatement interrompue et les symptômes pris en charge. La surveillance du patient devra continuer après la perfusion jusqu'à la résolution des symptômes.
Identité administrative
- Liste I
- Réservé à l'usage hospitalier
- Prescription réservée aux spécialistes en oncologie ou en hématologie ou aux médecins compétents en cancérologie ou en maladie du sang
- Surveillance particulière pendant le traitement
- Flacon de 5 mL, CIP 3400955021803, UCD 3400894178880, tarif de responsabilité HT = 364 euros par UCD
- Flacon de 20 mL, CIP 3400955021810, UCD 3400894178712, tarif de responsabilité HT = 1 456 euros par UCD
- Agrément aux collectivités avec prise en charge en monothérapie et en association à une bithérapie (Journal officiel du 18 juin 2019, texte 9)
- Prise en charge en sus des prestations d'hospitalisation, uniquement en association à une bithérapie (Journal officiel du 18 juin 2019, texte 8)
- Laboratoire Janssen-Cilag
Pour aller plus loin
Arrêté du 13 juin 2019 - Agrément aux collectivités de DARZALEX, avec prise en charge en monothérapie et en trithérapie (Journal officiel du 18 juin 2019 - texte 9)
Arrêté du 12 juin 2019 - Inscription de DARZALEX sur la liste en sus des prestations d'hospitalisation (Journal officiel du 18 juin 2019 - texte 8)
Avis de la Commission de la Transparence - Indication de DARZALEX en monothérapie (HAS, 22 novembre 2017)
Avis de la Commission de la Transparence - Extension de prise en charge de DARZALEX en association à une bithérapie (HAS, 21 février 2018)
Avis de la Commission de la Transparence - Extension d'indication en association à une trithérapie (HAS, 17 avril 2019)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire






Commentaires
Cliquez ici pour revenir à l'accueil.