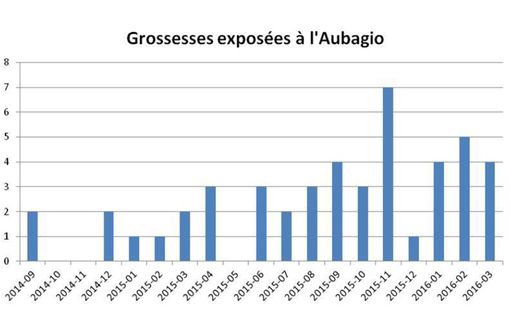
Evolution du nombre de grossesses exposées à AUBAGIO au cours du temps (source : ANSM et SNIIRAM).
AUBAGIO est contre-indiqué pendant la grossesse, rappelle l'ANSM
Dans un communiqué du 15 janvier 2019, l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) rappelle qu'AUBAGIO 14 mg comprimé pelliculé (tériflunomide) est :
- contre-indiqué pendant la grossesse,
- contre-indiqué chez les femmes en âge de procréer n'utilisant pas de contraception efficace.
Encadré - Indication thérapeutique d'AUBAGIO et modalités de prescription
| Traitement des patients adultes atteints de formes rémittentes de sclérose en plaques (SEP-RR) (Cf. VIDAL Reco "Sclérose en plaques"). AUBAGIO est un médicament d'exception, sous prescription réservée aux spécialistes en neurologie. |
Exposition de femmes enceintes au tériflunomide : 47 cas français relevés entre mi-2014 et fin 2016
Ce rappel de bon usage d'AUBAGIO a été déclenché par la publication des résultats d'une étude de cohorte française, rapportant des dizaines de cas d'exposition au tériflunomide chez des femmes enceintes.
L'objectif de l'étude SPAM (Safety-Pregnancy-Aubagio®-Multiple sclerosis) était de dénombrer et d'étudier les grossesses exposées à AUBAGIO en France, à partir des données de l'assurance maladie (SNIIRAM : Système National d'Information Inter-Régimes de l'Assurance Maladie). Elle a été réalisée par la plateforme de pharmaco-épidémiologie PEPS à Rennes.
Il s'agit d'une étude de cohorte portant sur des femmes en âge de procréer et atteintes de SEP, recevant un traitement (tériflunomide, interféron ou acétate de glatiramère) ou non traitées.
L'analyse a porté sur les données recueillies entre le 1er août 2014 et le 31 décembre 2016 (2014 est l'année de mise à disposition d'AUBAGIO sur le marché français, en ville, voir notre article du 5 novembre 2014) :
- Population totale incluse : 44 008 femmes en âge de procréer atteintes de SEP
- Nombre de grossesses recensées : 2 639
- Nombre de grossesses exposées au tériflunomide : 47
- L'incidence annuelle de grossesses exposées à AUBAGIO était 3 à 4 fois plus faible dans le groupe exposé à AUBAGIO que dans les 2 autres groupes (1,4 vs 5,6 et 4,7 pour 100 patientes-années, respectivement).
- Durée médiane d'exposition à AUBAGIO pendant la grossesse : 45 jours.
Trois fois plus d'interruptions de grossesse que chez les femmes enceintes prenant d'autres traitement
Selon cette étude, les grossesses sous AUBAGIO ont eu pour issues :
- 23 naissances d'enfant(s) né(s) vivant(s),
- 22 interruptions volontaires ou médicales de grossesse (3 fois plus que dans le groupe traité par interféron, glatiramère ou non traité),
- et 2 fausses couches spontanées.
Pas de conséquence détectée pour le moment chez les nouveaux-nés, malgré le non-respect de la procédure d'élimination accélérée
Aucune conséquence immédiate de l'exposition à AUBAGIO sur la santé des nouveau-nés à la naissance n'a été observée.
Autre constat, pour toutes ces grossesses sous AUBAGIO, la procédure d'élimination accélérée n'a pas été réalisée ou de manière incorrecte (durée insuffisante ou tardive).
Le tériflunomide : agent potentiellement embryotoxique et tératogène
Le tériflunomide est un agent immunomodulateur aux propriétés anti-inflammatoires. C'est le métabolite actif prédominant du léflunomide (ARAVA) indiqué dans le traitement de la polyarthrite rhumatoïde et du rhumatisme psoriasique.
Dès l'obtention de son AMM (autorisation de mise sur le marché), une restriction d'utilisation chez les femmes enceintes et les femmes en âge de procréer sans contraception efficace a été introduite, en raison du caractère tératogène et embryotoxique du tériflunomide rapporté dans les études précliniques chez le rat et le lapin à des doses proches de celles utilisées chez la femme.
En cas d'exposition pendant la grossesse, l'ANSM rappelle la nécessité d'une procédure d'élimination rapide
Le tériflunomide est éliminé lentement du plasma. Huit mois en moyenne sont nécessaires pour atteindre une concentration plasmatique inférieure à 0,02 mg/L.
Les femmes en âge de procréer doivent donc utiliser une contraception efficace pendant et après un traitement par tériflunomide, tant que la concentration plasmatique en tériflunomide reste supérieure à 0,02 mg/L.
Après l'arrêt du traitement, il est possible d'accélérer l'élimination du tériflunomide, afin d'en diminuer le plus rapidement possible la concentration plasmatique.
Une procédure spécifique est décrite dans le RCP (résumé des caractéristiques du produit) d'AUBAGIO. Elle doit être entreprise en cas de désir de grossesse ou de survenue d'une grossesse non planifiée chez des femmes traitées par AUBAGIO.
Encadré : Procédure d'élimination accélérée après l'arrêt du traitement par le tériflunomide (Cf. Monographie VIDAL AUBAGIO - rubrique Grossesse et allaitement)
Après avoir suivi une des deux procédures d'élimination accélérée, vérifier la concentration plasmatique à l'aide de 2 dosages réalisés à au moins 14 jours d'intervalle et prévoir un mois et demi entre la date de première détection d'une concentration inférieure à 0.02 mg /L et la date de fécondation. La colestyramine et la poudre de charbon actif peuvent influencer l'absorption des œstrogènes et des progestatifs : la fiabilité des contraceptifs oraux ne peut pas être garantie pendant la procédure d'élimination accélérée. L'utilisation d'autres moyens de contraception est recommandée pendant cette période. |
Pour aller plus loin
AUBAGIO (tériflunomide) : rappel de la contre-indication pendant la grossesse - Point d'information (ANSM, 15 janvier 2019)
Etude "SPAM (Safety-Pregnancy-Aubagio®-Multiple sclerosis)" (ANSM, 2019)
Documents de réduction du risque (MARR)
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.