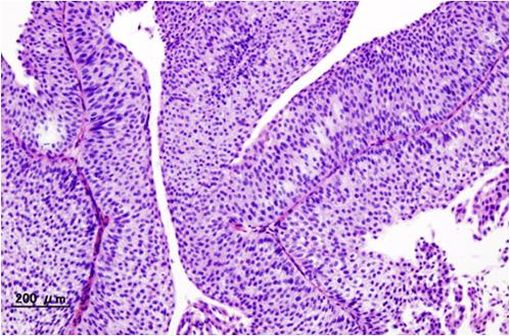
Image histo-pathologique d'un carcinome urothélial de la vessie. Biopsie transurétrale. Coloration H&E (illustration @Wikimedia).
Restriction d'indication dans le carcinome urothélial
S'appuyant sur les données préliminaires de 2 études cliniques, l'une portant sur KEYTRUDA (pembrolizumab), KEYNOTE-361, et l'autre sur TECENTRIQ (atezolizumab), IMvigor130, l'indication de ces anticorps monoclonaux hospitaliers dans le traitement du carcinome urothélial des patients adultes inéligibles à une chimiothérapie à base de cisplatine a été restreinte pour tenir compte du degré d'expression tumorale de PD-L1 (Cf. Encadré 1).
Encadré 1 - La protéine PD-L1 en bref
| PD-L1 (de l'anglais Programmed Death-Ligand 1) est une protéine transmembranaire exprimée à la surface des cellules présentatrices d'antigène. Sa liaison au récepteur de mort cellulaire programmée 1 (PD-R1, Programmed Death-Receptor 1), exprimé à la surface des lymphocytes T cytotoxiques (CD8) et à fonction régulatrice (CD4) activés, inhibe leur réponse immunitaire. Cette voie de signalisation constitue un point de contrôle du système immunitaire et permet de moduler les réactions immunitaires excessives. Toutefois, PD-L1 peut également être exprimée par diverses cellules néoplasiques. Une surexpression de PD-L1 par certaines tumeurs pourrait faciliter leur évasion de la réponse immunitaire anti-tumorale locale. Dans le cadre du traitement anti-tumoral, le pembrolizumab et l'atezolizumab bloquent l'interaction récepteur/ligand PD-R1/PD-L1 et potentialisent les réponses immunitaires des cellules T. |
Désormais, dans le cadre d'un traitement de première ligne d'un carcinome urothélial chez les patients inéligibles au cisplatine :
- KEYTRUDA ne doit être utilisé que lorsque les tumeurs expriment PD-L1 avec un CPS supérieur ou égal à 10 (CPS pour score positif combiné : nombre de cellules exprimant le PD-L1 (cellules tumorales, lymphocytes et macrophages) divisé par le nombre total de cellules tumorales multiplié par 100),
- TECENTRIQ ne doit être utilisé que si le patient présente une expression de PD-L1 supérieure ou égale à 5 % (c'est-à-dire plus de 5 % de cellules immunitaires marquées positives pour PD-L1).
Pour KEYTRUDA, la prise en compte de l'expression en PD-L1 est déjà mentionnée dans le cadre du cancer bronchique non à petites cellules (Cf. VIDAL Reco « cancer du poumon »).
Faible expression de PD-L1 : taux de survie réduit
Les données préliminaires des études cliniques de phase III, KEYNOTE-361 et IMvigor130, montrent que le taux de survie est réduit chez les patients dont la tumeur présente une faible expression de la protéine PD-L1, traités en première ligne en monothérapie respectivement par KEYTRUDA et par TECENTRIQ, par rapport à une chimiothérapie de référence.
- Etude KEYNOTE-361 relative à KEYTRUDA
Les données préliminaires montrent un taux de survie réduit lorsque KEYTRUDA est utilisé en monothérapie chez les patients dont les tumeurs expriment PD-L1 à un taux faible, avec un CPS inférieur à 10, en comparaison à la chimiothérapie standard.
Depuis le mois de février, les patients dont les tumeurs expriment PD-L1 avec un CPS inférieur à 10 ne sont plus inclus dans l'étude.
- Etude IMvigor130 relative à TECENTRIQ
- Bras A : atezolizumab en association à une chimiothérapie à base de platine [cisplatine ou carboplatine] et gemcitabine ;
- Bras B : atezolizumab en monothérapie ;
- Bras C : placebo en association à une chimiothérapie à base de platine [cisplatine ou carboplatine] et gemcitabine.
D'après les données préliminaires, on observe une survie diminuée dans le bras B, lorsque TECENTRIQ est utilisé en monothérapie, en comparaison à une chimiothérapie à base de platine :
- chez des patients atteints d'un carcinome urothélial métastatique qui n'ont pas reçu de traitement préalable ;
- et dont les tumeurs présentent une faible expression de la protéine PD-L1 : moins de 5 % de cellules immunitaires marquées positives pour PD-L1.
Pas de changement dans le traitement de seconde ligne du carcinome urothélial
L'indication de KEYTRUDA et de TECENTRIQ n'est pas modifiée dans le traitement des adultes atteints d'un carcinome urothélial localement avancé ou métastatique ayant reçu une chimiothérapie antérieure à base de sels de platine.
Pour aller plus loin
Keytruda (pembrolizumab) : Restriction d'indication dans le traitement des patients adultes atteints d'un carcinome urothélial localement avancé ou métastatique inéligibles à une chimiothérapie à base de cisplatine (ANSM, 10 juillet 2018)
Lettre du laboratoire MSD aux professionnels de santé - KEYTRUDA (sur le site de l'ANSM, juillet 2018)
Tecentriq (atezolizumab): Restriction d'indication dans le traitement des patients adultes atteints d'un carcinome urothélial localement avancé ou métastatique inéligibles à une chimiothérapie à base de cisplatine (ANSM, 10 juillet 2018)
Lettre du laboratoire Roche aux professionnels de santé - TECENTRIQ (sur le site de l'ANSM, juillet 2018)
Sur VIDAL.fr
Immunothérapie contre le cancer : prometteuse, mais "attention aux emballements" (The Lancet) (5 juillet 2018)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.