Représentation en 3D d'un virus de l'hépatite C (illustration).
Nouvelle association fixe d'AAD dans l'hépatite C chronique
EPCLUSA 400 mg/100 mg comprimé pelliculé est une nouvelle spécialité antivirale d'action directe (AAD) indiquée chez l'adulte dans le traitement de l'infection chronique par le virus de l'hépatite C (VHC) (Cf. VIDAL Reco "Hépatite C").
EPCLUSA est la 1re association fixe de 2 molécules pangénotypiques, c'est-à-dire actives sur tous les génotypes du VHC (1 à 6) :
- le sofosbuvir (400 mg par comprimé), analogue nucléotidique spécifique du virus de l'hépatite C (VHC), inhibiteur de la polymérase NS5B. Ce principe actif est déjà commercialisé en France, seul dans le médicament SOVALDI, et en association avec le lédipasvir dans le médicament HARVONI ;
- le velpatasvir (100 mg par comprimé), inhibiteur de la polymérase NS5A, jamais commercialisé en France à ce jour.
Une efficacité virologique pangénomique importante
Dans son avis du 19 octobre 2016, la Commission de la transparence (CT) a évalué l'efficacité d'EPCLUSA sur la base des 4 études de phase III suivantes (Cf. Tableau I) :
Tableau I - Études réalisées avec EPCLUSA chez les patients infectés par un VHC
de génotype 1 à 6
de génotype 1 à 6
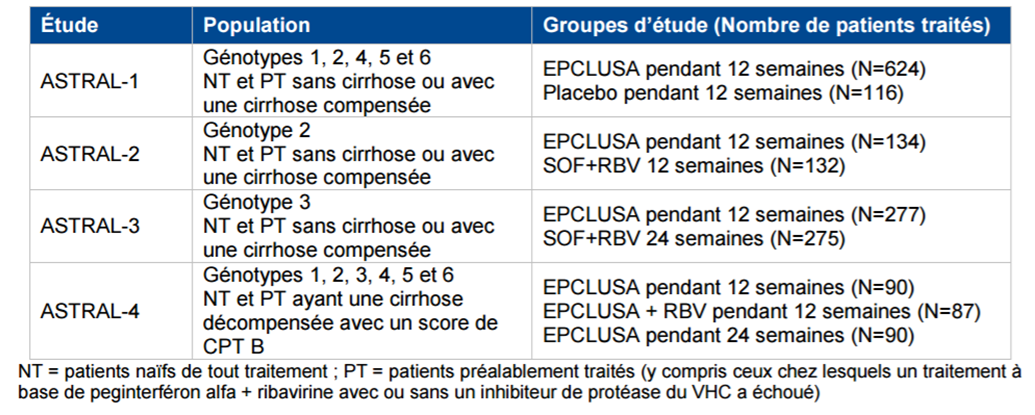
Le critère d'évaluation principal était la réponse virologique soutenue (taux d'ARN du VHC).
Les résultats de ces études ont été en faveur d'une efficacité pangénomique importante, supérieure à 90 %, avec 12 semaines de traitement sans ajout de ribavirine pour la majorité des patients.
Pour les patients de génotypes 1, 3 et 4, les quantités d'effet observées ont été du même ordre que celles rapportées avec les options thérapeutiques recommandées (HARVONI, SOVALDI + DAKLINZA).
Pour le génotype 2, EPCLUSA a été supérieur à la bithérapie SOVALDI + RIBAVIRINE pendant 12 semaines mais avec une différence de quantité d'effet modeste, en particulier chez les patients naïfs de traitement.
Pour les génotypes 5 et 6, les données sont limitées et ne permettent pas de différencier les médicaments disponibles entre eux.
En termes de tolérance, de résistance et d'interactions, le profil d'EPCLUSA a été satisfaisant et comparable à celui des autres combinaisons à base de sofosbuvir.
La CT précise qu'"aucune étude clinique n'a comparé les différentes combinaisons d'AAD actuellement disponibles et qu'aucun traitement ne peut être considéré comme optimal pour tous les patients". Le choix thérapeutique portera sur le traitement le mieux adapté à chaque situation clinique et virologique (Cf. Tableau II), de manière personnalisée et en accord avec le patient.
Tableau II - Schémas thérapeutiques préférentiels chez les patients naïfs,
pour les génotypes couverts par les AMM
pour les génotypes couverts par les AMM
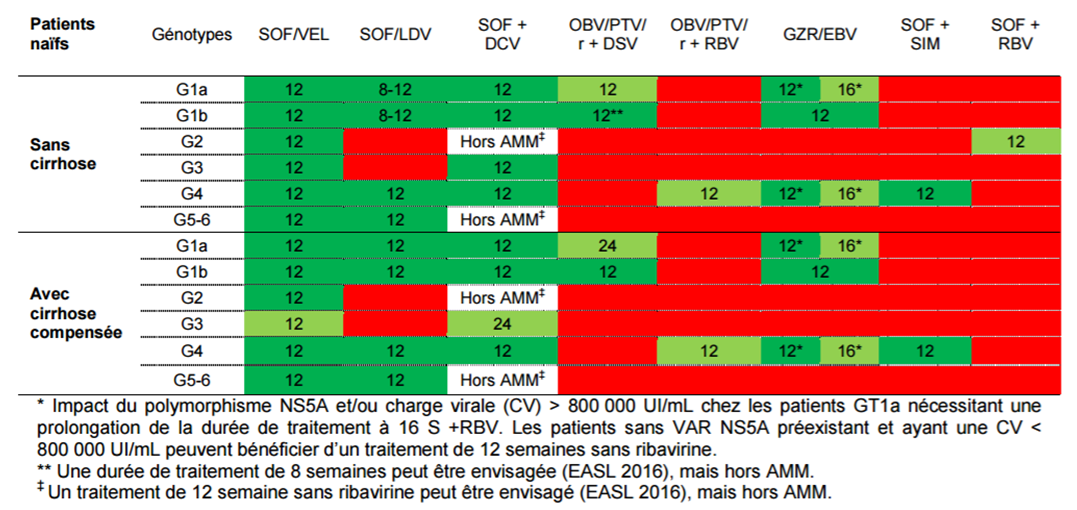
Avec un service médical rendu (SMR) jugé important et une amélioration du SMR modérée (ASMR IV), EPCLUSA fait ainsi partie des options thérapeutiques pour le traitement des patients ayant une hépatite C chronique de génotypes 1 à 6, sans ou avec cirrhose.
EPCLUSA en pratique
L'initiation et la surveillance du traitement par EPCLUSA doivent être confiées à un médecin expérimenté dans la prise en charge des patients infectés par le VHC.
La posologie est de 1 comprimé 1 fois par jour, avec ou sans nourriture.
La durée de traitement est de 12 semaines.
L'adjonction de ribavirine peut être envisagée :
- chez les patients infectés par un VHC de génotype 3 avec une cirrhose compensée ;
- chez les patients en échec d'un traitement précédent contenant un inhibiteur de la NS5A. Dans ce cas, la durée du traitement est de 24 semaines.
EPCLUSA est associé à la ribavirine chez les patients avec une cirrhose décompensée.
Surveillance et contrôle pendant le traitement par EPCLUSA
Plusieurs situations nécessitent une surveillance particulière pendant le traitement par EPCLUSA et notamment en cas de traitement concomitant.
- Administration concomitante avec l'amiodarone
Si l'utilisation concomitante de l'amiodarone est jugée nécessaire ou si un traitement par amiodarone a été prescrit au cours des mois précédents, les patients doivent être étroitement surveillés.
Les patients identifiés comme étant à risque élevé de bradyarythmie doivent faire l'objet d'une surveillance continue pendant 48 heures en milieu hospitalier adapté.
En présence de symptômes de bradycardie et de troubles de la conduction, une consultation médicale s'impose.
- Administration chez des sujets traités par antagonistes de la vitamine K
- Autres interaction médicamenteuses
A ce titre, il convient par exemple, avec les médicaments anti-acides, de respecter un intervalle de 4 heures entre la prise de l'anti-acide et celle d'EPCLUSA. Une augmentation du pH gastrique entraîne une diminution de la concentration du velpatasvir, et une baisse d'efficacité antivirale.
EPCLUSA fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité (Cf. Infos Pratiques VIDAL - Médicaments sous surveillance renforcée). Les professionnels de santé déclarent tout effet indésirable suspecté (Cf. ANSM - Comment déclarer un effet indésirable ?).
Identité administrative
- Liste I
- Prescription hospitalière réservée aux spécialistes en gastro-entérologie et hépatologie, en médecine interne ou en infectiologie
- Flacon de 28, CIP 3400930067314, UCD 3400894198062
- Agrément aux collectivités (Journal officiel du 1er avril 2017 - texte 22)
- Inscription sur la liste de rétrocession avec prise en charge à 100 % (Journal officiel du 1er avril 2017 - texte 24 et Journal officiel du 11 avril 2017 - texte 14)
- Prix de vente HT par UCD = 513,009 euros (Journal officiel du 11 avril 2017 - texte 49)
- Laboratoire Gilead Sciences
Conditions de prise en charge d'EPCLUSA et de l'ensemble des AAD
L'agrément à l'usage des collectivités et la prise en charge d'EPCLUSA sont subordonnés au respect de la condition relative à l'organisation des soins suivante : l'initiation du traitement est subordonnée à la tenue d'une réunion de concertation pluridisciplinaire et ce uniquement pour les patients :
|
Pour aller plus loin
Avis de la Commission de la transparence - EPCLUSA (HAS, 19 octobre 2016)
Sur VIDAL.fr
HARVONI et SOVALDI : prise en charge universelle dans l'hépatite C chronique (6 avril 2017)
DAKLINZA et OLYSIO : prise en charge universelle dans l'hépatite C chronique (23 mars 2017)
EXVIERA et VIEKIRAX : prise en charge universelle dans l'hépatite C chronique (28 février 2017)
Hépatite C chronique : ZEPATIER (elbasvir, grazoprevir), nouvelle association d'antiviraux d'action directe (10 janvier 2017)
Antiviraux d'action directe contre l'hépatite C : extension du remboursement (13 juin 2016)
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.