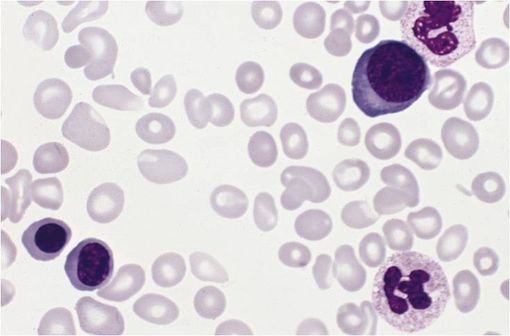
Frottis sanguin d'un patient atteint par la maladie de Vaquez (illustration @Wikimedia).
Un nouveau dosage à 10 mg de ruxolitinib
Un nouveau dosage de JAKAVI comprimé à 10 mg de ruxolitinib est désormais commercialisé en France, en complément des dosages à 5 mg, 15 mg et 20 mg.
Cet antinéoplasique inhibiteur des tyrosines kinases a reçu une AMM (autorisation de mise sur le marché) dans les mêmes indications que JAKAVI 5 mg, 15 mg et 20 mg à savoir :
- le traitement de la splénomégalie ou des symptômes liés à la maladie chez l'adulte atteint de myélofibrose primitive (appelée également myélofibrose chronique idiopathique), de myélofibrose secondaire à la maladie de Vaquez (polycythémie vraie) ou de myélofibrose secondaire à la thrombocytémie essentielle ;
- dans le traitement des adultes atteints de la maladie de Vaquez (polycythémie vraie, PV) qui sont résistants ou intolérants à l'hydroxyurée.
Les autres dosages de JAKAVI remboursables dans la maladie de Vaquez en 2e intention
Outre la mise à disposition de ce nouveau dosage à 10 mg, les autres dosages de JAKAVI à 5 mg, 15 mg et 20 mg sont désormais remboursables dans le traitement des adultes atteints de la maladie de Vaquez qui sont résistants ou intolérants à l'hydroxyurée.
L'efficacité et la tolérance de JAKAVI ont été évaluées au cours de l'étude RESPONSE (N Engl J Med 2015), une étude de phase III randomisée ouverte réalisée chez 222 patients en échec de traitement par hydroxyurée.
Le ruxolitinib était comparé au meilleur traitement disponible.
La proportion de patients ayant obtenu une réponse au traitement (contrôle de l'hématocrite et réduction du volume splénique d'au moins 35%) à la semaine 32 (critère de jugement principal) a été supérieure dans le groupe ruxolitinib (23/110 patients, 20,9%) par rapport au groupe meilleur traitement disponible (1/112, 0,9%), avec un RR = 28,64, un IC95% = [4,50 ; 1 206] (p < 0,0001).
En termes de tolérance, les données fournies dans cette nouvelle indication sont comparables au profil de tolérance connu jusqu'à présent pour JAKAVI, avec pour principaux événements indésirables observés dans l'étude RESPONSE : l'anémie (24,5%), les céphalées (20,9%), la diarrhée (19,1%), la fatigue (17,3%), le prurit (17,3%), les vertiges (13,6%) et la thrombocytopénie (11,8%).
Dans son avis du 25 novembre 2015, la Commission de la transparence a considéré que le SMR (service médical rendu) du ruxolitinib est important, et que l'ASMR (amélioration du service médical rendu) est mineure "en raison d'une meilleure tolérance à court terme (effets indésirables et amélioration des symptômes) et en l'absence de données de tolérance à long terme".
Le ruxolitinib, comme le pipobroman (VERCYTE), sont des traitements de seconde ligne de la maladie de Vaquez, lorsque le traitement de première intention (l'hydroxyurée, HYDREA) n'est pas approprié.
Des dosages adaptés aux différentes situations cliniques
Dans la maladie de Vaquez (PV) en 2e intention, le nouveau dosage de JAKAVI à 10 mg est adapté à la posologie initiale recommandée, à savoir 10 mg 2 fois par jour.
La dose de JAKAVI peut être modifiée en fonction de la tolérance et de l'efficacité :
- Des diminutions de la dose doivent être envisagées :
- Si le taux d'hémoglobine diminue en dessous de 12 g/dl.
- Elles sont recommandées en cas de diminution en dessous de 10 g/dl.
- Le traitement doit être interrompu :
- Lorsque le taux d'hémoglobine est inférieur à 8 g/dl.
- Après récupération des numérations sanguines au-dessus de ces seuils, le traitement peut être repris à la dose de 5 mg deux fois par jour, et la dose augmentée progressivement en surveillant étroitement l'hémogramme complet, avec numération et formule leucocytaire.
- La dose peut être augmentée :
- Si l'efficacité est considérée comme insuffisante et que les numérations sanguines sont adéquates, la dose peut être augmentée par paliers de 5 mg deux fois par jour au maximum, jusqu'à la dose maximale de 25 mg deux fois par jour.
- La dose initiale ne doit pas être augmentée durant les quatre premières semaines de traitement et par la suite, les augmentations de doses doivent se faire à intervalles de temps d'au moins 2 semaines. La dose maximale de JAKAVI est de 25 mg deux fois par jour.
- D'autres situations nécessitent une adaptation posologique :
- L'administration concomitante d'inhibiteurs puissants du CYP3A4 ou de fluconazole : la dose unitaire de JAKAVI doit être diminuée d'environ 50 %, à administrer 2 fois par jour ;
- Une insuffisance rénale sévère (clairance de la créatinine inférieure à 30 mL/min) ;
- Une insuffisance hépatique.
Identité administrative de JAKAVI 10 mg
- Liste I
- Prescription hospitalière réservée aux spécialistes en hématologie ou aux médecins compétents en maladies du sang
- Surveillance particulière pendant le traitement
- Boîte de 56, CIP 3400930002452
- Remboursable à 100 % (Journal officiel du 29 septembre 2016 - texte 33)
- Prix public TTC = 3 645,85 euros
- Agrément aux collectivités (Journal officiel du 29 septembre 2016 - texte 34)
- Laboratoire Novartis Pharma
L'étude pivot
Vannucchi AM, Kiladjian JJ, Griesshammer M, Masszi T, Durrant S, Passamonti F et al. Ruxolitinib versus standard therapy for the treatment of polycythemia vera. N Engl J Med 2015 ; 372 : 426-35
Pour aller plus loin
Arrêté du 22 septembre 2016 modifiant la liste des spécialités pharmaceutiques remboursables aux assurés sociaux - Extension du remboursement (Journal officiel du 27 septembre 2016 - texte 11)
Arrêté du 22 septembre 2016 modifiant la liste des spécialités pharmaceutiques agréées à l'usage des collectivités et divers services publics - Extension de l'agrément aux collectivités (Journal officiel du 27 septembre 2016 - texte 12)
Avis de la Commission de la Transparence - Extension de prise en charge dans la maladie de Vaquez des dosages à 5, 15 et 20 mg (HAS, 25 novembre 2015)
Avis de la Commission de la Transparence - Nouveau dosage à 10 mg (HAS, 3 février 2016)
Sur VIDAL.fr
JAKAVI (ruxolitinib) est désormais disponible en ville (6 juin 2013)
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute lãactualitûˋ par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)

.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.