Radiographie thoracique montrant une insuffisance cardiaque (illustration).
ENTRESTO, nouveau mécanisme d'action dans l'insuffisance cardiaque chronique
ENTRESTO comprimé pelliculé (sacubitril/valsartan) est un nouveau médicament indiqué chez les patients adultes dans le traitement de l'insuffisance cardiaque chronique symptomatique à fraction d'éjection réduite (Cf. Reco VIDAL Insuffisance cardiaque chronique).
ENTRESTO est une association fixe de valsartan, un antagoniste des récepteurs de l'angiotensine II (ARA II), et de sacubitril, le premier représentant d'une nouvelle classe thérapeutique, les inhibiteurs de néprilysine.
De ce fait, ENTRESTO présente un double mécanisme d'action en inhibant simultanément le récepteur de type 1 de l'angiotensine II (AT1), via le valsartan, et la néprilysine via le sacubitril et son métabolite actif, le LBQ657.
Des effets cardiovasculaires complémentaires
Chez les patients atteints d'insuffisance cardiaque, les effets cardiovasculaires d'ENTRESTO sont ainsi complémentaires et résultent :
- De l'augmentation des peptides qui sont dégradés par la néprilysine tels que les peptides natriurétiques par son métabolte actif (LBQ657) :
- Les peptides natriurétiques exercent leurs effets physiologiques en activant des récepteurs membranaires à activité guanylate-cyclase, entraînant une augmentation des concentrations du second messager hormonal, la guanosine monophosphate cyclique (GMPc).
- Ceci peut entraîner une vasodilatation, une natriurèse et une diurèse, une augmentation de la filtration glomérulaire et du débit sanguin rénal, une inhibition de la libération de rénine et d'aldostérone ainsi qu'une diminution de l'activité sympathique, et des effets anti-hypertrophique et anti-fibrotique.
- Et de l'inhibition simultanée des effets de l'angiotensine II par le valsartan :
- Le valsartan empêche les effets néfastes cardiovasculaires et rénaux de l'angiotensine II en bloquant sélectivement les récepteurs AT1 ainsi que la libération d'aldostérone dépendante de l'angiotensine II.
- Cela prévient l'activation continue du système rénine-angiotensine-aldostérone et provoque une vasoconstriction, une rétention hydrosodée, une activation de la croissance et de la prolifération des cellules entraînant un remodelage cardiovasculaire mal adapté.
Une spécialité hospitalière disponible sous trois dosages
Ce médicament est disponible à l'hôpital sous 3 dosages :
- ENTRESTO 24 mg/26 mg, correspondant à 24,3 mg de sacubitril et 25,7 mg de valsartan par unité de prise ;
- ENTRESTO 49 mg/51 mg, correspondant à 48,6 mg de sacubitril et 51,4 mg de valsartan par unité de prise ;
- ENTRESTO 97 mg/103 mg, correspondant à 97,2 mg de sacubitril et 102,8 mg de valsartan par unité de prise.
Avant d'obtenir une AMM européenne en septembre 2015, il a fait l'objet d'une ATU de cohorte à partir de mai 2015, sous le nom LCZ696
Ce médicament fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
Etude PARADIGM-HF : supériorité d'ENTRESTO versus énalapril en termes de décès et d'hospitalisation
L'efficacité d'ENTRESTO ( 97 mg/103 mg x 2 / jour) a été évaluée dans l'étude de phase III, PARADIGM-HF (McMurray and al. N Engl J Med 2014), multicentrique, randomisée en double aveugle versus énalapril (10 mg x 2 / jour), menée chez 8 442 patients souffrant d'insuffisance cardiaque chronique symptomatique (de classe II-IV de la NYHA) à fraction d'éjection réduite (FEVG <= 40 %), suivis sur une médiane de 27 mois.
Avant l'inclusion, les patients étaient tous traités de manière optimale par une association IEC/ARA II (dans plus de 99 %), des bêtabloquants (94 %), des antagonistes de l'aldostérone (58 %) et des diurétiques (82 %).
Le critère de jugement principal était un critère composite regroupant les décès d'origine cardiovasculaire ou les hospitalisations pour insuffisance cardiaque.
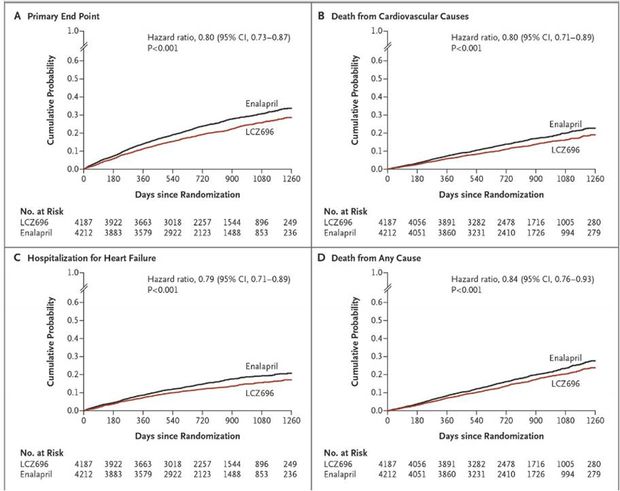
L'essai a été arrêté prématurément en raison de la supériorité significative des résultats obtenus avec ENTRESTO (Cf. Figure 1):
- sur le critère de jugement principal : 914 patients (21,8%) dans le groupe sacubitril/valsartan versus 1 117 patients (26,5%) dans le groupe énalapril (RR = 0,80; IC 95% : [0,73 ; 0.87] ; p < 0,001) ;
- en termes de décès toutes causes : 711 patients (17,0 %) dans le groupe sacubitril/valsartan 835 patients (19,8 %) dans le groupe énalapril (RR = 0,84; IC 95% : [0.76 ; 0.93] ; p < 0,001),
- dont 558 patients (13,3%) et 693 (16,5%) décès d'origine cardiovasculaire respectivement (RR = 0,80; IC 95% : [0,71 ;0.89] ; p < 0,001).
Figure 1 - Courbes de Kaplan–Meier des principaux résultats de l'étude PARADIGM-HF
(extrait du N Engl J Med 2014 ; 371 : 993-1004).
(extrait du N Engl J Med 2014 ; 371 : 993-1004).
En termes de tolérance, les patients du groupe sacubitril/valsartan ont présenté une hypotension et un
angio-oedème dans une proportion supérieure au groupe énalapril, mais une insuffisance rénale, une hyperkaliémie et une toux dans une moindre proportion que le groupe énalapril.
Une prise en charge d'ENTRESTO sur la base des indications de l'ATU
L'indication de l'AMM européenne, approuvée par le CHMP (Comité des médicaments à usage humain) en septembre 2015, est plus large que l'indication de l'ATU.
Une demande de remboursement et d'agrément aux collectivités est à l'étude.
Dans l'attente, ENTRESTO est pris en charge selon les conditions définies à l'article L.162-16-5-2 du code de la Sécurité sociale, c'est-à-dire dans l'indication de l'ATUc :
- Traitement chez l'adulte de l'insuffisance cardiaque avec dysfonction systolique ventriculaire gauche (fraction d'éjection ventriculaire gauche <= 40 %) symptomatique :
- de classe fonctionnelle NYHA II ayant présenté au moins 2 hospitalisations pour décompensation cardiaque dans l'année, documentée par une NT-proBNP >= 300 pg/ml (ou BNP >= 100 pg/ml) ou l'utilisation de diurétiques IV, ou de classe fonctionnelle NYHA III-IV,
- insuffisamment contrôlée par les thérapeutiques non médicamenteuses (chirurgie, resynchronisation cardiaque, etc.) ou médicamenteuses bien conduites : inhibiteurs de l'enzyme de conversion ou antagonistes du récepteur de l'angiotensine II, diurétiques et bêtabloquants.
Pour les patients insuffisants cardiaques non inclus dans l'indication de l'ATU : modalités de prise en charge
Certains patients insuffisant cardiaque sont concernés par l'indication de l'AMM mais ne font pas partie du périmètre de l'ATU, comme ceux ayant :
- une dysfonction systolique ventriculaire gauche (fraction d'éjection ventriculaire gauche inférieure ou égale à 40 %) symptomatique de classe fonctionnelle NYHA II ayant présenté moins de 2 hospitalisations pour décompensation cardiaque dans l'année documentée ou n'ayant pas utilisé de diurétiques IV ;
- une dysfonction systolique ventriculaire gauche symptomatique avec une fraction d'éjection ventriculaire gauche comprise entre 40 et 50 %.
- inhibiteurs de l'enzyme de conversion (IEC) : captopril, cilazapril, énalapril, fosinopril, lisinopril, périndopril, quinalapril, ramipril,
- antagonistes du récepteur de l'angiotensine II (ARA II), en cas d'intolérance aux IEC : candésartan, losartan, valsartan,
- diurétiques : bumétanide, furosémide, hydrochlorothiazde,
- bêtabloquants : bisoprolol, carvédilol, métoprolol, névibolol.
ENTRESTO en pratique
En initiation de traitement, la posologie d'ENTRESTO est de 1 comprimé de 49 mg/51 mg 2 fois par jour. Cette dose doit être doublée toutes les 2 à 4 semaines jusqu'à la dose cible de 97 mg/103 mg 2 fois par jour, en fonction de la tolérance du patient.
Chez les patients n'étant pas actuellement traités par un IEC ou un ARA II ou prenant ces médicaments à faible dose, la dose d'initiation d'ENTRESTO est plus faible, de 24 mg/26 mg 2 fois par jour. La posologie est ensuite doublée lentement, toutes les 3 à 4 semaines.
Une dose initiale de 24 mg/26 mg 2 fois par jour doit également être envisagée chez les patients ayant une PAS comprise entre 100 et 110 mmHg.
Les comprimés d'ENTRESTO doivent être administrés pendant ou en dehors des repas, avec un peu d'eau.
- Identification des populations particulières
- chez les patients ayant une kaliémie supérieure à 5,4 mmol/l ;
- chez les patients ayant une PAS (pression artérielle systolique) inférieure à 100 mm Hg.
- Ajustement de la dose en fonction du profil de tolérance
- si la PAS devient inférieure ou égale à 95 mm Hg,
- en cas d'hypotension symptomatique,
- en cas d'hyperkaliémie,
- en cas d'altération de la fonction rénale.
- Surveillance des patients : pression artérielle, rein, potassium
- la pression artérielle doit être contrôlée lors de l'initiation du traitement ou de l'adaptation de dose d'ENTRESTO, ou en routine au cours du traitement ;
- la fonction rénale des patients atteints d'insuffisance cardiaque doit toujours être évaluée. Les patients atteints d'insuffisance rénale légère et modérée ont plus de risque de développer une hypotension ;
- la kaliémie doit être surveillée avant et pendant le traitement. Le traitement ne doit pas être initié si la kaliémie est supérieure à 5,4 mmol/l. L'administration d'ENTRESTO peut être associée à un risque accru d'hyperkaliémie bien qu'une hypokaliémie puisse aussi survenir.
- Risque de survenue d'angioedème
ENTRESTO est contre-indiqué chez les patients ayant un antécédent d'angio-oedème lié à un traitement antérieur par IEC ou ARA II ou chez ceux ayant des angio-oedèmes héréditaires ou idiopathiques. Les patients noirs présentent un risque accru de développer cet effet secondaire.
La survenue d'un angio-oedème impose l'arrêt immédiat et définitif du traitement. Un traitement et une surveillance appropriés doivent être mis en place jusqu'à la disparition totale et durable des signes et symptômes.
- ENTRESTO et les autres médicaments
- les IEC ou les ARA II, en raison du risque accru d'angio-oedème. Compte tenu ce risque, un intervalle d'au moins 36 heures entre l'arrêt du traitement par IEC et l'initiation du traitement par ENTRESTO doit être respecté ;
- avec des produits contenant de l'aliskirène chez les patients atteints de diabète ou d'insuffisance rénale (DFGestimé < 60 ml/min/1,73 m²).
L'association d'ENTRESTO avec des inhibiteurs directs de la rénine tels que l'aliskirène n'est pas recommandée.
Identité administrative
- Liste I
- ENTRESTO 24 mg/26 mg, boîte de 28, CIP 3400930037904
- ENTRESTO 49 mg/51 mg, boîte de 56, CIP 3400930037911
- ENTRESTO 97 mg/103 mg, boîte de 56, CIP 3400930037928
- Prise en charge selon les conditions définies à l'article L.162-16-5-2 du code de la Sécurité sociale. Agréé aux collectivités et rétrocédable par prolongation des conditions d'inscription au titre de l'ATU de cohorte
- Demandes d'admission (remboursement et agrément aux collectivités) à l'étude.
- Laboratoire Novartis Pharma
Etude PARADIGM-HF
John J.V. McMurray and al. for the PARADIGM-HF Investigators and Committees Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure. N Engl J Med 2014 ; 371 : 993-1004
Pour aller plus loin
Code de la sécurité sociale - Article L162-16-5-2 (version en vigueur au 10 août 2014)
Annexe de l'avis n°2015.0095/SEM - Identification des alternatives pour un médicament post-ATU, pré-inscription article 48 ATUc (article L. 162-16-5-2 du code de la sécurité sociale) (HAS, novembre 2015)
Résumé EPAR à l'intention du public (EMA, 1er décembre 2015)
Plan de gestion des risque européen - résumé en anglais (EMA, 1er décembre 2015)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 8 minutes
8 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.