La posologie initiale de THALIDOMIDE CELGENE doit désormais être réduite à 100 mg/jour dans la prise en charge du myélome multiple non traité chez les patients de plus de 75 ans (illustration).
De nouvelles modalités posologiques sont recommandées chez les sujets de plus de 75 ans traités par thalidomide en association avec le melphalan et la prednisone, dans le cadre de la prise en charge du myélome multiple (voir VIDAL Reco "Myélome multiple") :
- la dose initiale de thalidomide recommandée est de 100 mg par jour ;
- la dose initiale de melphalan doit être réduite.
Dans le résumé des caractéristiques du produit (RCP) de THALIDOMIDE CELGENE, il n'était jusqu'alors pas préconisé d'ajustement spécifique de la posologie pour les personnes âgées, la dose recommandée étant de 200 mg par jour (voir monographie VIDAL de THALIDOMIDE CELGENE - Rubrique Posologie et Mode d'administration).
Des effets secondaires graves et de grade 5 plus fréquents chez les patients > 75 ans
Cette réduction de la dose initiale de thalidomide dans la population des plus de 75 ans est recommandée sur la base des résultats d'une étude de phase III (CC-5013-MM-020, N Engl J Med 2014), dont l'objectif était d'évaluer l'efficacité et la sécurité du lénalidomide plus dexaméthasone à faible dose versus l'association melphalan/prednisone/thalidomide (MPT).
Les données de tolérance de cette étude ont mis en évidence :
- une fréquence globale de survenue d'effets indésirables graves et d'effets indésirables de grade 5 plus élevée chez les patients de plus de 75 ans, comparativement aux patients plus jeunes (56,5 % versus 46,5 % et 10,3 % versus 5,3 % respectivement) ;
- des effets indésirables graves similaires dans les 2 groupes d'âge (<= 75 ans et > 75 ans), sans différence particulière dans les causes principales de décès entre les groupes d'âge.
En conclusion, la fréquence des effets indésirables graves a été plus élevée chez les patients de plus de 75 ans.
Le profil des effets indésirables rapportés chez les patients de plus de 75 ans, traités par thalidomide 100 mg une fois par jour, a été comparable à celui observé chez les patients de 75 ans et moins traités par thalidomide 200 mg une fois par jour.
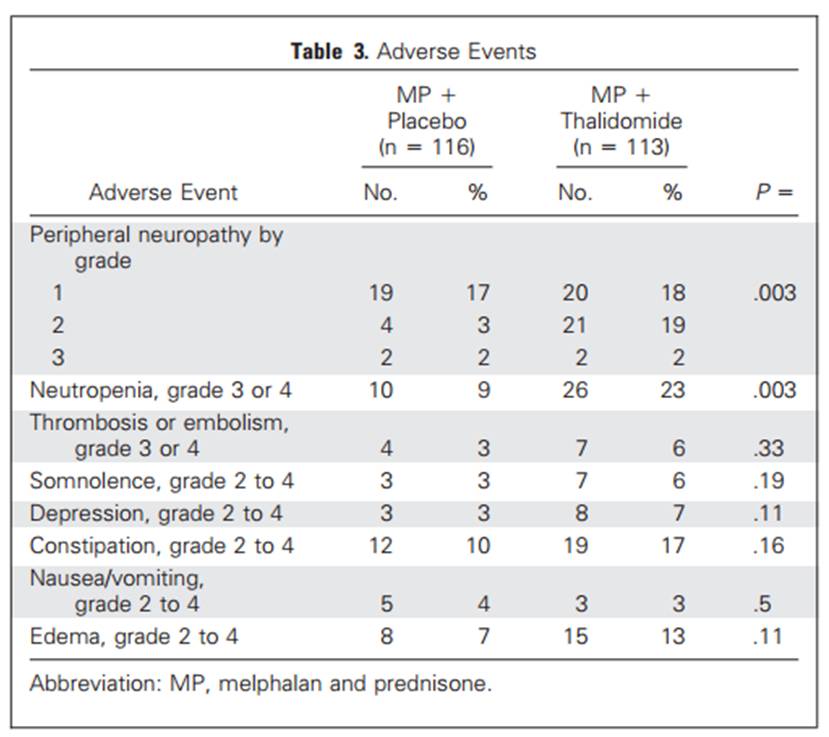
Ces conclusions ont été étayées par l'étude IFM 01/01 (J Clin Oncol 2009) ayant permis de comparer l'association melphalan-prednisone (MP) à l'association MP plus thalidomide (MPT) dans le traitement du myélome multiple chez des patients très âgés (> 75 ans) non préalablement traités (voir Figure 1).
Pour mémoire
THALIDOMIDE CELGENE 50 mg gélule est indiqué, en association au melphalan et à la prednisone, pour le traitement de première ligne des patients âgés de plus de 65 ans présentant un myélome multiple non traité ou présentant une contre-indication à la chimiothérapie à haute dose (Cf. Reco VIDAL Myélome multiple).
Pour aller plus loin
Communiqué : Thalidomide Celgene - Réduction de la dose initiale de thalidomide à 100 mg chez les patients âgés de plus de 75 ans (ANSM, 16 novembre 2015)
Lettre aux professionnels de santé (sur le site de l'ANSM, 16 novembre 2015)
Références
- Lotfi Benboubke and al. Lenalidomide and Dexamethasone in Transplant-Ineligible Patients with Myeloma. N Engl J Med 2014 ; 371 : 906-917
- Cyrille Hulin and al. Efficacy of Melphalan and Prednisone Plus Thalidomide in Patients Older Than 75 Years With Newly Diagnosed Multiple Myeloma : IFM 01/01 Trial. J Clin Oncol 2009 ; 27 : 3664-3670
Sur Vidal.fr
Thalidomide et risque de cancer secondaire hématologique : un risque accru à prendre en compte (15 avril 2013)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.