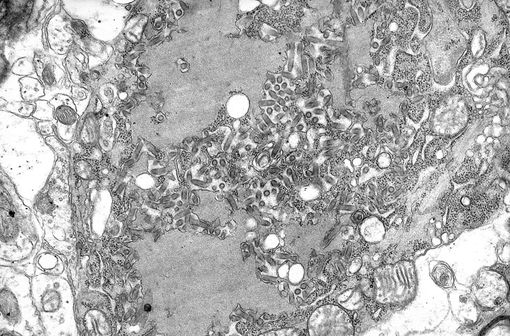
Virions de la rage (petits bâtonnets gris sombre) et corps de Negri (inclusions cellulaires plus larges pathognomoniques de la rage) en micrographie (illustration @Bibliothèque d'images de santé publique sur Wikimedia).
La laboratoire Sanofi a annoncé l'arrêt de commercialisation de l'immunoglobuline (Ig) humaine rabique IMOGAM RAGE, à la fin de l'année 2022.
IMOGAM RAGE est actuellement la seule spécialité à base d'Ig humaine rabique distribuée en France en prophylaxie postexposition à la rage.
Dans ce contexte, l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) autorise l'importation d'une spécialité identique à IMOGAM RAGE (même présentation et même concentration), dénommée BERIRAB et commercialisée en Allemagne, en Autriche et en Suisse. Cette spécialité sera mise à disposition des centres antirabiques fin 2022.
Ce dispositif d'importation constitue une solution temporaire, le temps de mettre en place une solution pérenne.
Le laboratoire Sanofi a annoncé l'arrêt de commercialisation prochain de la spécialité IMOGAM RAGE 150 UI/mL solution injectable (immunoglobuline humaine rabique - cf. Encadré ci-dessous) [1].
Selon le calendrier présenté par le laboratoire [2], l'arrêt de commercialisation d'IMOGAM RAGE devrait être effectif fin décembre 2022.
Des unités resteront disponibles sur le marché au plus tard jusqu'à la péremption du dernier lot disponible, en avril 2023.
| IMOGAM RAGE est utilisé en prophylaxie postexposition de l'infection par le virus de la rage consécutive à une griffure ou une morsure par un animal soupçonné d'être enragé, ou toute autre blessure, par exemple une contamination de la muqueuse par la salive de cet animal. L'immunoglobuline humaine rabique doit toujours être utilisée en association avec un vaccin rabique, selon les recommandations nationales et/ou de l'Organisation mondiale de la santé (OMS), à l'unique exception des patients déjà immunisés par un vaccin rabique et pouvant présenter des documents attestant la vaccination par un vaccin produit par culture cellulaire (c'est-à-dire une vaccination préexposition complète dans l'année précédente, une injection de rappel consécutive dans les cinq années précédentes ou une prophylaxie postexposition complète). Ces personnes peuvent recevoir le vaccin seul. L'administration doit impérativement être effectuée sous contrôle médical dans un centre antirabique spécialisé. |
Une décision stratégique du laboratoire
Cette décision n'est pas liée à des problèmes de sécurité ou de qualité de la spécialité IMOGAM RAGE.
Dans un courrier adressé aux centres antirabiques [2], le laboratoire explique que cette décision « a été prise en ligne avec la stratégie visant à recentrer son expertise et ses actifs sur son cœur de métier : le développement de vaccins pour la prévention des maladies infectieuses ».
Le laboratoire tient compte également des alternatives en immunoglobulines rabiques humaines proposées par d'autres laboratoires en Europe, aux États-Unis et au Canada.
Les alternatives à IMOGAM RAGE
IMOGAM RAGE est la seule spécialité à base d'immunoglobuline humaine rabique distribuée en France, utilisée pour neutraliser le virus de la rage chez des personnes exposées (prévention postexposition), en association avec un vaccin rabique.
Afin de couvrir les besoins d'immunoglobulines rabiques en France après la disparition d'IMOGAM RAGE, l'Agence de sécurité du médicament et des produits de santé (ANSM) a autorisé l'importation de la spécialité BERIBAB 150 UI/mL solution injectable, une autre immunoglobuline rabique humaine du laboratoire CSL Behring [3].
Ce médicament est actuellement commercialisé en Allemagne, en Autriche et en Suisse notamment.
IMOGAM RAGE versus BERIRAB : des spécialités équivalentes
BERIRAB 150 UI/mL solution injectable et IMOGAM RAGE 150 UI/mL sont des spécialités équivalentes :
- spécialités d'immunoglobuline humaine rabique à 150 UI/mL ;
- solution injectable en flacon de 2 mL.
Importation de BERIRAB dans les centres antirabiques : à partir de fin 2022
Des unités de la spécialité BERIRAB initialement destinées au marché suisse seront mises à disposition dans les centres antirabiques français recevant les patients susceptibles d'avoir été exposés au virus de la rage à partir de fin décembre 2022.
L'importation de BERIRAB sera maintenue jusqu'à ce qu'une solution pérenne soit mise en place.
[1] Arrêt de commercialisation - IMOGAM RAGE 150 UI/mL, solution injectable (ANSM, 24 mai 2022)
[2] Lettre d'information du laboratoire aux centres antirabiques et à la Direction de l'approvisionnement des produits de santé de l'Armée - IMOGAM RAGE (sur le site de l'ANSM, 23 mai 2022)
[3] Prévention de la rage : les centres antirabiques pourront utiliser BERIRAB à la place d'IMOGAM RAGE dès la fin 2022 (ANSM, 24 mai 2022)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.