Microphotographie montrant l'inflammation du gros intestin dans un contexte de maladie inflammatoire chronique de l’intestin (illustration @Nephron sur Wikimedia).
L'anticorps monoclonal à base d'adalimumab, HUMIRA 80 mg/0,8 mL solution injectable, est désormais disponible en boîte de 3 stylos préremplis.
Il s'ajoute à :
- la boîte de 1 stylo prérempli HUMIRA 80 mg/0,8 mL, commercialisée depuis 2018 (notre article du 14 juillet 2018) ;
- la boîte de 1 seringue préremplie HUMIRA 80 mg/0,8 mL, également commercialisée en 2018 (cf. Encadré 1).
Encadré 1 - Indications thérapeutiques d'HUMIRA 80 mg/0,8 mL en stylo ou seringue prérempli(e)
Polyarthrite rhumatoïde (PR), en association au méthotrexate (cf. VIDAL Reco "Polyarthrite rhumatoïde") :
- traitement de la polyarthrite rhumatoïde modérément à sévèrement active de l'adulte, lorsque la réponse aux traitements de fond, y compris le méthotrexate, est inadéquate ;
- traitement de la polyarthrite rhumatoïde sévère, active et évolutive chez les adultes non précédemment traités par le méthotrexate.
HUMIRA peut être donné en monothérapie en cas d'intolérance au méthotrexate ou lorsque la poursuite du traitement avec le méthotrexate est inadaptée.
Il a été montré qu'HUMIRA ralentit la progression des dommages structuraux articulaires mesurés par radiographie et améliore les capacités fonctionnelles lorsqu'il est administré en association au méthotrexate.
Psoriasis en plaques :
Hidrosadénite suppurée (HS) :
- traitement de l'hidrosadénite suppurée (maladie de Verneuil) active, modérée à sévère, chez les adultes et les adolescents à partir de 12 ans en cas de réponse insuffisante au traitement systémique conventionnel de l'HS.
Maladie de Crohn (MC) :
- traitement de la maladie de Crohn active modérée à sévère, chez les patients adultes qui n'ont pas répondu malgré un traitement approprié et bien conduit par un corticoïde et/ou un immunosuppresseur ou chez lesquels ce traitement est contre-indiqué ou mal toléré ;
- traitement de la maladie de Crohn active modérée à sévère, chez les enfants et les adolescents à partir de 6 ans, qui n'ont pas répondu à un traitement conventionnel comprenant un traitement nutritionnel de première intention et un corticoïde et/ou un immunomodulateur, ou chez lesquels ces traitements sont mal tolérés ou contre-indiqués.
Rectocolite hémorragique (RCH) :
- traitement de la rectocolite hémorragique active, modérée à sévère chez les patients adultes ayant eu une réponse inadéquate au traitement conventionnel, comprenant les corticoïdes et la 6-mercaptopurine (6-MP) ou l'azathioprine (AZA), ou chez lesquels ce traitement est contre-indiqué ou mal toléré.
Uvéite :
- traitement de l'uvéite non infectieuse, intermédiaire, postérieure et de la panuvéite chez les patients adultes ayant eu une réponse insuffisante à la corticothérapie, chez les patients nécessitant une épargne cortisonique, ou chez lesquels la corticothérapie est inappropriée ;
- traitement de l'uvéite antérieure chronique non infectieuse chez les enfants et les adolescents à partir de 2 ans en cas de réponse insuffisante ou d'intolérance au traitement conventionnel ou pour lesquels un traitement conventionnel est inapproprié.
|
Cette nouvelle présentation de 3 stylos préremplis de solution injectable HUMIRA 80 mg/0,8 mL est particulièrement adaptée à la posologie d'induction dans le traitement des maladies inflammatoires chroniques de l'intestin (MICI), que sont la maladie de Crohn (cf. VIDAL Reco "Maladie de Crohn") et la rectocolite hémorragique (cf. VIDAL Reco "Rectocolite hémorragique").
En effet, pour l'instauration du traitement par adalimumab dans ces indications, le schéma posologique (cf. Encadré 2) nécessite 3 injections sous-cutanées (SC) de 80 mg (soit 3 stylos préremplis à 80 mg) :
- 1 dose de 160 mg (2 injections de 80 mg) à la semaine 0 ;
- puis 1 dose de 80 mg (1 injection) à la semaine 2.
Encadré 2 - Schéma posologique du traitement par adalimumab dans la maladie de Crohn et la rectocolite hémorragique
- Traitement d'induction :
- 160 mg à la semaine 0, administrés sous forme de :
- 2 injections SC de 80 mg sur un jour,
- ou de 1 injection SC de 80 mg par jour pendant deux jours consécutifs,
- ou de 2 injections SC de 40 mg par jour pendant deux jours consécutifs),
- ou de 4 injections SC de 40 mg sur un jour ;
- 80 mg à la semaine 2.
- Traitement d'entretien :
- 1 dose de 40 mg administrée toutes les 2 semaines, en injection SC (sous-cutanée).
Certains patients chez qui une diminution de la réponse au traitement par HUMIRA 40 mg toutes les 2 semaines est observée peuvent bénéficier d'une augmentation de la posologie à 40 mg toutes les semaines ou 80 mg toutes les 2 semaines. |
Le stylo prérempli HUMIRA 80 mg/0,8 mL permet d'injecter 80 mg d'adalimumab.
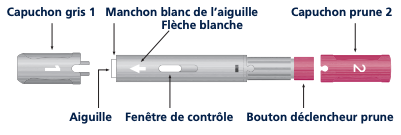
Il est protégé par 2 capuchons, à chaque extrémité :
- un capuchon gris pour protéger le système injecteur (côté aiguille),
- un capuchon prune pour protéger le bouton déclencheur (cf. Figure 1).
Figure 1 - Représentation schématique du stylo prérempli
Une fenêtre de contrôle permet de vérifier l'aspect de la solution.
Une flèche blanche est dessinée sur le stylo ; elle pointe vers le site d'injection.
Le stylo doit reposer à température ambiante pendant 15 à 30 minutes avant l'injection.
Les deux capuchons doivent être retirés juste avant l'injection.
L'injection sous-cutanée a lieu sur le devant des cuisses ou dans le ventre.
Le stylo doit être positionné au niveau du site d'injection selon un angle de 90 °.
L'injection est déclenchée en appuyant sur le bouton déclencheur. Un clic signale de début de l'injection.
L'injection est terminée lorsque l'indicateur jaune (dans la fenêtre de contrôle) arrête de bouger.
Identité administrative
- Liste I
- Prescription initiale hospitalière
- Prescription initiale et renouvellement réservés aux spécialistes en rhumatologie, en pédiatrie, en médecine interne, en gastroentérologie et hépatologie, en dermatologie ou en ophtalmologie
- Boîte de 3 stylos préremplis, CIP 3400930178805, UCD 3400894362654, prix public TTC = 1 877,29 euros
- Remboursable à 65 %, sur ordonnance de médicaments d'exception (cf. Encadré 3) (Fiche d'information thérapeutique publiée au Journal officiel du 17 avril 2020 - texte 20)
- Non agréé aux collectivités
- Inscrit sur la liste des spécialités prises en charge en sus des GHS (cf. Encadré 4)
- Laboratoire Abbvie
Encadré 3 - Périmètre de prise en charge de HUMIRA 80 mg/0,8 mL (seringue préremplie et stylo prérempli)
- dans les indications de l'AMM : dans la rectocolite hémorragique, la maladie de Crohn chez l'adulte et l'uvéite chez l'adulte ;
- dans le traitement du psoriasis en plaques chronique sévère de l'adulte, défini par :
- un échec (réponse insuffisante, contre-indication ou intolérance) à au moins deux traitements parmi les traitements systémiques non biologiques et la photothérapie,
- et une forme étendue et/ou un retentissement psychosocial important ;
- dans le traitement de la maladie de Crohn active, sévère, chez les enfants et les adolescents à partir de 6 ans, qui n'ont pas répondu à un traitement conventionnel comprenant un corticoïde, un immunomodulateur et un traitement nutritionnel de première intention, ou chez lesquels ces traitements sont mal tolérés ou contre-indiqués ;
- en association au méthotrexate, traitement de l'uvéite antérieure chronique non infectieuse associée à une arthrite juvénile idiopathique chez l'enfant à partir de 2 ans et l'adolescent, en cas de réponse insuffisante ou d'intolérance au traitement conventionnel ou pour lesquels un traitement conventionnel est inapproprié ;
- en association au méthotrexate dans le traitement de la polyarthrite rhumatoïde modérément à sévèrement active de l'adulte lorsque la réponse aux traitements de fond, y compris le méthotrexate, est inadéquate. HUMIRA peut être donné en monothérapie en cas d'intolérance au méthotrexate ou lorsque la poursuite du traitement avec le méthotrexate est inadaptée.
- Non remboursable dans l'indication « hidrosadénite suppurée de l'adulte et de l'adolescent à partir de 12 ans ».
|
Encadré 4 - Périmètre de prise en charge en sus des GHS - HUMIRA 80 mg/0,8 mL
- dans les indications de l'AMM : dans la rectocolite hémorragique et la maladie de Crohn chez l'adulte ;
- dans le traitement du psoriasis en plaques de l'adulte, chez les patients ayant un psoriasis en plaques chronique sévère, défini par :
- un échec (réponse insuffisante, contre-indication ou intolérance) à au moins deux traitements parmi les traitements systémiques non biologiques et la photothérapie,
- et une forme étendue et/ou un retentissement psychosocial important ;
- dans le traitement de la maladie de Crohn active, sévère, chez les enfants et les adolescents à partir de 6 ans qui n'ont pas répondu à un traitement conventionnel comprenant un corticoïde, un immunomodulateur et un traitement nutritionnel de première intention, ou chez lesquels ces traitements sont mal tolérés ou contre-indiqués.
|
Avis de la Commission de la Transparence - HUMIRA 80 mg (HAS, 20 novembre 2019)


 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.