La polyarthrite rhumatoïde est une maladie auto-immune caractérisée par la fabrication d'auto-anticorps dirigés contre la membrane synoviale des articulations (illustration).
Depuis début juillet 2019, l'inhibiteur d'interleukine-6 ROACTEMRA solution injectable est disponible en stylo auto-injecteur, en complément de la seringue préremplie.
Comme la seringue préremplie, ROACTEMRA solution injectable en stylo prérempli permet de délivrer 162 mg de tocilizumab (0,9 mL de solution).
Les indications thérapeutiques de ROACTEMRA en stylo prérempli sont :
- la polyarthrite rhumatoïde (Cf. VIDAL Reco "Polyarthrite rhumatoïde"), en association au méthotrexate (MTX) :
- traitement de la polyarthrite rhumatoïde (PR) active, sévère et évolutive chez les patients adultes non précédemment traités par MTX,
- traitement de la PR active, modérée à sévère, chez les patients adultes qui ont présenté soit une réponse inadéquate, soit une intolérance à un précédent traitement par un ou plusieurs traitements de fond (DMARDs) ou par un ou plusieurs antagonistes du facteur de nécrose tumorale (anti-TNF).
Il a été montré que ROACTEMRA, en association avec le méthotrexate, réduit le taux de progression des dommages structuraux articulaires mesurés par radiographie et améliore les capacités fonctionnelles.
- l'artérite à cellules géantes :
- traitement des patients adultes atteints d'artérite à cellules géantes (ACG).
A noter que la présentation ROACTEMRA en stylo prérempli n'est pas indiquée dans le traitement de l'arthrite juvénile idiopathique (Cf. VIDAL Reco Arthrite juvénile idiopathique) car elle n'a pas d'AMM (autorisation de mise sur le marché) chez l'enfant, contrairement à la présentation en seringue préremplie.
Cette dernière a en effet obtenu une extension de prise en charge dans le traitement de l'arthrite juvénile idiopathique le 4 juillet 2019 (Cf. monographie VIDAL de ROACTEMRA 162 mg solution injectable en seringue préremplie - Rubriques Indications et Prescription/Délivrance/Prise en charge).
ROACTEMRA stylo prérempli : en pratique
Le traitement par ROACTEMRA doit être instauré par des professionnels de santé expérimentés dans le diagnostic et le traitement de la PR et/ou de l'ACG.
Une carte de surveillance du patient devra être remise à tous les patients traités par ROACTEMRA.
La posologie recommandée de ROACTEMRA est de 162 mg une fois par semaine, administrée par voie sous-cutanée (Cf. Tableau I).
Une carte de surveillance du patient devra être remise à tous les patients traités par ROACTEMRA.
La posologie recommandée de ROACTEMRA est de 162 mg une fois par semaine, administrée par voie sous-cutanée (Cf. Tableau I).
Tableau I - Schéma posologique de ROACTEMRA
| Polyarthrite rhumatoïde | Artérite à cellules géantes |
| 162 mg 1 fois par semaine | 162 mg 1 fois par semaine, en association à une corticothérapie dégressive ROACTEMRA peut être utilisé seul après l'arrêt des corticoïdes. Il ne doit pas être utilisé en monothérapie pour traiter une rechute aiguë |
- une augmentation des enzymes hépatiques (ALAT, ASAT),
- une diminution du nombre de neutrophiles,
- une diminution du nombre de plaquettes.
Avant utilisation, ROACTEMRA doit être conservé au réfrigérateur, entre 2 et 8 °C. Une fois sorti du réfrigérateur, il doit être administré dans les 8 heures et doit être conservé à une température ne dépassant pas 30 °C.
Il ne doit pas être agité avant utilisation.
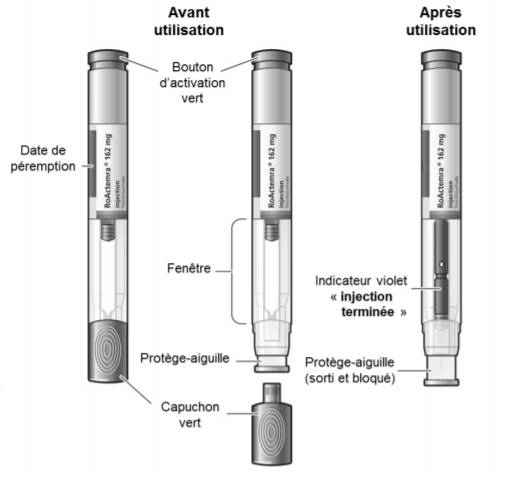
Le stylo présente (Cf. Figure 1) :
- un bouton d'activation vert : ce bouton est verrouillé. Il doit être déverrouillé en appuyant fermement le stylo contre la peau (avec un angle de 90 °). Après cette étape, l'injection peut être déclenchée en appuyant sur le bouton d'activation,
- une fenêtre de visualisation de la solution injectable. Après l'injection, un indicateur violet apparaît dans cette fenêtre et confirme que l'injection est terminée,
- un capuchon vert recouvrant le protège-aiguille. Après l'injection, le protège-aiguille est sorti et bloqué.
Figure 1 - Composants du stylo prérempli RoACTEMRA
Conseils aux patients en cas d'auto-injection
Le médecin devra évaluer l'aptitude du patient à être traité par voie sous-cutanée à domicile et l'informer de la nécessité de prévenir un professionnel de santé s'il présente des symptômes d'une réaction allergique. Les patients doivent consulter immédiatement un médecin s'ils présentent des symptômes de réactions allergiques graves.
Après une formation appropriée à la technique d'injection sous-cutanée, le patient considéré apte à l'auto-injection par le médecin peut s'administrer ROACTEMRA à l'aide du stylo prérempli.
Le patient doit être informé que :
Le médecin devra évaluer l'aptitude du patient à être traité par voie sous-cutanée à domicile et l'informer de la nécessité de prévenir un professionnel de santé s'il présente des symptômes d'une réaction allergique. Les patients doivent consulter immédiatement un médecin s'ils présentent des symptômes de réactions allergiques graves.
Après une formation appropriée à la technique d'injection sous-cutanée, le patient considéré apte à l'auto-injection par le médecin peut s'administrer ROACTEMRA à l'aide du stylo prérempli.
Le patient doit être informé que :
- le stylo prérempli ne doit pas être agité ;
- la totalité du contenu du stylo doit être injectée ;
- les sites d'injection recommandés doivent être alternés (abdomen, cuisse et partie supérieure du bras) ;
- les injections ne doivent jamais être réalisées dans des grains de beauté, des cicatrices ou des zones où la peau est sensible, contusionnée, rouge, dure, ou non intacte.
Le patient doit également être prévenu, qu'en cas d'oubli d'une injection sous-cutanée hebdomadaire de ROACTEMRA, il doit reprendre l'injection à la prochaine date préalablement programmée, afin de respecter un intervalle minimum de 7 jours entre 2 injections.
Tocilizumab et risque hépatique : rappel des modalités de surveillance
Le tocilizumab est associé à un risque hépatique grave. Ce risque a fait l'objet d'une mise en garde début juillet 2019 (notre article du 11 juillet).
Avant d'instaurer le traitement, un bilan hépatique doit être réalisé.
Chez les patients traités par tocilizumab, une surveillance hépatique étroite est nécessaire :
- contrôle des taux d'ALAT (alanine aminotransférase) et d'ASAT (aspartate aminotransférase) toutes les 4 à 8 semaines pendant les 6 premiers mois de traitement, puis toutes les 12 semaines par la suite. Selon les résultats, une adaptation posologique ou une interruption du traitement doivent être envisagées ;
- information des patients pour identifier des signes et symptômes d'atteinte hépatique.
Identité administrative
- Liste I
- Prescription initiale hospitalière annuelle, réservée aux spécialistes en rhumatologie ou en médecine interne
- Surveillance particulière pendant le traitement
- Boîte de 4 stylos préremplis ACTPen, CIP 3400930145524
- Remboursable à 65 % sur prescription médicale en conformité avec la fiche d'information thérapeutique (FIT publiée au Journal officiel du 4 juillet 2019 - texte 12)
- Prix public TTC = 897,62 euros
- Agrément aux collectivités (Journal officiel du 4 juillet 2019 - texte 13)
- Prise en charge en sus des GHS, uniquement dans le traitement de la polyarthrite rhumatoïde (PR) active, modérée à sévère en deuxième ligne de traitement ou plus
- Laboratoires Roche / Chugaï Pharma France
Encadré - Périmètre de prise en charge de ROACTEMRA en stylo prérempli
Traitement de la polyarthrite rhumatoïde en deuxième ligne de traitement
NB. Le traitement de la polyarthrite rhumatoïde active, sévère et évolutive chez les patients adultes non précédemment traités par MTX, en association au MTX n'est pas pris en charge. Traitement de l'artérite à cellules géantes
|
Pour aller plus loin
Avis de la Commission de la Transparence - ROACTEMRA en stylo prérempli (HAS, 19 septembre 2019)
Sur VIDAL.fr
ROACTEMRA (tocilizumab) : mise en garde contre le risque de toxicité hépatique grave (11 juillet 2019)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.