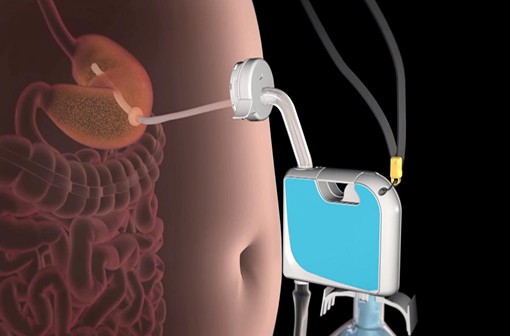
La pompe AspireAssist élimine 30 % des aliments ingérés à chaque repas.
Un dispositif permettant un pompage d'une partie du contenu de l'estomac après un repas
Le dispositif AspireAssist se compose d'une sonde implantée sous endoscopie dans la partie haute de la cavité de l'estomac. Cette sonde est abouchée à la peau du ventre par une valve, le "SkinPort", de la taille d'un jeton.
Une fois la stomie (déviation chirurgicale d'un conduit naturel) cicatrisée et la valve mise en place, le patient peut y connecter une pompe manuelle avec laquelle, 20 à 30 minutes après le repas, il aspire la partie supérieure du bol alimentaire, qui sera ensuite éliminée dans les toilettes. Une poche contenant de l'eau est reliée à la pompe et permet de diluer le bol avant de commencer le pompage.
Une fois le patient accoutumé à la procédure, celle-ci prend 10 à 15 minutes. Elle doit être renouvelée après chaque repas, en tout cas au moins deux fois par jour :
Etude sur 171 patients : un effet rapide et durable sur le poids par rapport aux patients non équipés
Si les résultats de l'étude clinique ayant mené à l'autorisation de mise sur le marché n'ont pas encore été publiés, certaines données ont été citées dans le communiqué de presse de la FDA.
Cette étude a porté sur 171 patients obèses, 111 ayant été équipés d'AspireAssist et l'ensemble des participants ayant bénéficié d'un suivi éducatif sur la nutrition et l'activité physique (donc un groupe contrôle de 60 patients).
Au bout d'une année, les patients équipés de la pompe avaient perdu 12,1 % de leur poids (environ 20 kg en moyenne) contre 3,6 % dans le groupe contrôle.
Dans les deux groupes, une amélioration modeste a été observée concernant les comorbidités fréquemment associées à l'obésité sévère à morbide (diabète de type 2, hypertension artérielle) ainsi qu'en terme de qualité de vie.
A noter qu'une étude pilote, effectuée sur un nombre restreint de patients (11 équipés de la pompe, 7 témoins) et publiée en 2013, a montré une réduction moyenne du poids d'environ 18 % à 1 an, réduction maintenue à 2 ans (20 % environ) dans le groupe "AspirAssist".
Des indications restreintes pour éviter les accidents et le mésusage
La FDA a autorisé la commercialisation d'AspireAssist dans le traitement de l'obésité sévère à morbide (IMC compris entre 35 et 55 kg/m2) chez les personnes de plus de 22 ans pour lesquelles un échec des traitements non chirurgicaux a été observé, en association systématique avec un programme éducatif destiné à améliorer l'équilibre alimentaire, réduire les apports caloriques et favoriser l'activité physique adaptée régulière.
Un suivi médical rapproché et des précautions du fabricant pour adapter le dispositif et en surveiller l'usage
L'usage d'AspireAssist, s'il semble pouvoir être continué pendant plusieurs années, exige un suivi médical rapproché. Par exemple, au fur et à mesure que le patient perd du poids, la longueur du tube relié à l'estomac doit être raccourcie pour que la valve soit toujours adhérente à la peau du ventre.
Pour s'assurer que les patients équipés de cette pompe ne soient pas perdus de vue, le connecteur entre la pompe externe et la valve est conçu pour cesser de fonctionner après 115 connexions (soit 5 à 6 semaines de traitement), afin de s'assurer que les patients respectent les consignes relatives au suivi médical rapproché.
De plus, pour limiter le mésusage, le dispositif est conçu pour que les patients ne puissent pas pomper plus de 30 % de leur bol alimentaire.
Des effets indésirables parfois gênants, dont des fistules
L'usage de la pompe AspireAssist a provoqué des effets indésirables le plus souvent sans gravité.
La pose du tube intragastrique a occasionné des douleurs abdominales transitoires, des infections de la peau, voire une migration de l'extrémité du tube dans la paroi stomacale.
Au long cours, les effets indésirables les plus fréquents de cette pompe ont été des nausées, des vomissements, de la constipation ou des diarrhées.
L'effet indésirable le plus grave a été l'apparition de fistule persistante lors du retrait du dispositif, chez les patients qui ont choisi de le faire retirer une fois leur objectif pondéral atteint.
Des contre-indications nombreuses à la pose d'AspireAssist
La FDA précise que cette pompe est contre-indiquée chez les patients qui souffrent :
- de troubles du comportement alimentaire (boulimie, hyperphagie, somnambulisme alimentaire, par exemple) ;
- d'hypertension artérielle non contrôlée par les traitements ;
- de maladies cardiovasculaires ou pulmonaires ;
- de troubles de la coagulation sanguine ;
- d'ulcères digestifs ou de maladies inflammatoires chroniques de l'intestin (MICI) ;
- de douleurs abdominales chroniques.
Pas d'augmentation du nombre de calories ingérées par repas, selon les analyses effectuées lors des études pilotes
Une des craintes des autorités réglementaires était la possibilité que cette pompe gastrique entraîne une augmentation des apports alimentaires, en compensation du déficit calorique. L'étude présentée à la FDA montre que les personnes équipées d'AspireAssist n'ont augmenté ni le volume, ni la valeur calorique des aliments ingérés.
De plus, pour faciliter la vidange, le patient doit avoir mastiqué longuement ses aliments, allongeant ainsi la durée moyenne du repas, ce qui, selon les patients, a réduit la quantité d'aliments ingérés en laissant le temps à la satiété d'être perçue.
Au-delà du dispositif, dont le principe même peut être l'objet de critiques et d'un défaut d'acceptabilité, l'autorisation de la FDA et l'étude qui la sous-tend confirment un élément important dans le traitement de l'obésité sévère. Pour reprendre les mots des auteurs de l'étude pilote d'AspireAssist publiée en 2013 : « La quantité d'aliments ingérés à chaque repas ne semble pas reposer que un signal physiologique qui agirait pour parvenir à l'ingestion d'un nombre de calories minimum nécessaire, mais aussi sur des facteurs psychosociaux et sur la gratification apportée par l'odorat, le goût et la mastication ».
[édit 1/7] Une influence sur le microbiote intestinal, qui favoriserait moins l'absorption des calories, et donc la prise de poids ?
Comme le suggère Ysengrain en commentaire, il est possible aussi que cette vidange gastrique et ses conséquences modifient l'influence du microbiote intestinal (voir notre article) sur la capacité intestinale d'absorption des calories : chez les personnes obèses, la composition de ce microbiote apparaît modifiée, avec un rapport entre le nombre de bactéries Firmicutes et le nombre de bactéries Bacteroidetes en augmentation (forte baisse des bacteroidetes) en comparaison du rapport constaté chez les sujets minces. Cette modification entraîne l'absorption supplémentaire de calories pour un repas, par rapport à un sujet mince.
La vidange gastrique, en diminuant les apports, modifierait la composition de ce microbiote, qui favoriserait alors moins l'obésité (sorte de cercle vertueux).
A l'appui de ce cette hypothèse (non démontrée avec ce dispositif de vidange gastrique), une petite étude récente (Biomed Res Int., février 2015) a montré que chez 5 patients ayant subi une chirurgie bariatrique (réduction de l'estomac, voir notre article sur ses caractéristiques et son impact, ainsi que la place de cette chirurgie dans la prise en charge de l'obésité), la composition du microbiote change (modification du rapport Firmicutes/Bacteroidetes avec augmentation des Bacteroidetes). En conséquence, la capacité d'absorption des calories diminue en dehors des repas, et augmente pendant ces derniers, selon l'analyse des auteurs.
A l'inverse, les auteurs ont constaté que chez les 5 patients qui n'ont pas subi cette chirurgie mais un régime très strict, le microbiote ne s'améliore pas, reste un "microbiote d'obèse".
Cela signifierait donc que la réduction mécanique des apports pourrait permettre des pertes de poids plus durables, les personnes obèses traitées ainsi retrouvant un microbiote de personne mince.
Tout ceci demande bien sûr confirmation à plus grande échelle, l'étude du microbiote n'en étant encore qu'à ses balbutiements, certes très prometteurs [/édit].
En conclusion : une alternative moins invasive à la chirurgie bariatrique ?
Ce dispositif n'est pas en vente en France, mais l'est déjà dans de nombreux pays hors des Etats-Unis, ce qui laisse envisager une possible arrivée en France. Ce dispositif, malgré son étrangeté et ses risques, aura-t-il sa place dans la prise en charge thérapeutique des patients atteints d'obésité sévère ou morbide et chez qui les mesures de restriction calorique, soutien psychologique ont échoué ?
En tout cas, il est à noter que sa pose paraît bien moins invasive que la chirurgie bariatrique, qui vise à réduire la taille de l'estomac pour accélérer la sensation de satiété et diminuer les apports. La question de l'acceptabilité par les personnes concernées sera bien entendue essentielle, de même que le suivi et la lutte contre le mésusage.
Pour aller plus loin
Le communiqué de presse de la FDA à propos d'AspireAssist (en anglais)
« FDA approves AspireAssist obesity device », 14 juin 2016
L'étude pilote d'AspireAssist publiée en 2013 (en anglais)
Shelby Sullivan et al. « Aspiration Therapy Leads to Weight Loss in Obese Subjects: A Pilot Study. » Gastroenterology. 2013 Dec; 145(6): 1245–52.
Le site consacré à AspireAssist par le fabricant, Aspire Bariatrics (en français)
L'étude comparant le microbiote de personnes obèses opérées de l'estomac à celui de personnes suivant un régime strict
Antje Damms-Machado et coll., « Effects of Surgical and Dietary Weight Loss Therapy for Obesity on Gut Microbiota Composition and Nutrient Absorption », Biomed Res Int. 2015; 2015: 806248. Published online 2015 Feb 1
Sur VIDAL.fr :
VIDAL Reco "Obésité"
Chirurgie bariatrique et obésité (étude) : le risque de décès diminuerait de moitié dans les années suivant l'intervention (janvier 2015)
Obésité : la chirurgie bariatrique diminuerait le risque de survenue d'un diabète de type 2 (novembre 2014)
MetaGenoPolis, une initiative pour mieux comprendre les milliards de bactéries du microbiote intestinal (août 2013)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.