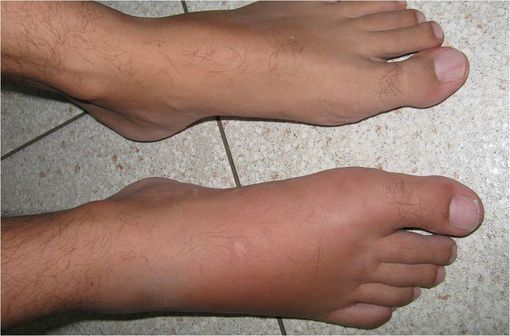
Érysipèle du pied droit (illustration @Grook Da Oger, sur Wikimedia).
La France dispose à nouveau d'une spécialité de benzathine benzylpénicilline
BENZATHINE BENZYLPENICILLINE SANDOZ poudre et solvant pour suspension injectable intramusculaire (IM) est un nouveau médicament de benzathine benzylpénicilline commercialisé en France.
Cette pénicilline retard est indiquée chez les adultes, adolescents, enfants et nouveau-nés dans le traitement et la prophylaxie des infections suivantes dues à des bactéries sensibles à la pénicilline :
- Dans le traitement des pathologies suivantes :
- érysipèle
- syphilis précoce (primaire et secondaire)
- syphilis tardive (à l'exception de la neurosyphilis et d'anomalies du LCR)
- pian et pinta, des tréponématoses endémiques non vénériennes, rares en France.
- Dans la prophylaxie :
- du rhumatisme articulaire aigu (chorée, cardiopathie rhumatismale)
- de la glomérulonéphrite post-streptococcique
- de l'érysipèle.
BENZATHINE BENZYLPENICILLINE SANDOZ est disponible en 2 dosages, à 1,2 MUI et 2,4 MUI.
Le dosage à 0,6 MUI n'est pas commercialisé à ce jour, pour des raisons industrielles.
L'EXTENCILINE était en rupture de stock depuis 2014
La benzathine benzylpénicilline est le traitement de référence de la syphilis et pour la prévention du rhumatisme articulaire aigu.
Jusqu'en 2014, la seule spécialité de benzathine benzylpénicilline commercialisée en France était EXTENCILLINE.
Les spécialités de BENZATHINE PENICILLINE SANDOZ prennent le relais de SIGMACILLINA 1,2 MUI/2,5 mL suspension injectable IM, spécialité importée d'Italie depuis février 2014, suite à l'arrêt de commercialisation d'EXTENCILLINE (notre article du 12 février 2014). SIGMACILLINA sera encore disponible dans les pharmacies hospitalières jusqu'à épuisement des stocks.
Les spécialités BENZATHINE BENZYLPENICILLINE SANDOZ présentent une composition en principe actif identique à celle d'EXTENCILLINE.
Leur composition en excipient à effet notoire diffère notamment par la présence de phospholipides de soja dans la spécialité Sandoz, exposant au risque de survenue de réaction d'hypersensibilité (choc anaphylactique, urticaire).
BENZATHINE BENZYLPENICILLINE SANDOZ n'a pas le statut de générique de l'EXTENCILLINE.
Posologies et volumes d'injection recommandés
Les doses recommandées de benzathine benzylpénicilline dépendent :
- de l'indication : la posologie tient compte de la sévérité et du type d'infection (Cf. monographie VIDAL - Posologie et Mode d'administration),
- de l'âge et de la fonction hépatique et rénale du patient : un ajustement posologique est nécessaire chez les sujets insuffisants rénaux et insuffisants hépatiques.
Le traitement peut être administré :
- en dose unique : syphilis primaire et secondaire, pian, pinta ;
- pendant plusieurs semaines : syphilis stade tardif ;
- pendant plusieurs années : prophylaxie du rhumatisme articulaire aigu, de la glomérulonéphrite post-streptococcique et de l'érysipèle.
BENZATHINE BENZYLPENICILLINE SANDOZ étant une pénicilline retard, un volume total de 5 mL par site d'injection est considéré comme la limite tolérée.
Par conséquent, il ne faut pas administrer plus de 5 mL de la suspension prête à être injectée en un site unique quel que soit le moment.
L'injection doit être effectuée le plus lentement possible et seulement en exerçant une faible pression.
Il faut éviter de frotter après l'injection.
Les différents sites d'injection en IM profonde stricte selon l'âge des patients
BENZATHINE BENZYLPENICILLINE SANDOZ doit être administré strictement en injection intramusculaire profonde :
- dans le quadrant supéro-externe du muscle grand fessier
- ou dans la zone ventro-glutéale de Hochstetter avec l'aiguille orientée vers la crête iliaque ou selon la méthode de von Hochstetter.
Chez les enfants, le site d'injection recommandé est le muscle quadriceps fémoral (quadriceps femoris). L'injection dans le muscle deltoïde n'est appropriée que si la masse musculaire est adéquate ; dans ce cas, il convient de faire attention au nerf radial.
Chez les nourrissons et les jeunes enfants, la zone périphérique du quadrant supéro-externe de la région fessière ne doit être utilisée comme zone d'injection que dans des cas exceptionnels (par exemple brûlures étendues) afin d'éviter des lésions du nerf sciatique.
L'aiguille doit être aussi verticale que possible par rapport à la surface de la peau.
L'injection doit être réalisée aussi loin que possible des principaux vaisseaux.
Dans tous les cas, une aspiration doit être effectuée avant l'injection. Si une aspiration de sang ou une douleur surviennent pendant l'injection, celle-ci doit être arrêtée.
En cas de traitement à long terme, par exemple dans le traitement de la syphilis, il est recommandé d'administrer chaque injection à bonne distance de l'injection précédente.
Prévenir et surveiller les réactions allergiques notamment
Selon le résumé des caractéristiques du produit (Cf. Monographie VIDAL - Mises en garde et précautions d'emploi) :
- un test d'hypersensibilité devrait être pratiqué si possible avant le traitement,
- une surveillance médicale serait conseillée pendant au moins une demi-heure après l'injection, en raison de possibles réactions allergiques immédiates graves même après la première administration.
Le traitement doit être arrêté immédiatement :
- dès l'apparition d'une réaction allergique ;
- en cas de diarrhée sévère et persistante évoquant une colite pseudomembraneuse.
Identité administrative
- Liste I
- BENZATHINE BENZYLPENICILLINE SANDOZ 1,2 MUI, boîte de 1 flacon + 1 ampoule de solvant de 5 mL, CIP 3400930002841
- BENZATHINE BENZYLPENICILLINE SANDOZ 2,4 MUI, boîte de 1 flacon + 1 ampoule de solvant de 5 mL, CIP 3400930002858
- Prix public TTC = 11,14 euros (pour les 2 dosages)
- Remboursable à 65 % (Journal officiel du 1er avril 2016, texte 28)
- Agrément aux collectivités (Journal officiel du 1er avril 2016, texte 29)
- Laboratoire Sandoz
Pour aller plus loin
Se reporter à la monographie VIDAL de BENZATHINE BENZYLPENICILLINE SANDOZ
Traitement de la syphilis et prévention du rhumatisme articulaire aigu : Mise à disposition de spécialités à base de benzathine benzylpénicilline en France - Point d'information (ANSM, 1er avril 2016)
EXTENCILLINE 600 000 UI, 1,2 M U.I. et 2,4 M U.I., poudre et solvant pour suspension injectable (IM) - Arrêt de commercialisation (ANSM, 1er avril 2016)
Avis de la Commission de la Transparence (HAS, 21 janvier 2015)
Sur VIDAL.fr
EXTENCILLINE : arrêt de commercialisation et mise à disposition d'une spécialité importée (12 février 2014)
EXTENCILLINE 0,6 MUI et 1,2 MUI poudres et solvants pour suspension injectable : rupture de stock attendue fin septembre (16 Septembre 2013)
Pour aller plus loin
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.