Pseudomonas aeruginosa en microscopie optique à balayage (illustration @CDC/ Janice Haney Carr, sur Wikimedia).
TADIM, nouvelle spécialité de colistiméthate sodique, prodrogue de la colistine
TADIM poudre pour solution à 1 MUI pour inhalation par nébuliseur est une nouvelle spécialité de colistiméthate sodique, une prodrogue de la colistine (famille des polymyxines), indiqué chez l'adulte et l'enfant dans la prise en charge des infections pulmonaires chroniques dues à Pseudomonas aeruginosa chez les patients atteints de mucoviscidose.
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens.
Ce médicament est présenté en flacon de poudre à reconstituer. Un flacon contient 1 MUI de colistiméthate sodique correspondant à environ 80 mg.
Le colistiméthate est une prodrogue de la colistine (famille des polymyxines).
Différents types de système d'inhalation validés par l'autorisation de mise sur le marché de TADIM
TADIM est destiné à être inhalé par nébulisation, en utilisant un nébuliseur adapté :
- soit un système de nébulisation « classique » nécessitant un générateur pneumatique (de type système Pari LC) ;
- soit un système de nébulisation portable dit « système I-neb AAD », équipé des technologies AAD (délivrance adaptée d'aérosol) et VMT (technologie de la membrane vibrante) ou un système Respironics Sidestream avec un compresseur Portaneb.
Tableau I - Caractéristiques de nébulisation de la colistiméthate sodique
sur la base d'études in vitro réalisées avec différents systèmes d'inhalation
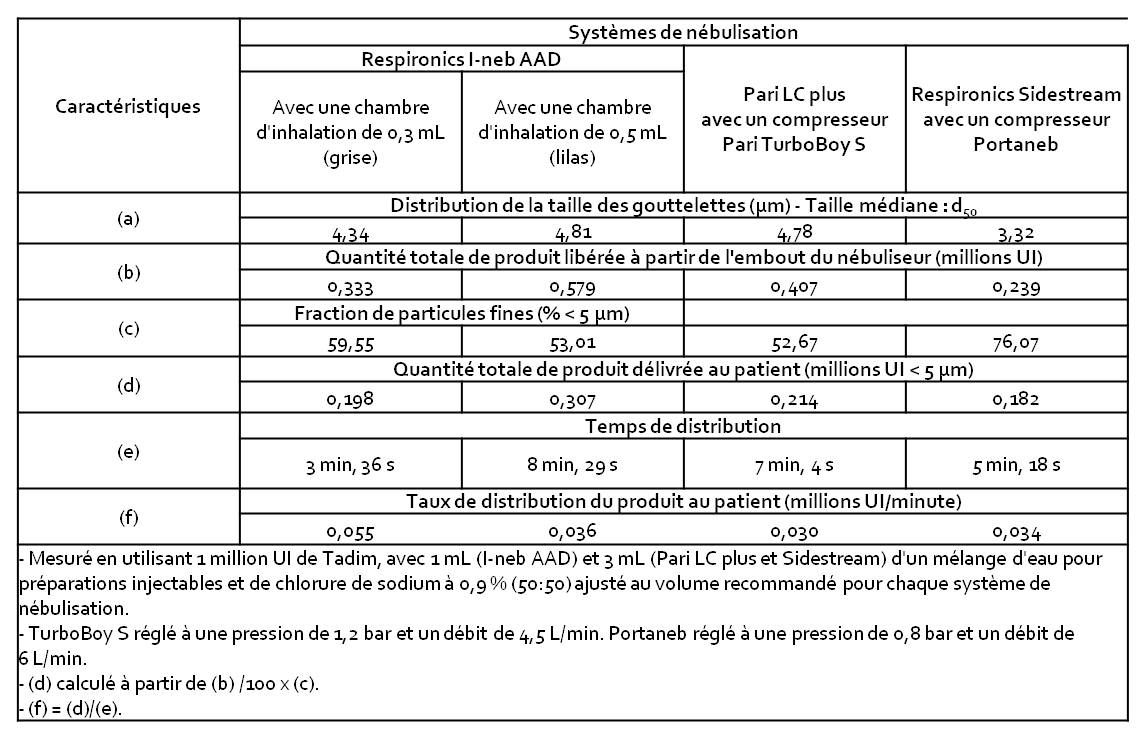
sur la base d'études in vitro réalisées avec différents systèmes d'inhalation

Un seul système de nébulisation étudié dans les essais cliniques
Dans son avis du 22 janvier 2014, la Commission de la transparence indique qu'"aucune étude clinique n'a évaluée l'efficacité et la tolérance du colistiméthate de sodium (ou colistine) dans le cadre de son utilisation avec les systèmes de nébulisation portables équipés des technologies AAD et VMT (système I-neb AAD) ou le système Respironics Sidestream avec un compresseur Portaneb".
A l'inverse, elle précise que "l'utilisation du colistiméthate de sodium (ou colistine) par voie inhalée avec un système de nébulisation « classique » nécessitant un générateur pneumatique, dans le traitement de l'infection à Pseudomonas aeroginosa est bien établi avec un profil d'efficacité et de tolérance satisfaisant".
TADIM remboursable uniquement dans le cadre de son administration avec un système de nébulisation classique
Dans ce contexte, la Commission juge la place de TADIM difficile à préciser dans la stratégie thérapeutique lorsqu'il est utilisé avec le système I-neb AAD ou le système Respironics Sidestream avec compresseur Portaneb.
Elle considère en revanche que TADIM représente une option thérapeutique en alternative à l'usage de la colistine actuellement commercialisée sous forme de solution pour inhalation par nébuliseur, COLIMYCINE 1 MUI.
A ce titre, TADIM est remboursable et agréé aux Collectivités dans les indications et aux posologies de l'AMM lorsque l'administration est réalisée par un système de nébulisation classique nécessitant un générateur pneumatique.
Le service médical rendu de TADIM a été jugé insuffisant dans le cadre de son administration avec le système de nébulisation portable équipé des technologies AAD et VMT (système l-neb AAD) ou le système Respironics Sidestream avec un compresseur Portaneb.
Toutefois, la Commission "s'inquiète d'une utilisation préférentielle du dispositif portable, sans évaluation clinique, du fait de sa mise à disposition gratuite et de sa commodité d'emploi susceptible de rendre le patient plus autonome dans la prise en charge de sa maladie."
TADIM en pratique
Les doses recommandées de TADIM tiennent compte de l'âge du patient :
Dans son avis du 22 janvier 2014, la Commission de la transparence indique qu'"aucune étude clinique n'a évaluée l'efficacité et la tolérance du colistiméthate de sodium (ou colistine) dans le cadre de son utilisation avec les systèmes de nébulisation portables équipés des technologies AAD et VMT (système I-neb AAD) ou le système Respironics Sidestream avec un compresseur Portaneb".
A l'inverse, elle précise que "l'utilisation du colistiméthate de sodium (ou colistine) par voie inhalée avec un système de nébulisation « classique » nécessitant un générateur pneumatique, dans le traitement de l'infection à Pseudomonas aeroginosa est bien établi avec un profil d'efficacité et de tolérance satisfaisant".
TADIM remboursable uniquement dans le cadre de son administration avec un système de nébulisation classique
Dans ce contexte, la Commission juge la place de TADIM difficile à préciser dans la stratégie thérapeutique lorsqu'il est utilisé avec le système I-neb AAD ou le système Respironics Sidestream avec compresseur Portaneb.
Elle considère en revanche que TADIM représente une option thérapeutique en alternative à l'usage de la colistine actuellement commercialisée sous forme de solution pour inhalation par nébuliseur, COLIMYCINE 1 MUI.
A ce titre, TADIM est remboursable et agréé aux Collectivités dans les indications et aux posologies de l'AMM lorsque l'administration est réalisée par un système de nébulisation classique nécessitant un générateur pneumatique.
Le service médical rendu de TADIM a été jugé insuffisant dans le cadre de son administration avec le système de nébulisation portable équipé des technologies AAD et VMT (système l-neb AAD) ou le système Respironics Sidestream avec un compresseur Portaneb.
Toutefois, la Commission "s'inquiète d'une utilisation préférentielle du dispositif portable, sans évaluation clinique, du fait de sa mise à disposition gratuite et de sa commodité d'emploi susceptible de rendre le patient plus autonome dans la prise en charge de sa maladie."
TADIM en pratique
Les doses recommandées de TADIM tiennent compte de l'âge du patient :
- chez les adultes, les adolescents et les enfants de 2 ans et plus, la posologie recommandée est de 1 à 2 MUI 2 à 3 fois par jour. La dose maximale est 6 MUI/jour ;
- chez l'enfant de moins de 2 ans, la posologie recommandée est de 0,5 à 1 MUI 2 fois par jour, avec une posologie maximale de 2 MUI/jour.
- Prescription en UI
Dans l'Union Européenne (UE), la dose de colistiméthate sodique (CMS) doit être prescrite et administrée seulement en unités internationales (UI).
Aux États-Unis et dans d'autres parties du monde, la dose est exprimée en milligrammes d'activité de colistine base (mg ACB).
Ces différentes expressions de dose en termes d'activité ont conduit à des confusions et des erreurs médicamenteuses.
Le tableau de conversion suivant est proposé pour information et les valeurs doivent être seulement considérées comme indicatives et approximatives (cf. Tableau II).
Aux États-Unis et dans d'autres parties du monde, la dose est exprimée en milligrammes d'activité de colistine base (mg ACB).
Ces différentes expressions de dose en termes d'activité ont conduit à des confusions et des erreurs médicamenteuses.
Le tableau de conversion suivant est proposé pour information et les valeurs doivent être seulement considérées comme indicatives et approximatives (cf. Tableau II).
Tableau II - Tableau indicatif de conversion de la dose de colistiméthate sodique
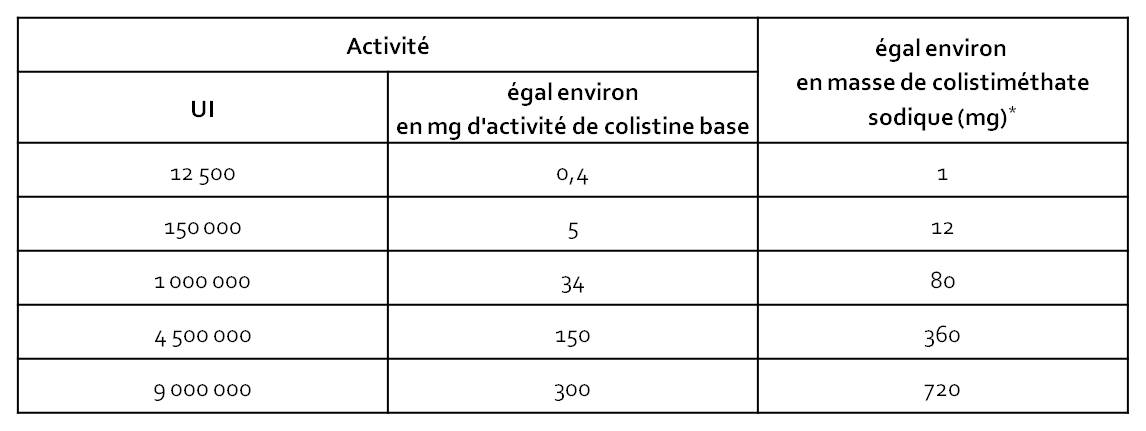
* Activité indicative de la substance active = 12 500 UI/mg.
- Reconstitution avec de l'eau ppi
Deux modes de reconstitution de TADIM peuvent être utilisés :
- avec de l'eau pour préparations injectables (eau ppi) afin d'obtenir une solution hypotonique limpide, incolore à jaune pâle,- avec un mélange 50/50 d'eau ppi et de solution de chlorure de sodium à 0,9 %, afin d'obtenir une solution isotonique limpide, incolore à jaune pâle.
- Conservation : utilisation immédiate de préférence
La stabilité physicochimique de la solution a été démontrée pendant 24 heures à température ambiante.
En cas d'auto-administration de l'antibiotique nébulisé, il doit être recommandé aux patients d'utiliser la solution immédiatement après sa préparation.
Si cela n'est pas possible, la solution doit être conservée au réfrigérateur pendant 24 heures au maximum.
En cas d'auto-administration de l'antibiotique nébulisé, il doit être recommandé aux patients d'utiliser la solution immédiatement après sa préparation.
Si cela n'est pas possible, la solution doit être conservée au réfrigérateur pendant 24 heures au maximum.
- Dispersion de l'aérosol dans l'environnement
Les nébuliseurs habituellement utilisés fonctionnent sur la base d'un flux continu et il est vraisemblable qu'une partie du produit administré soit libéré dans l'environnement du patient.
Avec un nébuliseur classique, il est recommandé de réaliser le traitement dans une pièce correctement ventilée, en particulier dans un contexte hospitalier où il est possible que plusieurs patients utilisent un nébuliseur en même temps.
Un système de tuyaux ou des filtres peuvent permettre d'éviter la dispersion de l'aérosol dans l'environnement.
Identité administrative
Avec un nébuliseur classique, il est recommandé de réaliser le traitement dans une pièce correctement ventilée, en particulier dans un contexte hospitalier où il est possible que plusieurs patients utilisent un nébuliseur en même temps.
Un système de tuyaux ou des filtres peuvent permettre d'éviter la dispersion de l'aérosol dans l'environnement.
Identité administrative
- Liste I
- Prescription initiale hospitalière de 6 mois
- Renouvellement non restreint
- Boîte de 30 flacons, renfermant un disque TADIM DISK pour utilisation avec le système I-neb AAD, CIP 3400938711325
- Remboursable à 65 % (Journal officiel du 11 juillet 2014 - texte 25)
- Prix public TTC = 341,74 euros
- Agrément aux collectivités (Journal officiel du 11 juillet 2014 - texte 26)
- Laboratoire Zambon France
Pour aller plus loin
Consultez les monographies VIDAL
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.