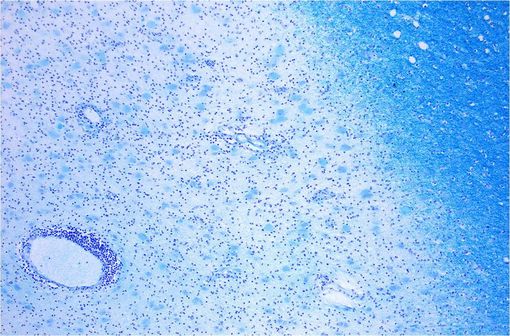
Lésions de démyélinisation par scléroses multiples (illustration @Marvin 101, sur Wikimedia).
Un effet immunosuppresseur à l'origine d'effets secondaires graves
De nouvelles recommandations d'utilisation et de surveillance sont ajoutées au résumé des caractéristiques du produit (RCP) de l'immunosuppresseur sélectif GILENYA 0,5 mg gélule (fingolimod).
Indiqué dans le traitement de fond des formes très actives de sclérose en plaques (SEP) rémittente-récurrente, le fingolimod présente des effets immunosuppresseurs, exposant les patients à des effets indésirables graves tels que :
- un carcinome basocellulaire : des cas ont été rapportés dans les essais cliniques et depuis la commercialisation de GILENYA ;
- une leucoencéphalopathie multifocale progressive (LEMP) à virus John-Cunningham (JCV), d'issue potentiellement fatale (voir notre article du 30 avril 2015) ;
- des lymphomes ;
- des infections opportunistes, y compris les infections du système nerveux central.
Une surveillance renforcée : examen dermatologique, IRM et NFS
Dans un courrier adressé aux neurologues et aux médecins généralistes, le laboratoire Novartis détaille les recommandations visant à renforcer la sécurité d'emploi de GILENYA.
- Prévention du risque de carcinome basocellulaire : examen dermatologique
Cet examen doit être pratiqué avant l'initiation du traitement, après au moins 1 an, puis au moins une fois par an si nécessaire.
En cas de lésions suspectes, une consultation dermatologique doit être programmée.
- Prévention du risque de LEMP : IRM
En cas de suspicion de LEMP, le traitement doit être interrompu en attendant les résultats de l'IRM et tant que le diagnostic de LEMP n'est pas écarté.
A noter qu'un test de détection des anticorps anti-JCV négatif n'exclut pas la possibilité d'une infection ultérieure par le JCV. L'influence de la lymphopénie sur la précision du test de détection des anticorps anti-JCV n'a pas été étudiée chez les patients traités par fingolimod.
L'information des patients et de leur entourage est importante pour permettre une prise en charge précoce, en présence de signes évocateurs de LEMP.
- Prévention du risque d'infections opportunistes
- infections virales par le virus herpès simplex, ou le virus varicelle-zona ;
- infections fongiques, comme les méningites à cryptocoques ;
- infections bactériennes, à mycobactéries atypiques par exemple.
Le traitement par GILENYA ne doit pas être instauré en cas d'infection active sévère non résolue. L'instauration du traitement doit alors être différée.
En cas de survenue d'une infection sévère chez un patient sous GILENYA, le traitement doit être interrompu. La reprise du traitement doit être évaluée au cas par cas.
Il est nécessaire de rester vigilant quant à l'apparition d'éventuelles infections pendant la période d'élimination du fingolimod, qui peut prendre jusqu'à 2 mois après l'arrêt du traitement.
- NFS, un contrôle périodique
Cette surveillance doit permettre de s'assurer de la résolution des effets immunitaires du traitement antérieur (cytopénie).
La NFS doit ensuite être contrôlée de façon périodique pendant le traitement :
- à 3 mois de traitement,
- puis au moins 1 fois par an,
- et en présence de signes d'infection.
Pour mémoire
GILENYA est indiqué en monothérapie comme traitement de fond des formes très actives de sclérose en plaques (SEP) rémittente-récurrente pour les groupes de patients adultes suivants (Cf. Reco VIDAL Sclérose en plaques) :
- patients présentant une forme très active de la maladie malgré un traitement complet et bien conduit par au moins un traitement de fond de la sclérose en plaques,
- ou patients présentant une sclérose en plaques rémittente-récurrente sévère et d'évolution rapide, définie par 2 poussées invalidantes ou plus au cours d'une année associées à 1 ou plusieurs lésion(s) rehaussée(s) après injection de gadolinium sur l'IRM cérébrale ou une augmentation significative de la charge lésionnelle en T2 par rapport à une IRM antérieure récente.
Pour aller plus loin
Fingolimod (Gilenya®) : Risques liés aux effets sur le système immunitaire (ANSM, 27 janvier 2016)
Lettre aux neurologues et aux médecins généralistes (sur le site de l'ANSM, 27 janvier 2016)
Sur Vidal.fr
GILENYA (fingolimod) : premier cas de LEMP chez un patient atteint de SEP, naïf d'autres traitements immunosuppresseurs (30 avril 2015)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.