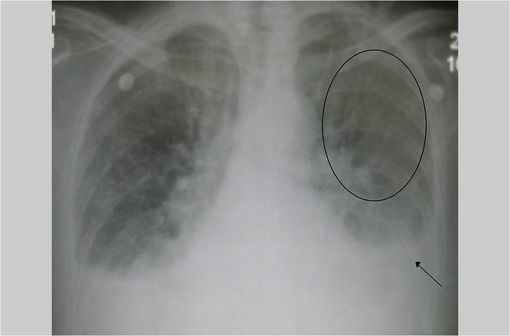
Œdème pulmonaire aigu : taille du cœur augmentée, redistribution vasculaire apicale (cercle) et petit épanchement pleural bilatéral (flèche) [illustration @Dr James Heilman, sur Wikimedia).
Une évaluation des données de sécurité d'emploi issues des essais cliniques et de la notification spontanée a mis en évidence l'existence d'un risque d'insuffisance cardiaque (IC) suite à la prise de crizotinib.
Le crizotinob est le principe actif de XALKORI, un antinéoplasique inhibiteurs des protéine-tyrosine kinases, indiqué dans le traitement des patients adultes ayant reçu au moins un traitement antérieur pour un cancer du poumon non à petites cellules (CPNPC) anaplastic lymphoma kinase (ALK)-positif et avancé (Cf. Reco VIDAL Cancer du poumon).
Selon les données des études cliniques : 1,1 % d'IC tous grades confondus
Les données des études cliniques ont porté sur 1 669 patients traités par crizotinib pour un cancer du poumon non à petites cellules ALK-positif. Selon ces données :
- 19 patients ont présenté une insuffisance cardiaque tous grades confondus pendant le traitement, soit une fréquence de survenue de 1,1 % ;
- 8 patients ont présenté une insuffisance cardiaque de grade 3 ou 4 pendant le traitement, soit 0,5 % ;
- 3 cas d'issue fatale ont été rapportés, soit 0,2 %.
Un effet indésirable identifié par le dispositif de pharmacovigilance
L'augmentation du risque d'insuffisance cardiaque associé au traitement par crizotinib a été identifiée par le système de pharmacovigilance.
Depuis la commercialisation de XALKORI (en janvier 2013 en France, sorti de la réserve hospitalière en septembre 2013) jusqu'au 25 février 2015, 40 cas d'insuffisance cardiaque ont été signalés sur un total de 14 700 patients traités pendant cette période, soit une fréquence de survenue de 0,27 %.
Parmi les 40 notifications, 15 patients sont décédés.
Un risque accru en début de traitement
Les données de pharmacovigilance montrent que la majorité des cas est survenue lors du premier mois de traitement.
Les symptômes d'insuffisance cardiaque ont disparu après l'arrêt du traitement chez 7 patients :
- pour 3 d'entre eux, les symptômes sont réapparus à la reprise du traitement par crizotinib ;
- 3 de ces 7 patients ne présentaient aucun trouble cardiaque associé (antécédents médicaux, co-morbidité, traitements concomitants).
Mise en garde supplémentaire : en pratique
La surveillance des patients recevant XALKORI doit permettre d'identifier les signes évocateurs d'insuffisance cardiaque tels qu'une dyspnée, un oedème, une prise de poids rapide due à une rétention d'eau.
Cette nouvelle mise en garde concerne tous les patients, avec ou sans antécédents cardiaques.
Elle s'ajoute aux mesures de surveillance déjà mentionnées dans le résumé des caractéristiques du produit (RCP) de XALKORI :
- hépatotoxicité : bilan de la fonction hépatique incluant ALAT, ASAT et bilirubine totale, 1 fois par semaine au cours des 2 premiers mois de traitement, puis 1 fois par mois et si cliniquement indiqué, et plus fréquemment en cas d'augmentation de grade 2, 3 ou 4 ;
- pneumopathie interstitielle : surveillance des symptômes pulmonaires évocateurs ;
- allongement de l'intervalle QT : surveillance périodique des électrocardiogrammes (ECG), des électrolytes et de la fonction rénale ;
- bradycardie ;
- neutropénie et leucopénie : numération de la formule sanguine, incluant une numération différentielle des globules blancs, si cliniquement indiquée ;
- perforation gastro-intestinale ;
- insuffisance rénale ;
- effets visuels.
Arrêt, suspension ou modification du traitement
La présence de signes et symptômes évoquant une insuffisance cardiaque doit conduire à la mise en place de mesures adaptées par les spécialistes en oncologie ou les médecins compétents en cancérologie hospitaliers, auxquels cette prescription est réservée.
Ces mesures peuvent consister en une diminution des doses de crizotinib, une suspension du traitement, ou un arrêt complet.
Pour aller plus loin
XALKORI (crizotinib) gélules à 200 et 250 mg pour voie orale : ajout d'une nouvelle mise en garde concernant l'insuffisance cardiaque (ANSM, 15 octobre 2015)
Lettre aux médecins oncologues et cardiologues (sur le site de l'ANSM, 6 octobre 2015)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.