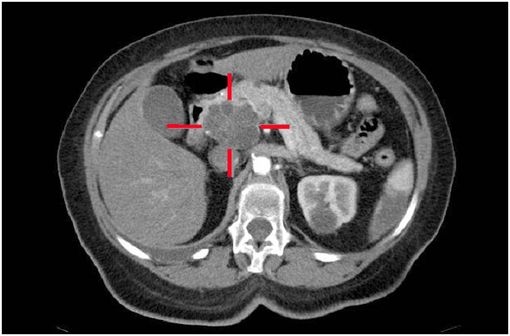
Adénocarcinome kystique de la tête du pancréas sur une coupe de scanner avec injection de produit de contraste (illustration @MBq, sur Wikimedia).
L'arrêté du 15 septembre 2015 publié au Journal officiel du 22 septembre 2015 étend la prise en charge du médicament ABRAXANE 5 mg/ml poudre pour suspension injectable pour perfusion (paclitaxel albumine) au traitement du cancer pancréatique.
Plus précisément, ABRAXANE en association avec la gemcitabine est désormais agréé aux collectivités dans le traitement de première ligne de l'adénocarcinome du pancréas métastatique chez les patients adultes.
Jusqu'à présent, ABRAXANE était agréé aux collectivités uniquement dans le traitement de deuxième ligne du cancer du sein métastatique (Cf. Reco VIDAL Cancer du sein).
Une médiane de survie globale allongée de 1,8 mois
Dans son avis du 15 octobre 2014, la Commission de la transparence s'est appuyée sur l'étude MPACT (CA046) de phase III, randomisée en ouvert, comparant l'efficacité et la tolérance en première ligne de l'association nab-paclitaxel (125 mg/m² en perfusion IV) + gemcitabine (1 000 mg/m² en perfusion IV) versus gemcitabine seule (1 000 mg/m² en perfusion IV) chez 861 patients ayant un adénocarcinome du pancréas métastatique (voir l'étude : Von Hoff and al. N Engl J Med 2013).
Le critère principal de jugement était la survie globale, définie comme la durée entre la rodomisation et le décès du patient.
Les résultats ont montré que la médiane de survie globale a été allongée de 1,8 mois dans le groupe nab-paclitaxel + gemcitabine par apport au groupe gemcitabine seule (8,5 mois vs 6, 7 mois respectivement, HR = 0,72 ; IC95 % = [0,617 ; 0,835] ; p < 0,0001).
Le pourcentage de survie estimé à 12 mois a été :
- de 35 % (108/431 patients) dans le groupe nab-paclitaxel + gemcitabine (IC95 % = [29,7;39,5]) ;
- versus 22 % (69/430 patients) dans le groupe gemcitabine seule (IC95 % = [18,1;26,7]).
- de 9 % (16 patients) dans le groupe nab-paclitaxel + gemcitabine (IC95 % = [6,2;13,1] ;
- versus 4 % (7 patients) dans le groupe gemcitabine seule (IC95 % = [2,3;7,2]).
En termes de tolérance, la toxicité de l'association nab-paclitaxel/gemcitabine a été plus élevée que celle de la gemcitabine seule, et principalement d'ordres hématologique (neutropénie de grades 3-4 dans 1/3 des cas dans 1/3 des cas : 33 % vs 21 %), neurologique (neuropathie périphérique de grades 3-4 : 17 % vs 21 %) et gastro-intestinale.
De même, les interruptions de traitement pour événement indésirable et les événements indésirables de grades >= 3 ont été plus nombreux (35 % vs 24 % et 89 % vs 75 %, respectivement).
La Commission de la transparence a conclu à un service médical rendu (SMR) important d'ABRAXANE en traitement de première ligne du cancer du pancréas métastatique.
"Il s'agit d'un traitement de première ligne chez les patients en bon état général, compte tenu du profil de toxicité (patients âgés de moins de 75 ans, ayant un score de performance de Karnofsky >= 80 %)".
En pratique : deux perfusions successives de 30 minutes chacune
Selon l'autorisation de mise sur le marché (AMM), ABRAXANE doit être utilisé en association avec la gemcitabine dans l'adénocarcinome du pancréas (Voir Monographie VIDAL d'ABRAXANE - Rubrique Posologie et mode d'administration).
La dose recommandée d'ABRAXANE est de 125 mg/m² administrée en perfusion intraveineuse de 30 minutes les jours 1, 8 et 15 de chaque cycle de 28 jours.
La dose concomitante recommandée de gemcitabine est de 1 000 mg/m² administrée en perfusion intraveineuse de 30 minutes immédiatement après la fin de l'administration d'ABRAXANE les jours 1, 8 et 15 de chaque cycle de 28 jours.
Ce traitement doit être soumis à une surveillance médicale, notamment hématologique.
Une neutropénie et/ou une thrombopénie survenant en début ou au cours d'un cycle doivent conduire à une réduction de la dose d'ABRAXANE, voire à une interruption du traitement.
Le traitement doit également être interrompu, ou la posologie modifiée, en cas de neuropathie périphérique de grade 3 ou 4, de toxicité cutanée de grade 2 ou 3 et de toxicité gastro-intestinale de grade 3 (mucite ou diarrhée).
Pour mémoire
ABRAXANE (paclitaxel) est un médicament antinéoplasique du groupe des taxanes.
Il est présenté en poudre pour suspension injectable pour perfusion à 5 mg/ml (dans une formulation de nanoparticules liées à l'albumine), en flacon de 100 mg (CIP 3400938441871).
Selon l'AMM (autorisation de mise sur le marché), ABRAXANE dispose de 3 indications :
- en monothérapie dans le traitement du cancer du sein métastatique, chez les patients adultes en échec du traitement de première ligne du cancer métastasé, et pour qui le traitement standard incluant une anthracycline n'est pas indiqué ;
- en association avec la gemcitabine, dans le traitement de première ligne de l'adénocarcinome du pancréas métastatique chez les patients adultes ;
- en association avec le carboplatine, dans le traitement de première ligne du cancer bronchique non à petites cellules chez les patients adultes qui ne sont pas candidats à une chirurgie potentiellement curative et/ou une radiothérapie.
ABRAXANE est disponible uniquement à l'hôpital.
Il est soumis à une prescription hospitalière, réservée aux spécialistes en oncologie ou en hématologie ou aux médecins compétents en cancérologie.
Pour aller plus loin
Se reporter à la monographie VIDAL d'ABRAXANE
Arrêté du 15 septembre 2015 modifiant la liste des spécialités pharmaceutiques agréées à l'usage des collectivités (Journal officiel, 22 septembre 2015 - texte 12)
Avis de la Commission de la Transparence (HAS, 15 octobre 2014)
Etude pivot
Von Hoff DD, Ervin T, Arena FP, Chiorean EG, Infante J, Moore M. Increased survival in pancreatic cancer with nabpaclitaxelplus gemcitabine. N Engl J Med. 2013;369:1691-703 (article)
Pour aller plus loin
Consultez les monographies VIDAL
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.