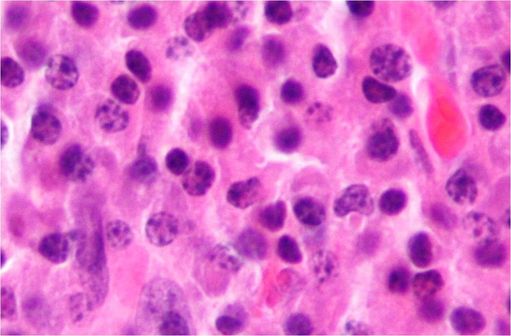
Histologiquement, le myélome multiple est un plasmocytome (illustration @ Nephron, sur Wikimedia).
Les risques suivants ont récemment été identifiés suite à une revue des données de sécurité par les autorités de santé européennes dans le cadre de la surveillance régulière du pomalidomide :
- risque de toxicité hépatique aiguë ;
- risque de pneumopathie interstitielle diffuse ;
- risque d'insuffisance cardiaque.
Surveiller les paramètres de la fonction hépatique
La revue des données de sécurité du pomalidomide a permis d'identifier des cas graves d'hépatite aiguë, pouvant entraîner une hospitalisation et nécessiter l'arrêt du traitement.
Ce risque serait plus élevé au cours des 6 premiers mois de traitement.
Des cas d'insuffisance hépatocellulaire aiguë (dont certains d'issue fatale) ont été rapportés, sans démonstration du lien de causalité avec le pomalidomide.
Pour minimiser le risque de toxicité hépatique, il est recommandé de surveiller les paramètres de la fonction hépatique :
- plus particulièrement au cours des 6 premiers mois de traitement par pomalidomide ;
- puis en tenant compte des données cliniques du patient.
Surveiller attentivement les symptômes pulmonaires
Les cas de pneumopathies interstitielles diffuses ont principalement été observés au cours des 6 premiers mois de traitement par pomalidomide, et jusqu'à 18 mois dans certains cas.
La mise en place d'une corticothérapie et l'arrêt définitif du traitement par pomalidomide conduisent généralement à la résolution de la pneumopathie.
Il est recommandé :
- de réaliser une évaluation respiratoire attentive en cas d'apparition subite ou d'aggravation inexpliquée de symptômes pulmonaires chez des patients traités par pomalidomide, afin d'éliminer le diagnostic de pneumopathie interstitielle diffuse ;
- de suspendre le traitement pendant l'évaluation de ces symptômes ;
- de mettre en place un traitement approprié si le diagnostic se révèle positif.
Surveiller les patients à risque d'insuffisance cardiaque
Le risque d'insuffisance cardiaque a été observé principalement chez des patients présentant une cardiopathie préexistante ou des facteurs de risque cardiaque (hypertension artérielle).
Des événements associés ont été rapportés, tels qu'une insuffisance cardiaque congestive, une insuffisance cardiaque aiguë et un oedème pulmonaire.
Le pomalidomide serait également associé à un risque de fibrillation auriculaire.
Ces événements sont survenus majoritairement au cours des 6 premiers mois de traitement.
Il est recommandé de surveiller régulièrement, pendant toute la durée du traitement par pomalidomide, la survenue de signes ou symptômes évoquant une insuffisance cardiaque, chez les patients à risque.
Pour mémoire
IMNOVID est indiqué, en association avec la dexaméthasone, dans le traitement du myélome multiple en rechute et réfractaire chez les patients adultes ayant déjà reçu au moins deux traitements antérieurs comportant le lénalidomide et le bortézomib, et dont la maladie a progressé pendant le dernier traitement (voir Reco VIDAL "Myélome multiple").
Pour aller plus loin
Communiqué - Pomalidomide (Imnovid®) : nouvelles recommandations importantes de minimisation des risques (ANSM, 27 avril 2015)
Lettre aux oncologues, hématologues, médecins compétents en cancérologie ou maladies du sang, pharmaciens hospitaliers (sur le site de l'ANSM, 21 avril 2015)
Sur VIDAL.fr
IMNOVID gélule (pomalidomide) : nouveau médicament dans la prise en charge du myélome multiple (12 décembre 2013)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.