
FIBROVEIN solution injectable IV (tétradécyl sulfate de sodium) est un nouvel agent sclérosant pour injection locale, indiqué chez l'adulte dans le traitement :
- des varices primaires non compliquées,
- des varices récidivantes ou résiduelles suite à une intervention chirurgicale,
- des veines réticulaires, des veinules et des varicosités des membres inférieurs caractérisées par une dilatation simple.
FIBROVEIN est disponible sous 4 concentrations : 0,2 %, 0,5 %, 1 % et 3 %.
Le choix de la concentration se fera en fonction du type et du diamètre des varices à scléroser :
- les varicosités ne doivent être traitées qu'avec une solution à 0,2 %,
- les veines réticulaires avec une solution à 0,5 %,
- la solution de 1 % est plus utile pour les varices de petit ou moyen calibre
- la solution à 3 % est réservée aux varices de gros calibre.
Les concentrations à 1 % et 3 % sont les seules à être autorisées pour une utilisation sous forme de mousse dans le traitement des plus grosses veines.
La mousse ne doit être utilisée que pour le traitement des grosses veines et le volume total maximum à injecter par séance doit être rigoureusement respecté.
Les posologies chez l'adulte et le sujet âgé sont les suivantes :
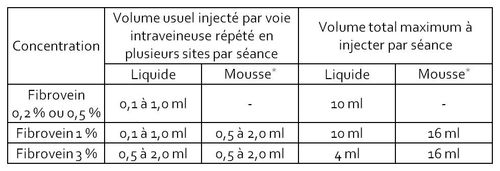
* Le volume est la somme des composants liquide + air.
Une formation est nécessaire pour réaliser la sclérothérapie à la mousse
Dans sa lettre aux professionnels de santé (angiologues, phlébologues, cardiologues), le laboratoire STD Pharmaceutical Products Limited rappelle que la sclérothérapie à la mousse présente des risques spécifiques à cette forme.
Une formation appropriée des médecins est nécessaire afin d'apprendre comment préparer et administrer correctement la mousse, en tenant compte des mises en garde spéciales et des précautions d'emploi de la spécialité utilisée (voir Guide de préparation de FIBROVEIN 1 % et 3 % pour la sclérothérapie à la mousse, joint à la lettre du laboratoire).
Des contre-indications et des précautions d'emploi
L'utilisation de FIBROVEIN est contre-indiquée chez les patients ayant un foramen ovale perméable (FOP) symptomatique connu.
La sclérothérapie est contre-indiquée chez les patients présentant un risque élevé de thrombose.
L'utilisation de FIBROVEIN nécessite des précautions d'emploi :
- chez les patients porteurs d'un FOP connu mais asymptomatique,
- chyezles patients présentant des difficultés respiratoires ou une forte prédisposition allergique,
- et chez les patients présentant des antécédents de migraine.
Informer et surveiller le patient
Les patients doivent être informés par le praticien des risques inhérents à la technique.
Les patients doivent être surveillés après la sclérothérapie. Un contrôle doit être réalisé un mois après la réalisation de cet acte.
Identité administrative
- Liste I
- FIBROVEIN 0,2 %, 2 flacons de 5 ml, CIP 3400926882365
- FIBROVEIN 0,2 %, 5 flacons de 5 ml, CIP 3400926882426
- FIBROVEIN 0,2 %, 10 flacons de 5 ml, CIP 3400926882594
- FIBROVEIN 0,5 %, 5 ampoules de 2 ml, CIP 3400926882655
- FIBROVEIN 1 %, 5 ampoules de 2 ml, CIP 3400926883256
- FIBROVEIN 3 %, 5 ampoules de 2 ml, CIP 3400926883607
- FIBROVEIN 3 %, 2 flacons de 5 ml, CIP 3400926883317
- FIBROVEIN 3 %, 5 flacons de 5 ml, CIP 3400926883485
- FIBROVEIN 3 %, 10 flacons de 5 ml, CIP 3400926883546
- Non remboursable
- Laboratoire Novex Pharma
Pour aller plus loin
Monographie VIDAL de FIBROVEIN (mise à jour du 22 octobre 2014)
Communiqué - Fibrovein 0.2%, 0.5%, 1% et 3%, solution injectable (tetradecyl sulfate de sodium : bon usage et sécurité d'emploi de la sclérothérapie à la mousse (ANSM, 25 novembre 2014)
Lettre du laboratoire STD Pharmaceutical Products Limited aux professionnels de santé (sur le site de l'ANSM, 25 novembre 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Sources
- ANSM (Agence nationale de sécurité du médicament et des produits de santé) Laboratoire Novex Pharma
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.