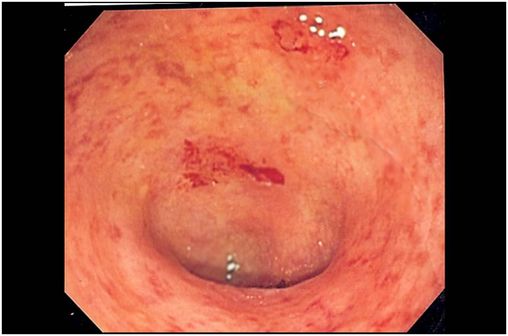
Image endoscopique de lésions de rectocolite hémorragique localisées au niveau du côlon sigmoïde (cliché @ UC granularity sur Wikimedia).
ENTYVIO 300 mg poudre pour solution à diluer pour solution pour perfusion (védolizumab) est un nouvel anticorps monoclonal humanisé indiqué dans les situations suivantes :
- traitement de la rectocolite hémorragique active modérée à sévère chez les patients adultes présentant une réponse insuffisante ou une perte de réponse ou une intolérance à un traitement conventionnel ou par anti-TNF (antagoniste du facteur de nécrose tumorale alpha) ;
- traitement de la maladie de Crohn active modérée à sévère chez les patients adultes présentant une réponse insuffisante ou une perte de réponse ou une intolérance à un traitement conventionnel ou par anti-TNF (antagoniste du facteur de nécrose tumorale alpha).
Le traitement par ENTYVIO doit être instauré et supervisé par des professionnels de santé expérimentés dans le diagnostic et le traitement de la rectocolite hémorragique et la maladie de Crohn. La notice et la carte d'alerte patient doivent être fournies aux patients.
A propos du védolizumab
Le védolizumab est un anticorps monoclonal humanisé obtenu par la technique de l'ADN recombinant.
Il a été conçu pour se fixer à l'intégrine alpha-4-bêta-7, une protéine principalement rencontrée à la surface de certains leucocytes présents dans l'intestin.
Dans le cas de la rectocolite hémorragique ou de la maladie de Crohn, ces cellules peuvent être à l'origine d'une inflammation de l'intestin.
En bloquant l'intégrine alpha-4-bêta-7, le védolizumab réduit l'inflammation de l'intestin ainsi que les symptômes de ces maladies.
ENTYVIO dans la rectocolite hémorragique
Dans le traitement de la rectocolite hémorragique, la posologie recommandée d'ENTYVIO est de 300 mg administrés par perfusion intraveineuse suivie de perfusions supplémentaires à 2 et 6 semaines, puis toutes les 8 semaines.
La poursuite du traitement devra être attentivement reconsidérée si aucun bénéfice thérapeutique n'est observé à la 10ème semaine.
Les patients échappant au traitement peuvent bénéficier d'une augmentation de la fréquence d'administration en passant à 300 mg d'ENTYVIO toutes les 4 semaines.
Chez les patients ayant répondu au traitement par ENTYVIO, les corticostéroïdes peuvent être réduits et/ou arrêtés, conformément aux normes de soins standards.
ENTYVIO dans la maladie de Crohn
Dans le traitement de la maladie de Crohn, la posologie recommandée est de 300 mg administrés par perfusion intraveineuse suivie de perfusions supplémentaires à 2 et 6 semaines, puis toutes les 8 semaines.
Les patients chez lesquels aucune réponse n'a été observée peuvent bénéficier d'une administration d'ENTYVIO à la 10ème semaine.
À partir de la 14ème semaine, le traitement sera poursuivi toutes les 8 semaines chez les patients répondeurs. Le traitement devra être arrêté si aucun bénéfice thérapeutique n'est observé à la 14ème semaine.
Certains patients ayant échappé au traitement peuvent bénéficier d'une augmentation de la fréquence d'administration en passant à 300 mg d'ENTYVIO toutes les 4 semaines.
Chez les patients ayant répondu au traitement par ENTYVIO, les corticostéroïdes peuvent être réduits et/ou arrêtés, conformément aux normes de soins standards.
Administration et surveillance : en pratique
ENTYVIO est administré par voie intraveineuse uniquement, en perfusion de 30 minutes.
Le médicament doit être reconstitué puis dilué avant l'administration intraveineuse selon les instructions détaillées dans la monographie VIDAL d'ENTYVIO.
Une surveillance des patients s'impose durant et après la perfusion.
Tous les patients doivent faire l'objet d'une surveillance continue pendant chaque perfusion :
- pour les deux premières perfusions, il convient de les garder en observation pendant environ 2 heures après la fin de la perfusion afin de déceler d'éventuels signes et symptômes d'hypersensibilité aiguë ;
- pour toutes les perfusions suivantes, les patients seront surveillés pendant environ 1 heure après la fin de la perfusion.
Identité administrative
- Liste I
- Médicament réservé à l'usage hospitalier
- Prescription réservée aux spécialistes en gastroentérologie et hépatologie ou en médecine interne
- Flacon unitaire de 20 ml, CIP 3400958672873
- Laboratoire Takeda
ENTYVIO est agréé aux collectivités dans le traitement de la RCH et de la maladie de Crohn actives modérées à sévères.
La prise en charge est accordée uniquement pour les patients en échec (réponse insuffisante, perte de réponse ou intolérance) des corticoïdes, des immunosuppresseurs et des anti-TNF (Journal officiel du 10 janvier 2017 - texte 3).
Les patients naïfs de traitement anti-TNF sont exclus du périmètre de prise en charge d'ENTYVIO. Dans cette population, la Commission de la Transparence a jugé le SMR (service médical rendu) insuffisant (Avis du 7 janvier 2015). /FIN EDIT
Pour aller plus loin
Se reporter à la monographie VIDAL d'ENTYVIO (mise à jour du 23 octobre 2014)
Résumé à l'intention du public (EMA, 16 juin 2014)
EDIT du 13 janvier 2017 :
Inscription sur la liste des spécialités agréées aux collectivités (Journal officiel du 10 janvier 2017 - texte 3)
Avis de la Commission de la Transparence (HAS, 7 janvier 2015)
/FIN EDIT
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.