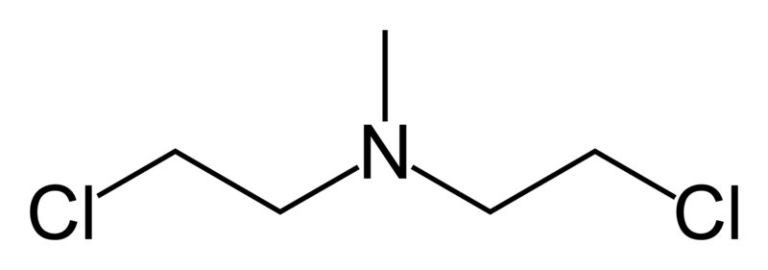
La chlorméthine a été le premier agent alkylant à être utilisé en thérapeutique en 1942 (image : © Benjah-bmm27, Wikimedia).
Le laboratoire Orphan Europe, en accord avec l'ANSM (Agence nationale de sécurité du médicament et des produits de santé), informe les professionnels de santé de la mise à disposition exceptionnelle et transitoire de MUSTARGEN (chlorhydrate de méchloréthamine, ou chlorméthine), spécialité importée des Etats-Unis afin de pallier la rupture de stock de CARYOLYSINE 10 mg solution à diluer et solvant pour solution injectable et pour application cutanée (chlorhydrate de chlorméthine).
MUSTARGEN est proposé en tant qu'alternative de CARYOLYSINE dans le traitement du lymphome cutané T épidermotrope (mycosis fongoïdes).
En pratique
A la différence de CARYOLYSINE, MUSTARGEN se présente sous forme d'une poudre en flacon, contenant 10 mg de méchloréthamine (ou chlorméthine) mélangée à du chlorure de sodium.
La composition en excipients diffère entre la spécialité américaine et la spécialité française.
Dans le traitement du lymphome cutané T épidermotrope, l'administration de MUSTARGEN doit être cutanée. En raison des propriétés cytotoxiques de la mechloréthamine, les procédures spéciales de reconstitution et de manipulation doivent être étudiées et suivies méticuleusement.
MUSTARGEN : usage hospitalier exclusif
L'ANSM a réservé l'usage de MUSTARGEN au milieu hospitalier.
La prescription est réservée aux oncologues et dermatologues ayant une spécialisation en oncologie.
Une hospitalisation à domicile (HAD) du patient pourra être mise en œuvre, sur demande du médecin traitant, en accord avec le médecin coordinateur du service d'HAD afin d'assurer la reconstitution et l'administration sécurisée du MUSTARGEN par des professionnels de santé au domicile du patient.
Sources et ressources complémentaires
CARYOLYSINE 10 mg, solution à diluer et solvant pour solution injectable et pour application cutanée (chlorméthine) - Rupture de stock (ANSM, 26 septembre 2013)
Lettre du laboratoire ORPHAN EUROPE aux médecins oncologues, pharmaciens hospitaliers et médecins coordonateurs d'HAD (sur le site de l'ANSM, 9 septembre 2013)
Notice d'information de MUSTARGEN (sur le site de l'ANSM, 26 septembre 2013)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.