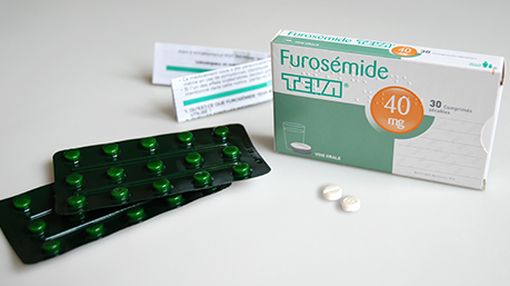
La découverte d'un comprimé de zopiclone dans un blister de Furosémide TEVA 40 semble être un "phénomène isolé".
L'alerte a été donnée le 7 juin dernier. La présence de comprimés de zopiclone dans une boîte de FUROSEMIDE TEVA 40 mg comprimé sécable, signalée par un pharmacien d'officine de Saint-Malo, a conduit le laboratoire génériqueur et l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) à retirer les lots Y175 et Y176 de ce médicament. Quelques jours plus tard, cette mesure était étendue à tous les lots de FUROSEMIDE TEVA 40 mg comprimé sécable.
Suite à cette alerte, plusieurs cas d'effets indésirables graves ont été signalés chez des patients traités par du FUROSEMIDE TEVA 40 mg , dont le décès d'un homme de 91 ans à Marseille. Les examens pratiqués ont cependant montré l'absence de zopiclone dans l'organisme de ce dernier.
L'inspection ne montre pas d'anomalie de conditionnement
L'inspection du site de conditionnement Teva, effectuée par l'ANSM dès le lundi 10 juin, n'a pas permis d'identifier de "défaut majeur dans l'organisation, les pratiques ou les équipements". L'activité de ce site n'a par conséquent pas été suspendue.
Aucun élément objectif ne permet donc aujourd'hui d'expliquer la présence éventuelle de comprimés de zopiclone dans les blisters de FUROSEMIDE TEVA 40 mg.
Aucun élément objectif ne permet donc aujourd'hui d'expliquer la présence éventuelle de comprimés de zopiclone dans les blisters de FUROSEMIDE TEVA 40 mg.
Une enquête complémentaire ouverte par le Parquet de Paris (pôle santé) doit permettre d'explorer d'autres hypothèses, comme celle d'un acte de malveillance isolé.
Recherche infructueuse de comprimés de zopiclone dans les boîtes de Furosémide
En parallèle, le laboratoire Teva a procédé à une vérification sous contrôle d'huissier des boîtes de furosémide récupérées. Selon les dernière données, 2 374 boîtes ont été examinés, correspondant à plus de 70 000 comprimés, sans qu'aucun comprimé de zopiclone n'ait été retrouvé.
Le donneur d'alerte confirme avoir découvert une inversion de comprimés
Devant l'absence d'anomalie et d'autres inversions de comprimés dans les boîtes de Furosémide Teva 40, la question s'est posée, notamment sur les réseaux sociaux, de la réalité du signalement initial effectué par un pharmacien de Saint-Malo à l'origine du rappel de lot.
Mais ce dernier, Interrogé le 19 avril par France 3 Bretagne, a confirmé les circonstances l'ayant conduit à avertir le laboratoire de cette anomalie, suite à la plainte d'une de ses patientes. Il réfute une éventuelle erreur, sa collaboratrice ayant découvert, après avoir ouvert toutes les boîtes de Furosémide TEVA 40, un comprimé de zopiclone dans un blister intact, "bien fermé" de FUROSEMIDE TEVA 40 mg :
Mais ce dernier, Interrogé le 19 avril par France 3 Bretagne, a confirmé les circonstances l'ayant conduit à avertir le laboratoire de cette anomalie, suite à la plainte d'une de ses patientes. Il réfute une éventuelle erreur, sa collaboratrice ayant découvert, après avoir ouvert toutes les boîtes de Furosémide TEVA 40, un comprimé de zopiclone dans un blister intact, "bien fermé" de FUROSEMIDE TEVA 40 mg :
Dominique Maraninchi : un "phénomène isolé", mais les investigations se poursuivent
Invité sur Europe 1, Dominique Maraninchi, directeur de l'ANSM, a justifié les précautions prises depuis le 7 juin, précautions "nécessaires pour garantir la sécurité des patients". A l'heure actuelle et d'après les résultats des investigations en cours, cette anomalie apparaît comme un phénomène isolé, ce que le directeur de l'Agence estime plutôt rassurant.
Cependant, même si Mr Maraninchi parle de "fin d'alerte" (à 03:58 dans la vidéo ci-dessous), le FUROSEMIDE TEVA 40 mg reste encore indisponible à ce jour :
Cependant, même si Mr Maraninchi parle de "fin d'alerte" (à 03:58 dans la vidéo ci-dessous), le FUROSEMIDE TEVA 40 mg reste encore indisponible à ce jour :
Les enquêtes se poursuivent donc, afin de comprendre comment des comprimés de zopiclone se sont retrouvés dans des boîtes de furosémide.
Surtout, ne pas interrompre le traitement !
Le directeur de l'ANSM a également insisté sur les risques encourus par les patients en cas d'interruption de leur traitement par furosémide 40 mg. Il a rappelé par ailleurs que tout avait été mis en place afin que les patients poursuivent leur traitement par furosémide (une substitution par du furosémide 40 mg d'une autre marque a en effet été organisée en pharmacie d'officine dès le 10 juin).
En France, 57 000 patients étaient traités par du FUROSEMIDE TEVA 40 mg, sur 800 000 patients traités par furosémide.
Sources et ressources complémentaires
Furosémide Teva 40 mg : Point de situation au 19 juin 2013 - Point d'information, ANSM (19 juin 2013)
INFO FRANCE 3. Furosémide : le pharmacien à l'origine de l'affaire s'exprime pour la première fois, FranceTV Info (19 juin 2013)
Furosémide Teva : "il y a fin d'alerte", interview e Dominique Maraninchi, Europe 1 (20 juin 2013)
Dossier FUROSEMIDE TEVA 40 mg, ANSM (juin 2013)
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 3 minutes
3 minutes 2 commentaires
2 commentaires 




Les commentaires sont momentanément désactivés
La publication de commentaires est momentanément indisponible.