Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- ENFLONSIA
- ENFLONSIA 105 mg sol inj ser préremplie
Sommaire
clesrovimab
EEN sans dose seuil : polysorbate 80
Cip : 3400930328613
Modalités de conservation : Avant ouverture : 2° < t < 8° durant 30 mois (Conserver à l'abri de la lumière, Ne pas agiter, Conserver dans son emballage, Conserver au réfrigérateur, Ne pas congeler)
Après ouverture : 20° < t < 25° durant 48 heures (A utiliser une fois sorti du réfrigérateur, Eliminer toute fraction restante de manière appropriée)
| FORMES et PRÉSENTATIONS |
Solution injectable IM (limpide à légèrement opalescente, incolore à légèrement jaune, avec un pH de 5,5-6,5, et une osmolalité de 320-420 mOsm/kg).
Boîte contenant : 1 seringue préremplie de 0,7 mL de solution, avec piston et capuchon + 1 aiguille.
| COMPOSITION |
Chaque seringue préremplie contient 105 mg de clesrovimab dans 0,7 mL.
Le clesrovimab est un anticorps monoclonal entièrement humain de type immunoglobuline G1 kappa (IgG1κ) produit dans des cellules d'ovaires de hamster chinois (CHO) par la technologie de l'ADN recombinant.
Excipient à effet notoire
Ce médicament contient 0,14 mg de polysorbate 80 pour chaque dose de 105 mg (0,7 mL).
Histidine, chlorhydrate d'histidine monohydraté, chlorhydrate d'arginine, saccharose, polysorbate 80 (E433), eau pour préparations injectables.
| INDICATIONS |
Enflonsia est indiqué pour la prévention des infections des voies respiratoires inférieures dues au virus respiratoire syncytial (VRS) chez les nouveau-nés et les nourrissons au cours de leur première saison de circulation du VRS.
Enflonsia doit être utilisé conformément aux recommandations officielles en vigueur.
| POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
| CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
| MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Hypersensibilité, notamment l'anaphylaxie
En cas d'apparition de signes et symptômes d'une réaction cliniquement significative d'hypersensibilité ou d'anaphylaxie, un traitement approprié et/ou des soins de soutien doivent être initiés.
Personnes atteintes de thrombocytopénie et de troubles de la coagulation
Comme pour toute autre injection intramusculaire, le clesrovimab doit être administré avec prudence chez les nourrissons atteints de thrombocytopénie ou de tout trouble de la coagulation, car des saignements ou des ecchymoses peuvent survenir après une administration intramusculaire chez ces individus.
Excipients à effet notoire
Ce médicament contient 0,14 mg de polysorbate 80 par dose. Les polysorbates peuvent provoquer des réactions allergiques.
| INTERACTIONS |
Connectez-vous pour accéder à ce contenu
| EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
| SURDOSAGE |
Il n'existe pas de traitement spécifique en cas de surdosage avec du clesrovimab. En cas de surdosage, il convient de surveiller la survenue d'effets indésirables chez le patient et de lui administrer un traitement symptomatique approprié.
| PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
| PHARMACOCINÉTIQUE |
Connectez-vous pour accéder à ce contenu
| SÉCURITÉ PRÉCLINIQUE |
Les données non cliniques issues des études de tolérance à dose unique, de toxicité à doses répétées et de réactivité tissulaire croisée n'ont pas révélé de risque particulier pour l'homme.
| INCOMPATIBILITÉS |
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
| DURÉE DE CONSERVATION |
30 mois
Enflonsia peut être conservé à température ambiante (20 °C-25 °C) pendant 48 heures au maximum. Après avoir été sorti du réfrigérateur, il doit être utilisé dans les 48 heures ou jeté.
| PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
Conserver au réfrigérateur (2 °C-8 °C). Ne pas congeler.
Conserver la seringue préremplie dans l'emballage extérieur à l'abri de la lumière.
Ne pas secouer.
| PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
Avant l'injection, sortez la boîte du réfrigérateur et laissez la seringue préremplie atteindre la température ambiante pendant environ 15 minutes. Les médicaments parentéraux doivent être inspectés visuellement pour détecter la présence de particules ou une décoloration avant l'administration. Enflonsia ne doit pas être utilisé en cas de présence de particules ou d'une décoloration. Ne pas utiliser Enflonsia si la seringue préremplie est tombée ou est endommagée ou si le dispositif de sécurité sur la boîte a été brisé ou si la date de péremption est dépassée.
Reportez-vous à la Figure 1 pour les composants de la seringue préremplie.
Figure 1 : Composants de la seringue préremplie
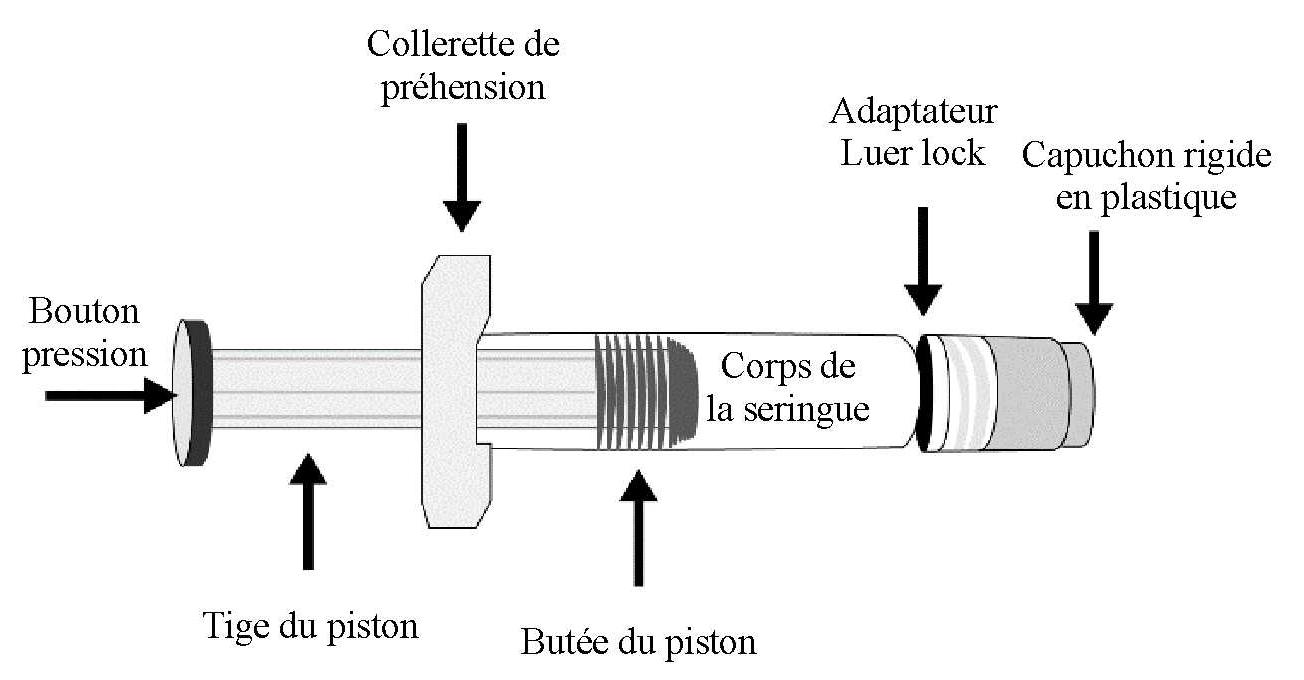
Étape 1 : Tenir le corps de la seringue d'une main et dévisser le capuchon en le tournant dans le sens inverse des aiguilles d'une montre avec l'autre main. Ne pas retirer l'adaptateur Luer lock ni la collerette de préhension.
Étape 2 : Fixer l'aiguille Luer lock stérile en la tournant dans le sens des aiguilles d'une montre jusqu'à ce qu'elle soit solidement attachée à la seringue.
Étape 3 : Injecter tout le contenu de la seringue préremplie par voie intramusculaire, dans la partie antérolatérale de la cuisse. Le médicament ne doit pas être injecté dans la zone du muscle fessier ni dans des zones où il pourrait y avoir un tronc nerveux important et/ou un vaisseau sanguin.
Enflonsia est à usage unique. Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
| PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|
Non remb Séc soc et non agréé Collect à la date du 15/04/2026.