Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- EFLUELDA
- EFLUELDA susp inj ser préremplie
Sommaire
Cip : 3400930305010
Modalités de conservation : Avant ouverture : 2° < t < 8° durant 12 mois (Conserver à l'abri de la lumière, Conserver dans son emballage, Conserver au réfrigérateur, Ne pas congeler)
| FORMES et PRÉSENTATIONS |
Suspension injectable.
EFLUELDA, après avoir été agité doucement, est un liquide opalescent, incolore.
Boîte contenant : 1 seringue préremplie de 0,5 mL de solution, munie d'un bouchon-piston et d'un capuchon de protection + aiguille séparée.
| COMPOSITION |
Virus de la grippe (inactivé, fragmenté) des souches suivantes* :
Pour une dose de 0,5 mL :
* cultivées sur œufs embryonnés de poules
** hémagglutinine
Ce vaccin est conforme aux recommandations de l'OMS (dans l'Hémisphère Nord) et à la décision de l'UE pour la saison 2025/2026.
EFLUELDA peut contenir des traces d'œuf, comme l'ovalbumine, et des traces de formaldéhyde, utilisés lors du procédé de fabrication (voir rubrique Contre-indications).
Solution de chlorure de sodium isotonique tamponnée au phosphate de sodium (chlorure de sodium, phosphate de sodium monobasique, phosphate de sodium dibasique, eau pour préparations injectables), octoxinol-9.
| INDICATIONS |
EFLUELDA est indiqué pour l'immunisation active des personnes âgées de 60 ans et plus en prévention de la grippe.
EFLUELDA doit être utilisé sur la base des recommandations officielles sur la vaccination contre la grippe.
| POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
| CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
| MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Hypersensibilité :
Comme pour tous les vaccins injectables, il est nécessaire de toujours disposer d'un traitement médical approprié et de surveiller le patient dans l'éventualité d'une réaction anaphylactique suite à l'administration du vaccin.
Précautions d'emploi :
EFLUELDA ne doit en aucun cas être administré par voie intravasculaire.
Maladie intercurrente :
La vaccination doit être différée chez les patients présentant une maladie fébrile aiguë jusqu'à résolution de la fièvre.
Syndrome de Guillain-Barré :
Si un syndrome de Guillain-Barré (SGB) est survenu dans les 6 semaines suivant une vaccination grippale antérieure, la décision d'administrer EFLUELDA doit se faire sur la base d'une évaluation minutieuse des bénéfices et risques potentiels.
Thrombocytopénie et troubles de la coagulation :
Comme avec les autres vaccins administrés par voie intramusculaire, ce vaccin doit être administré avec précaution chez les patients présentant une thrombocytopénie ou un trouble de la coagulation, car des saignements peuvent survenir suite à une administration intramusculaire chez ces personnes.
Syncope :
Une syncope (évanouissement), en réaction psychogène à l'injection avec une aiguille, peut survenir après, voire avant, toute vaccination. Des mesures doivent être mises en place pour prévenir toute blessure due à l'évanouissement et prendre en charge les réactions syncopales.
Immunodéficience :
La réponse en anticorps chez les patients présentant une immunodépression endogène ou iatrogène peut être insuffisante.
Protection :
Comme pour tout vaccin, une réponse protectrice peut ne pas être obtenue chez tous les sujets vaccinés.
Sodium :
Ce vaccin contient moins de 1 mmol (23 mg) de sodium par dose, c'est-à-dire qu'il est essentiellement « sans sodium ».
| INTERACTIONS |
Connectez-vous pour accéder à ce contenu
| FERTILITÉ/GROSSESSE/ALLAITEMENT |
EFLUELDA est uniquement indiqué chez les personnes âgées de 60 ans et plus.
EFLUELDA n'a pas été évalué cliniquement chez les femmes enceintes ou allaitantes.
Grossesse
Les vaccins grippaux inactivés à dose standard (15 microgrammes d'hémagglutinine de chaque souche virale par dose) peuvent être utilisés à tous les stades de la grossesse. Les données de sécurité disponibles sont plus importantes pour les deuxième et troisième trimestres de grossesse que pour le premier trimestre. Les données mondiales d'utilisation des vaccins grippaux inactivés à dose standard n'indiquent pas d'issues anormales pour le fœtus et la mère attribuables au vaccin. Cependant, les données sur l'utilisation chez les femmes enceintes de vaccins grippaux contenant 60 microgrammes d'hémagglutinine de chaque souche virale par dose sont limitées.
Allaitement
EFLUELDA peut être administré en cas d'allaitement. D'après l'expérience acquise avec les vaccins grippaux à dose standard, aucun effet chez les nourrissons allaités n'est attendu.
Fertilité
Les effets possibles d'EFLUELDA sur la fertilité humaine n'ont pas été étudiés.
| CONDUITE et UTILISATION DE MACHINES |
EFLUELDA n'a aucun effet ou un effet négligeable sur l'aptitude à conduire des véhicules et à utiliser des machines.
| EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
| SURDOSAGE |
Des cas d'administration d'une dose plus importante que la dose recommandée (surdosage) ont été rapportés avec EFLUELDA, lors d'utilisations accidentelles dans la population âgée de moins de 60 ans en raison d'une erreur médicamenteuse. Lorsque des effets indésirables étaient rapportés, ils correspondaient au profil de tolérance connu d'EFLUELDA (voir rubrique Effets indésirables).
| PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
| SÉCURITÉ PRÉCLINIQUE |
Les données non cliniques issues des études conventionnelles de tolérance locale et de toxicité à dose répétée n'ont pas révélé de risque particulier pour l'Homme.
Le potentiel cancérogène ou mutagène d'EFLUELDA et ses effets sur les fonctions de reproduction et de développement n'ont pas été évalués.
| INCOMPATIBILITÉS |
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
| DURÉE DE CONSERVATION |
12 mois.
| PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
A conserver au réfrigérateur (entre 2 °C et 8 °C). Ne pas congeler. Conserver la seringue dans l'emballage extérieur à l'abri de la lumière.
| PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
Le vaccin doit être amené à température ambiante avant utilisation.
Agiter avant emploi.
Le vaccin doit être inspecté visuellement pour détecter la présence de particules et/ou un changement de couleur avant administration chaque fois que la solution et le conditionnement le permettent. Le vaccin ne doit pas être utilisé si des particules ou un changement de couleur sont observés.
Préparation pour administration :
La seringue préremplie peut être fournie avec un Luer Lock et un capuchon de protection rigide (Figure A) ou souple (Figure D). La seringue contenant la suspension injectable doit être inspectée visuellement avant administration. En cas de présence de particules étrangères, de fuite, d'activation prématurée du piston ou d'embout défectueux, jetez la seringue préremplie.
Figure A : seringue Luer Lock avec un capuchon de protection rigide
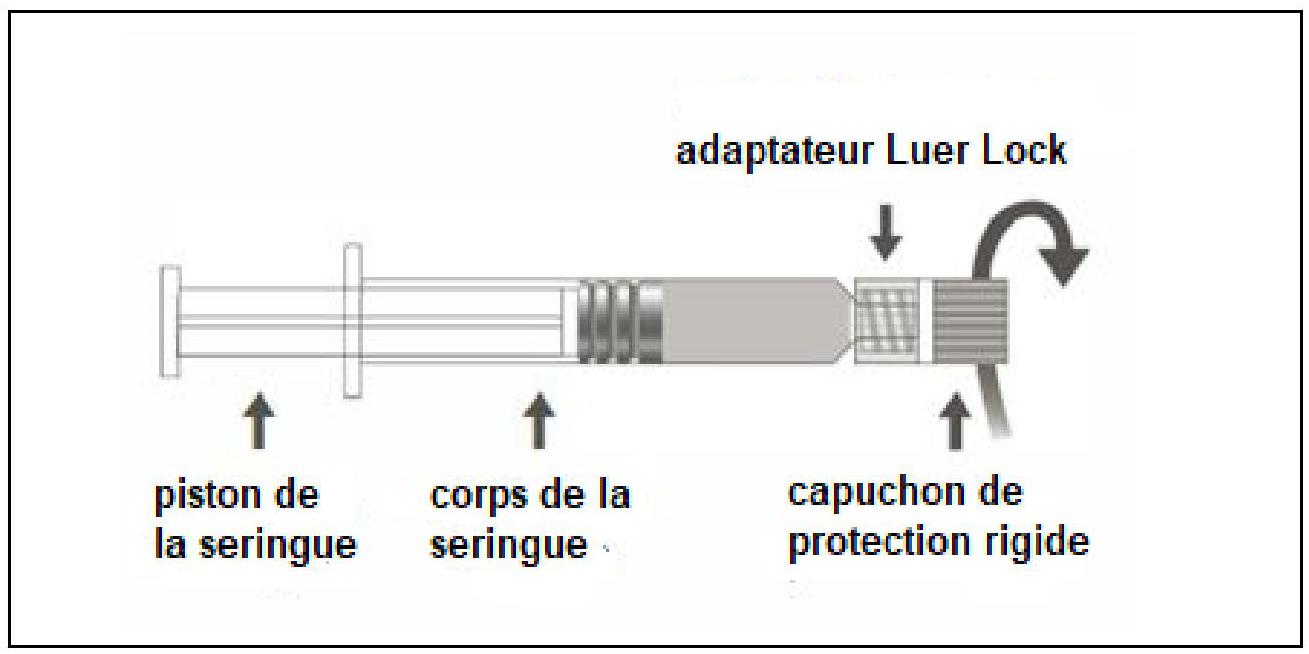
| Étape 1 : En tenant l'adaptateur Luer lock d'une main (éviter de tenir le piston ou le corps de la seringue), dévisser le capuchon de protection en le tournant. |
|
| Étape 2 : Pour fixer l'aiguille à la seringue, visser doucement l'aiguille à l'adaptateur Luer lock jusqu'à sentir une légère résistance. |
|
Figure D : seringue Luer Lock avec un capuchon de protection souple
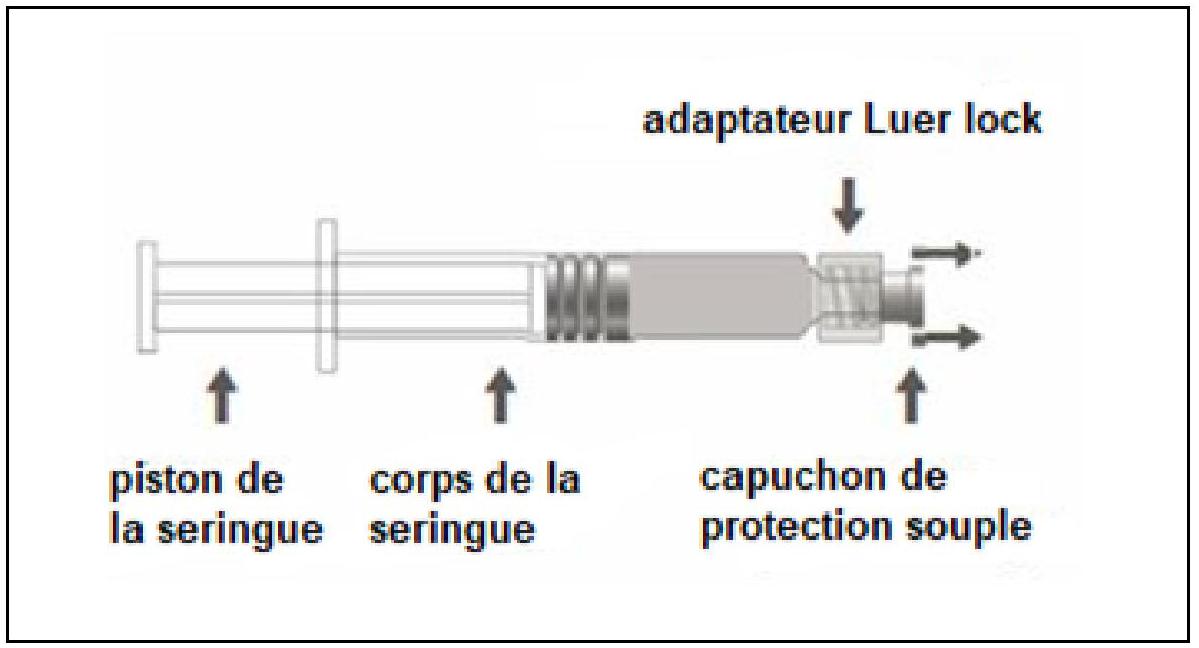
| Étape 1 : En tenant l'adaptateur Luer lock d'une main (éviter de tenir le piston ou le corps de la seringue), retirer le capuchon de protection souple. |
|
| Étape 2 : Pour fixer l'aiguille à la seringue, visser doucement l'aiguille à l'adaptateur Luer lock jusqu'à sentir une légère résistance |
|
La seringue est destinée à un usage unique et ne doit pas être réutilisée. Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
| PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|
| Prix : |
|
Remb Séc Soc à 65 % et agréé Collect dans la prévention de la grippe chez l’adulte de 65 ans et plus selon les recommandations vaccinales en vigueur (avis de la HAS du 6 février 2025 et du 10 avril 2025). Prise en charge à 100 % dans le cadre de la campagne de vaccination.



Vaccins contre la grippe saisonnière : la période de précommande prolongée d'un mois

Grippe saisonnière : prolongation de la campagne vaccinale jusqu'à fin février 2026