Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- ALBEY VENIN DE GUEPE POLISTES SP
- ALBEY VENIN DE GUEPE POLISTES SP 120 µg pdre/solv p sol inj
Sommaire
Cip : 3400930281604
| FORMES et PRÉSENTATIONS |
Poudre (blanche à légèrement jaunâtre) et solvant (solution incolore ; la présence d'agrégats ou de floculats peut être observée ; pH = 6,3-7,7) pour solution injectable.
Boîte contenant : 1 flacon de poudre + 1 flacon de 1,8 ml de solvant.
| COMPOSITION |
Venin de guêpe quantité correspondant en protéines à 120 microgrammes pour un flacon de poudre.
Chaque flacon contient 100 μg/ml de venin après reconstitution de la solution avec 1,2 ml de solvant.
Flacon de poudre : Mannitol
Solvant : Albumine humaine, chlorure de sodium, phénol, eau pour préparations injectables
| INDICATIONS |
ALBEY VENIN DE GUÊPE Polistes spp. 120 microgrammes est indiqué pour :
L'indication repose sur l'association des tests diagnostiques positifs et d'un historique de réactions systémiques sévères.
ALBEY VENIN DE GUÊPE Polistes spp. 120 microgrammes est indiqué chez les adultes, adolescents et enfants de plus de 2 ans. Le bénéfice/risque de l'immunothérapie allergénique aux venins d'hyménoptères doit être soigneusement évalué avant d'initier le traitement chez les enfants de 2 à 5 ans.
| POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
| CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
| MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Les réactions systémiques modérées survenues après piqûres d'hyménoptères, comme une urticaire ou un angio-oedème sans composante respiratoire, ne constituent pas des indications formelles de l'immunothérapie. Pour les patients ayant un facteur de risque associé en cas de piqûre d'hyménoptères ou dont la qualité de vie est gravement altérée par la crainte d'être piqués par une guêpe, le recours à l'immunothérapie peut toutefois être envisagé si les tests diagnostiques de dosage des IgE sont positifs.
Risque d'effets systémiques sévères :
Du fait du risque de réactions allergiques systémiques sévères pouvant mettre en jeu le pronostic vital, toute injection de ce médicament doit être réalisée sous la responsabilité d'un médecin expérimenté en immunothérapie allergénique et dans des conditions permettant la mise en place d'un traitement d'urgence (comprenant de l'adrénaline injectable pour la prise en charge d'un éventuel choc anaphylactique). Les patients doivent être informés des signes et symptômes associés nécessitant un avis médical immédiat. En cas de survenue de réaction systémique, la poursuite de l'immunothérapie allergénique devra être réévaluée par le médecin.
Patients asthmatiques :
Comme pour tout traitement d'immunothérapie allergénique, il est nécessaire de vérifier, avant chaque injection, que l'asthme est bien contrôlé.
En cas d'aggravation récente de l'asthme, appréciée par la clinique et/ou la mesure du Débit Expiratoire de Pointe (DEP) et/ou du Volume Expiratoire Mesuré durant la première Seconde (VEMS), le traitement doit être suspendu. Il ne sera repris qu'après amélioration et avis du médecin prescripteur.
Surveillance des patients à risques cardiovasculaire ou broncho-pulmonaire :
Du fait du risque majoré en cas de survenue de réaction systémique à l'injection, l'immunothérapie allergénique aux venins d'hyménoptères devra être réalisée sous surveillance stricte en milieu hospitalier chez les patients ayant des facteurs de risque associés tels que les pathologies cardiovasculaires et/ou broncho-pulmonaires. Ces pathologies sous-jacentes doivent être stabilisées avant l'initiation du traitement par immunothérapie allergénique aux venins d'hyménoptères
Mastocytose :
Le risque de survenue de réactions systémiques sévères est augmenté chez les patients présentant une mastocytose et/ou une tryptasémie élevée > 20 ng/ml. En outre, l'efficacité de l'immunothérapie allergénique aux venins d'hyménoptères peut être amoindrie dans ces situations comparativement à la population générale allergique. L'immunothérapie allergénique aux venins d'hyménoptères chez ces patients devra être réalisée sous surveillance stricte en milieu hospitalier.
Traitements concomitants :
En cas de nécessité absolue de maintien de ces traitements chez des patients chez qui une immunothérapie allergénique aux venins d'hyménoptères est envisagée, le rapport bénéfice/risque de l'indication de cette immunothérapie allergénique devra être soigneusement évalué et le traitement ne pourra être réalisé que sous surveillance stricte en milieu hospitalier.
Maladies néoplasiques, déficit immunitaire, immunodéficience, immunosuppression et maladie auto-immune en rémission :
En l'état actuel des connaissances les effets d'une immunothérapie allergénique aux venins d'hyménoptères chez les sujets ayant un cancer ou présentant un déficit immunitaire acquis ne sont pas clairement documentés.
Un traitement concomitant avec des agents immunosuppresseurs peut réduire l'efficacité de l'immunothérapie allergénique. De plus, la prudence est requise lors de la prescription d'une immunothérapie allergénique aux venins d'hyménoptères chez les sujets présentant une maladie auto-immune en rémission.
Par conséquent, le rapport bénéfice/risque de l'indication d'une immunothérapie allergénique aux venins d'hyménoptères devra être soigneusement pesé dans ces situations.
Excipients :
Ce médicament contient moins de 1 mmol (23 mg) de sodium par flacon, c'est-à-dire qu'il est essentiellement « sans sodium ».
| INTERACTIONS |
Connectez-vous pour accéder à ce contenu
| FERTILITÉ/GROSSESSE/ALLAITEMENT |
Grossesse
Aucune étude de reproduction n'a été conduite chez l'animal avec ALBEY VENIN DE GUÊPE Polistes spp.
Il n'existe pas d'étude épidémiologique de l'utilisation d'ALBEY VENIN DE GUÊPE Polistes spp. chez la femme enceinte.
La pratique des tests de diagnostic cutanés avec ALBEY VENIN DE GUÊPE Polistes spp. n'est pas recommandée pendant la grossesse afin de ne pas exposer la femme enceinte à un risque de réaction allergique générale.
Dans tous les cas, l'immunothérapie allergénique aux venins d'hyménoptères ne doit pas être initiée pendant la grossesse. Généralement, la survenue d'une grossesse pendant l'immunothérapie allergénique n'impose pas l'arrêt du traitement s'il est bien toléré. Néanmoins, le risque de réaction allergique systémique (choc anaphylactique) ne pouvant être exclu y compris en phase d'entretien, le médecin évaluera le bien-fondé de la poursuite de l'immunothérapie allergénique aux venins d'hyménoptères pendant la grossesse.
Allaitement
Il n'existe pas de données sur le passage d'ALBEY VENIN DE GUÊPE Polistes spp. dans le lait maternel.
Aucune étude n'a été menée chez l'animal pour étudier le passage d'ALBEY VENIN DE GUÊPE Polistes spp. dans le lait maternel.
Le médecin évaluera s'il y a lieu ou non d'interrompre le traitement avec ALBEY VENIN DE GUÊPE Polistes spp. au regard du bénéfice du traitement pour la mère.
Fertilité
Il n'a pas été conduit d'étude sur la fertilité avec ALBEY VENIN DE GUÊPE Polistes spp.
| CONDUITE et UTILISATION DE MACHINES |
ALBEY VENIN DE GUÊPE Polistes spp. n'a aucun effet ou un effet négligeable sur l'aptitude à conduire des véhicules et à utiliser des machines.
| EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
| SURDOSAGE |
Symptômes
Si une dose supérieure à la dose prescrite a été injectée, le risque et la gravité d'effets indésirables augmentent avec possibilité de réactions allergiques locales ou systémiques graves.
Voir effets indésirables en Effets indésirables.
Conduite à tenir :
Le traitement doit être adapté à l'état clinique du patient. Le patient devra rester sous surveillance médicale jusqu'à résolution complète des symptômes.
| PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
| PHARMACOCINÉTIQUE |
Connectez-vous pour accéder à ce contenu
| SÉCURITÉ PRÉCLINIQUE |
Aucune étude à long terme chez l'animal n'a été réalisée avec ALBEY VENIN DE GUÊPE Polistes spp. pour déterminer son potentiel cancérigène ou d'altération de la fertilité.
Des études de génotoxicité sur des cellules bactériennes n'ont montré aucun effet mutagène d'ALBEY VENIN DE GUÊPE Polistes spp.
| INCOMPATIBILITÉS |
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
| DURÉE DE CONSERVATION |
3 ans.
Après reconstitution et dilution, les durées maximales de conservation varient selon la concentration des solutions :
Concentration (μg/ml) |
Durée maximale de conservation |
100 |
28 jours |
inférieure à 100 |
A préparer le jour même |
| PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
Le produit avant et après reconstitution, ainsi que les dilutions, doivent être conservés au réfrigérateur (entre +2 °C et +8 °C).
Pour les conditions de conservation du médicament après reconstitution et dilution, voir la rubrique Durée de conservation.
| PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
Précautions à prendre pour la préparation, la manipulation et l'administration du médicament
Les schémas de reconstitution et de dilution sont présentés ci-dessous :
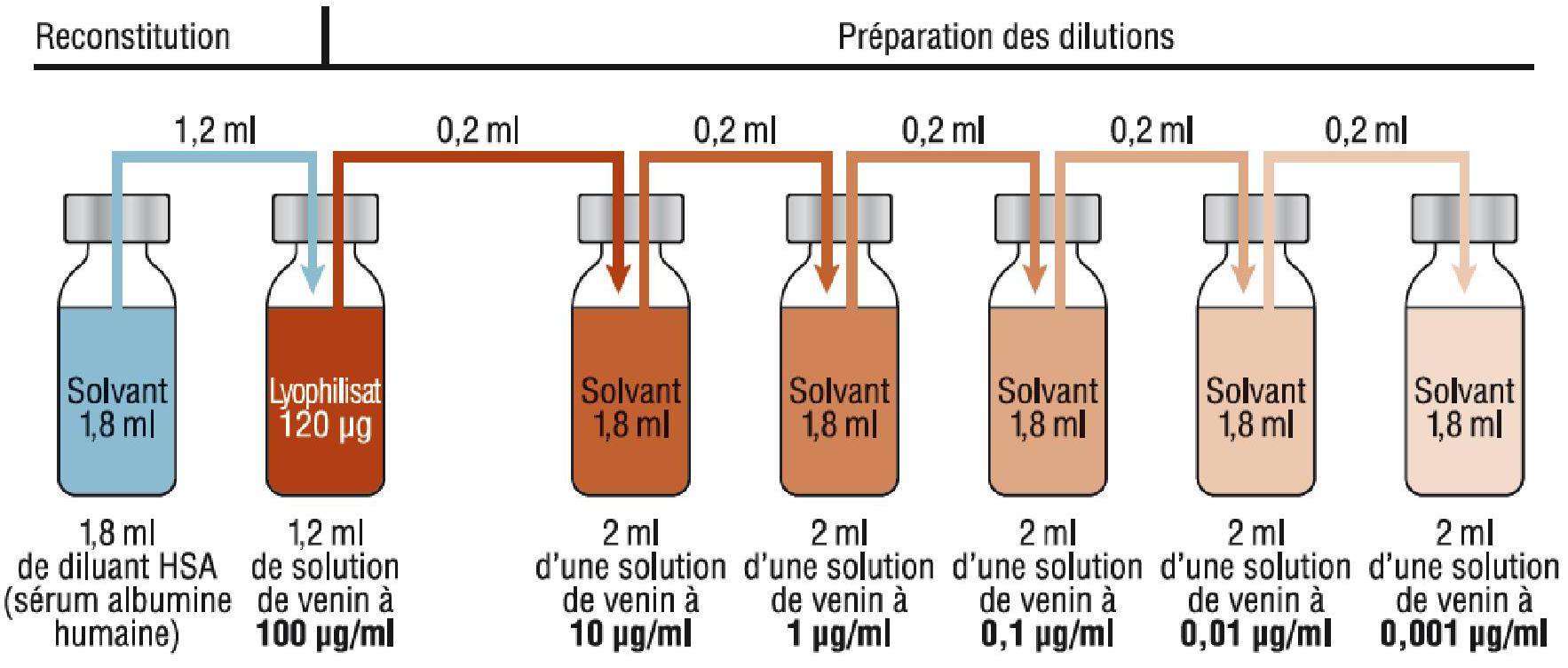
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
| PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|
| Prix : |
|