Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- AFQLIR
- AFQLIR 40 mg/ml sol inj ser préremplie
Sommaire
EEN avec dose seuil : polysorbate 20
Cip : 3400930306567
Modalités de conservation : Avant ouverture : 2° < t < 8° durant 36 mois (Conserver à l'abri de la lumière, Conserver dans son emballage, Conserver au réfrigérateur, Ne pas congeler)
Après ouverture : < 30° durant 14 jours (Conserver dans son emballage)
| FORMES et PRÉSENTATIONS |
Solution injectable (injection) (limpide, incolore à jaune légèrement brunâtre, iso-osmotique).
Seringue préremplie contenant 0,165 mL de solution, marquée par une ligne de dosage, munie d'un bouchon-piston et d'un adaptateur Luer Lock avec un capuchon à son extrémité. Boîte de 1.
| COMPOSITION |
1 mL de solution injectable contient 40 mg d'aflibercept*.
Chaque seringue préremplie contient 6,6 mg d'aflibercept dans 0,165 mL de solution. Ceci fournit la quantité nécessaire de produit pour délivrer une seule dose de 0,05 mL contenant 2 mg d'aflibercept.
* Protéine de fusion composée des fragments des domaines extracellulaires des récepteurs de type 1 et 2 du VEGF (facteur de croissance de l'endothélium vasculaire) humain fusionnés au fragment Fc de l'IgG1 humaine, produite dans des cellules ovariennes K1 de hamster chinois (CHO) par la technique de l'ADN recombinant.
Excipient à effet notoire
Chaque dose administrée de 0,05 mL contient 0,02 mg de polysorbate 20 (E 432).
Polysorbate 20 (E 432), histidine, monochlorhydrate monohydraté de L-histidine, tréhalose dihydraté, hydroxyde de sodium (pour l'ajustement du pH), acide chlorhydrique (pour l'ajustement du pH), eau pour préparation injectable.
| INDICATIONS |
Afqlir est indiqué chez l'adulte dans le traitement de :
| POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
| CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
| MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Réactions liées aux injections intravitréennes
Les injections intravitréennes, y compris celles d'aflibercept, ont été associées à des endophtalmies, des inflammations intraoculaires, des décollements de la rétine rhegmatogènes, des déchirures de la rétine et des cataractes traumatiques iatrogènes (voir rubrique Effets indésirables). Des techniques d'injection aseptiques appropriées doivent toujours être utilisées lors de l'administration d'Afqlir. De plus, les patients doivent être surveillés au cours de la semaine suivant l'injection pour permettre un traitement précoce en cas d'infection.
Les patients doivent être informés que tout symptôme évocateur d'une endophtalmie ou de l'un des événements mentionnés ci-dessus doit être signalé sans délai.
La seringue préremplie contient plus que la dose recommandée de 2 mg d'aflibercept (correspondant à 0,05 mL). Le volume excédentaire doit être expulsé avant l'administration (voir rubriques Posologie et mode d'administration et Elimination/Manipulation).
Des augmentations de la pression intraoculaire ont été observées dans les 60 minutes suivant des injections intravitréennes, y compris après injection d'aflibercept (voir rubrique Effets indésirables). Des précautions particulières sont nécessaires chez les patients présentant un glaucome mal contrôlé (ne pas injecter Afqlir tant que la pression intraoculaire est ≥ 30 mmHg). Dans tous les cas, la pression intraoculaire ainsi que la perfusion de la tête du nerf optique doivent donc être surveillées et prises en charge de manière appropriée.
Immunogénicité
Afqlir étant une protéine thérapeutique, il existe un risque d'immunogénicité (voir rubrique Effets indésirables). Les patients doivent être informés que tout signe ou symptôme d'inflammation intraoculaire doit être signalé, en particulier une douleur, une photophobie, ou une rougeur, qui peuvent être des signes cliniques liés à une hypersensibilité.
Effets systémiques
Des effets indésirables systémiques incluant des événements hémorragiques non oculaires et des événements thromboemboliques artériels ont été rapportés après injection intravitréenne d'inhibiteurs du VEGF. Il existe un risque théorique que ces événements soient liés à l'inhibition du VEGF. Les données concernant la sécurité du traitement sont limitées chez les patients présentant une OVCR, une OBVR, un OMD ou une NVC myopique et ayant des antécédents d'accident vasculaire cérébral ou d'accident ischémique transitoire ou d'infarctus du myocarde dans les 6 derniers mois. La prudence s'impose lors du traitement de ces patients.
Autre
Comme avec les autres traitements anti-VEGF intravitréens indiqués dans le traitement de la DMLA, de l'OVCR, de l'OBVR, de l'OMD et de la NVC myopique, il convient de prendre en compte les éléments suivants :
Populations chez lesquelles les données sont limitées
Les données concernant le traitement de patients présentant un OMD en lien avec un diabète de type I, ou de patients diabétiques dont le taux d'HbA1c est supérieur à 12 %, ou de patients présentant une rétinopathie diabétique proliférante, sont limitées. L'aflibercept n'a pas été étudié chez les patients présentant une infection systémique active, ou une pathologie oculaire associée comme un décollement de la rétine ou un trou maculaire. Il n'existe pas non plus de données concernant le traitement par l'aflibercept chez les patients diabétiques présentant une hypertension non contrôlée. Ce manque de données doit être pris en considération par le médecin au moment de traiter ces patients.
Dans le cadre de la NVC myopique, il n'y a aucune expérience concernant l'utilisation de l'aflibercept chez les patients non asiatiques, les patients précédemment traités pour la NVC myopique et les patients présentant des lésions extra-fovéolaires.
Informations concernant les excipients
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose, c'est-à-dire qu'il est essentiellement « sans sodium ».
Ce médicament contient 0,02 mg de polysorbate 20 dans chaque dose administrée de 0,05 mL (50 microlitres) de solution. Les polysorbates peuvent entraîner des réactions allergiques. Demander au patient s'il présente des allergies connues.
| INTERACTIONS |
Connectez-vous pour accéder à ce contenu
| FERTILITÉ/GROSSESSE/ALLAITEMENT |
Femmes en âge de procréer
Les femmes en âge de procréer doivent utiliser une contraception efficace pendant le traitement et pendant au moins 3 mois après la dernière injection intravitréenne d'aflibercept (voir rubrique Mises en garde et précautions d'emploi).
Grossesse
Il n'existe pas de données sur l'utilisation d'aflibercept chez la femme enceinte.
Les études menées chez l'animal ont mis en évidence une toxicité embryo-fœtale (voir rubrique Sécurité préclinique).
Même si l'exposition systémique après administration dans l'œil est très faible, Afqlir ne doit pas être utilisé pendant la grossesse à moins que le bénéfice attendu pour la mère ne l'emporte sur le risque potentiel pour le fœtus.
Allaitement
Basé sur des données humaines très limitées, de faibles quantités d'aflibercept peuvent être excrétées dans le lait maternel. L'aflibercept est une protéine de haut poids moléculaire et la quantité de médicament absorbée par le nourrisson devrait être limitée. Les effets de l'aflibercept sur un nouveau-né/nourrisson allaité sont inconnus.
Par mesure de précaution, l'allaitement n'est pas recommandé pendant l'utilisation d'Afqlir.
Fertilité
Les résultats des études menées chez l'animal avec une exposition systémique élevée indiquent que l'aflibercept peut altérer la fertilité chez le mâle et la femelle (voir rubrique Sécurité préclinique). De tels effets ne sont pas attendus suite à une administration intraoculaire avec une exposition systémique très faible.
| CONDUITE et UTILISATION DE MACHINES |
Le traitement par Afqlir a une influence mineure sur l'aptitude à conduire des véhicules ou à utiliser des machines du fait de possibles troubles visuels temporaires associés soit à l'injection soit à l'examen de l'œil. Les patients ne doivent pas conduire ou utiliser de machines tant qu'ils n'ont pas récupéré une fonction visuelle suffisante.
| EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
| SURDOSAGE |
Dans les essais cliniques, des doses allant jusqu'à 4 mg ont été administrées à intervalles mensuels et des cas isolés de surdosage à 8 mg ont été observés.
Un surdosage par injection d'un volume trop important peut entraîner une augmentation de la pression intraoculaire. Par conséquent, en cas de surdosage, la pression intraoculaire doit être surveillée et, si cela est jugé nécessaire par le médecin ayant procédé à l'injection, un traitement adéquat doit être instauré (voir rubrique Elimination/Manipulation).
| PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
| PHARMACOCINÉTIQUE |
Connectez-vous pour accéder à ce contenu
| SÉCURITÉ PRÉCLINIQUE |
Dans les études de toxicité à doses répétées chez l'animal, des effets n'ont été observés qu'à des niveaux d'exposition systémique considérés comme nettement supérieurs à l'exposition maximale observée chez l'homme après une administration intravitréenne à la dose clinique prévue. Ces effets ont de ce fait peu de pertinence clinique.
Des érosions et des ulcérations de l'épithélium respiratoire dans les cornets nasaux chez les singes traités par aflibercept par voie intravitréenne ont été observées à des expositions systémiques supérieures à l'exposition maximale observée chez l'homme. L'exposition systémique pour l'aflibercept libre, basée sur la Cmax et l'ASC, était respectivement d'environ 200 et 700 fois supérieure aux valeurs correspondantes observées chez l'être humain après une injection intravitréenne de 2 mg. À la dose sans effet indésirable observé (NOAEL) de 0,5 mg/œil chez le singe, l'exposition systémique basée sur la Cmax et l'ASC était respectivement de 42 et 56 fois supérieure.
Aucune étude n'a été menée sur le potentiel mutagène ou cancérogène de l'aflibercept.
Un effet de l'aflibercept sur le développement intra-utérin a été mis en évidence dans les études sur le développement embryo-fœtal menées sur des lapines en gestation après administration intraveineuse (3 à 60 mg/kg) et sous-cutanée (0,1 à 1 mg/kg). La NOAEL maternelle était respectivement de 3 mg/kg ou 1 mg/kg. La NOAEL concernant le développement n'a pas été déterminée. À la dose de 0,1 mg/kg, l'exposition systémique basée sur la Cmax et l'ASC cumulée pour l'aflibercept libre était respectivement environ 17 et 10 fois supérieure par rapport aux valeurs correspondantes observées chez l'homme après une injection intravitréenne de 2 mg.
Les effets sur la fertilité chez le mâle et la femelle ont été évalués au cours de l'étude sur 6 mois chez le singe recevant une administration intraveineuse d'aflibercept à des doses allant de 3 à 30 mg/kg. Une absence ou une irrégularité des menstruations associée à des altérations des niveaux d'hormones reproductives femelles et des modifications dans la morphologie et la mobilité des spermatozoïdes ont été observées à toutes les doses testées. En se basant sur la Cmax et l'ASC pour l'aflibercept libre observées à une dose intraveineuse de 3 mg/kg, les expositions systémiques étaient respectivement environ 4 900 et 1 500 fois supérieures par rapport à l'exposition observée chez l'homme après une dose intravitréenne de 2 mg. Toutes les modifications étaient réversibles.
| INCOMPATIBILITÉS |
En l'absence d'études de compatibilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
| DURÉE DE CONSERVATION |
3 ans
| PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
A conserver au réfrigérateur (entre 2 °C et 8 °C).
Ne pas congeler.
Conserver dans l'emballage d'origine afin de protéger de la lumière.
Le blister non ouvert peut être conservé à l'extérieur du réfrigérateur en dessous de 30 °C pendant 7 jours maximum. Après l'ouverture du blister, respecter des conditions d'asepsie.
| PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
La seringue préremplie est à usage unique exclusivement pour le traitement d'un seul œil. Le fait d'extraire plusieurs doses à partir d'une même seringue préremplie pourrait augmenter le risque de contamination et d'infection ultérieure.
La seringue préremplie contient plus que la dose recommandée de 2 mg d'aflibercept (correspondant à 0,05 mL).
Mode d'emploi de la seringue préremplie :
Conservation et inspection
|
|
Conserver Afqlir au réfrigérateur entre 2 °C et 8 °C ; ne pas congeler. Conserver la seringue préremplie dans l'emballage extérieur à l'abri de la lumière. |
||||||
|
|
Avant l'utilisation, le blister non ouvert d'Afqlir peut être conservé à une température inférieure à 30 °C pendant 7 jours maximum. Après l'ouverture du blister, respecter des conditions d'asepsie. |
||||||
|
|
Afqlir est une solution limpide et incolore à légèrement jaune-brunâtre. |
||||||
| La solution doit être inspectée visuellement afin de détecter la présence de particules étrangères, d'une turbidité et/ou d'un changement de coloration ou de son aspect physique avant son administration. Dans l'un ou l'autre de ces cas, jeter le médicament. |
|||||||
|
|
|||||||
Préparation et administration
Chaque seringue préremplie doit uniquement être utilisée pour le traitement d'un seul œil.
Ne pas ouvrir le blister stérile contenant la seringue préremplie en dehors de la salle d'administration prévue à cet effet.
Pour l'injection intravitréenne, une aiguille d'injection de 30 G x 13 mm doit être utilisée.
Utiliser une technique aseptique pour effectuer les étapes suivantes.
Description de la seringue préremplie
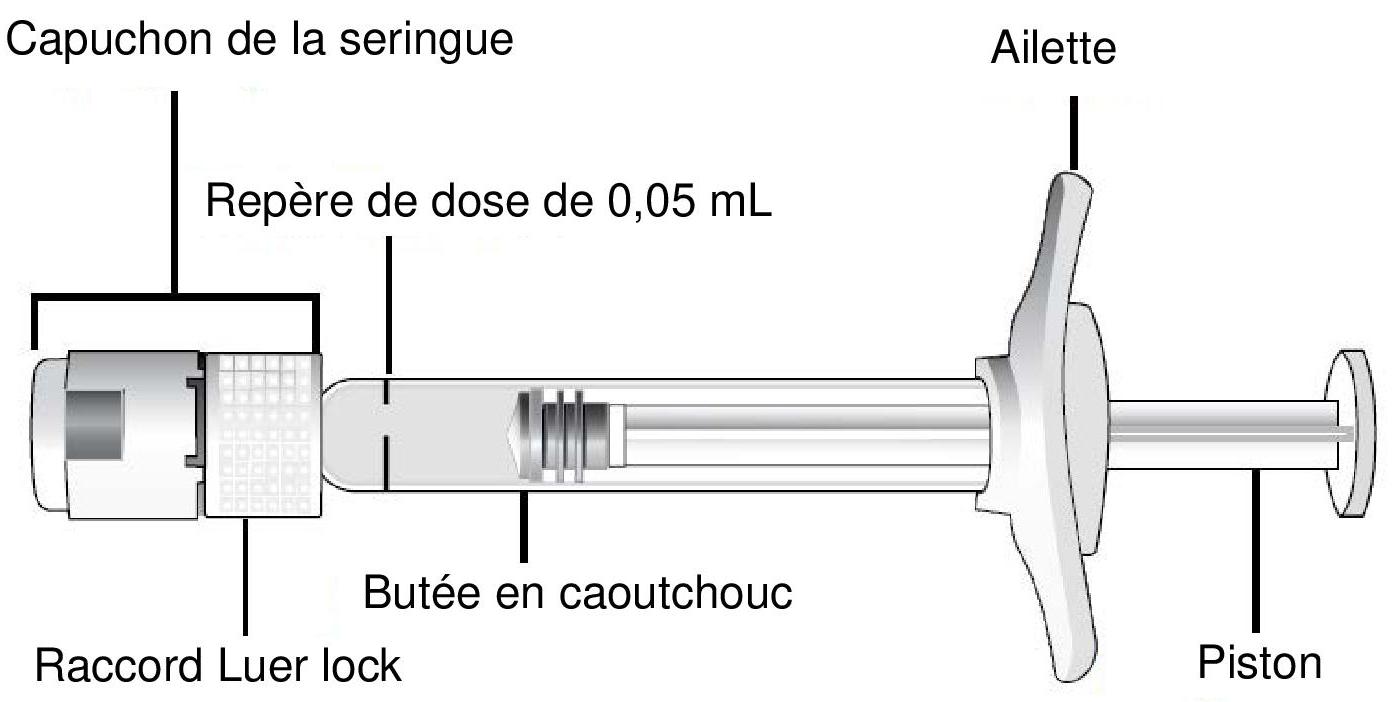
| 1 |
Dès que tout est prêt pour l'administration d'Afqlir, ouvrir l'emballage extérieur et en retirer le blister stérilisé. Ouvrir délicatement le blister en garantissant la stérilité de son contenu. Conserver la seringue sur le plateau stérile jusqu'au moment de l'assemblage. |
|
| 2 |
Retirer de manière aseptique la seringue du blister stérilisé. |
|
| 3 |
|
Pour retirer le capuchon de la seringue, maintenir la seringue d'une main tout en utilisant l'autre main pour saisir le capuchon de la seringue entre le pouce et l'index. Casser le capuchon (sans le faire tourner ni le tordre). |
| 4 |
|
Fixer fermement, de manière aseptique, une aiguille d'injection de 30 G x 13 mm sur l'extrémité Luer Lock de la seringue par un mouvement de rotation. |
| 5 |
|
En tenant la seringue avec l'aiguille dirigée vers le haut, vérifier l'absence de bulles d'air dans la seringue. |
| 6 |
|
Éliminer toutes les bulles et expulser l'excédent de médicament en appuyant lentement sur le piston pour aligner le bord du dôme du piston avec la ligne de dosage noire sur la seringue (équivalant à 50 microlitres). |
| 7 |
Injecter lentement jusqu'à ce que la butée en caoutchouc atteigne l'extrémité de la seringue pour administrer le volume de 0,05 mL. Confirmer l'administration de la totalité de la dose en vérifiant que la butée en caoutchouc a atteint la fin du cylindre de la seringue. |
|
| 8 |
La seringue préremplie est à usage unique exclusivement. L'extraction de doses multiples à partir d'une seringue préremplie peut augmenter le risque de contamination et d'infection consécutive. |
| PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|
| Prix : |
|
traitement de la forme néovasculaire (humide) rétrofovéolaire de la dégénérescence maculaire liée à l'âge (DMLA) chez l'adulte.
Le traitement par AFQLIR doit uniquement être administré par injection intravitréenne et par des ophtalmologistes expérimentés dans ce type d'injection ;
traitement de la baisse d'acuité visuelle due à l'œdème maculaire secondaire à une occlusion de la veine centrale de la rétine (OVCR) chez l'adulte ;
traitement de la baisse d'acuité visuelle due à l'œdème maculaire diabétique, en cas de forme diffuse ou de fuites proches du centre de la macula, chez les patients adultes ayant une baisse d'acuité visuelle inférieure ou égale à 5/10 et chez lesquels la prise en charge du diabète a été optimisée ;
traitement chez l'adulte de la baisse d'acuité visuelle due à une néovascularisation choroïdienne (NVC) myopique ;
traitement de la baisse d'acuité visuelle due à l'œdème maculaire secondaire à une occlusion de branche veineuse rétinienne (OBVR) chez l'adulte.


Biomédicaments et substitution à l'officine : ajout du groupe aflibercept