Contenu médical destiné aux professionnels de santé.
Thrombopénies et thromboses induites par l’héparine
Particularités chez le patient hémodialysé
Physiopathologie générale, manifestations biocliniques, et diagnostic
Professeur Yves Gruel, Université de Tours, France.
Les thrombopénies induites par l’héparine (TIH) sont une entité clinico-biologique qui sont associées, qu’elles soient classiques ou atypiques, à un état prothrombotique le plus souvent sévère conduisant à des manifestations thrombotiques pouvant mettre en jeu le pronostic vital du patient. Les TIH sont dues au développement d’anticorps dirigés le plus souvent contre le FP4 complexé à l’héparine, activant les plaquettes ainsi que d’autres cellules sanguines, et les rendant ainsi procoagulantes. Les TIH sont assez rares chez les patients hémodialysés mais néanmoins possibles et parfois plus difficiles à diagnostiquer.
Physiopathologie générale
Les TIH sont dues essentiellement à des anticorps spécifiques du facteur plaquettaire 4 (FP4), chimiokine présente dans les granules alpha plaquettaires, et qui possède un anneau de charges positives à sa surface, sur lequel peuvent se fixer des structures électronégatives (1). Parmi elles, on peut citer les glycosaminoglycanes naturels à la surface des cellules sanguines, ou thérapeutiques, comme les héparines, mais aussi certaines bactéries, l’ADN/l’ARN et la capside de certains virus.
Ces structures électronégatives peuvent modifier la conformation du FP4 et induire ainsi une réponse immunitaire atypique conduisant à la synthèse d’anticorps anti-FP4.
La pathogénicité de ces anticorps dépendra de leur capacité à activer les cellules sanguines via la liaison de leur fragment Fc aux récepteurs FcγR exprimés à leur surface. Parmi eux, FcγRIIA (CD32) joue un rôle central.
L’activation plaquettaire et cellulaire ainsi induite conduit à un état d’hypercoagulabilité majeur et des thromboses, caractéristiques biocliniques essentielles des TIH.
- TIH classiques
Les TIH sont la conséquence d’une réponse immunitaire atypique associée à la synthèse, sans switch isotypique, et donc à l’apparition simultanée d’anticorps IgM, IgA et IgG spécifiques du FP4 modifié par l’héparine (H) (1). Tous les patients traités par l’héparine ne développent pas d’anticorps anti-FP4/H, et seule une minorité de ceux synthétisant ces anticorps deviennent symptomatiques avec une TIH.
Plusieurs facteurs de risque d’immunisation anti-FP4 et de TIH ont en fait été identifiés. Certains sont dépendants du traitement lui-même, puisque parmi les héparines et dérivés, seules les héparines non fractionnées (HNF), très électro-négatives, se fixent avec une forte affinité au niveau d’un anneau de charges positives exprimé par le tétramère de FP4, entrainant des changements conformationnels exposant des épitopes aux pôles de la protéine, expliquant le développement beaucoup plus fréquent d’anticorps anti-FP4 sous HNF que sous HBPM.
La réponse immunitaire vis à- vis des complexes FP4/H dépend aussi du contexte clinique justifiant le traitement héparinique. Ainsi, l’incidence des TIH est-elle plus élevée chez les patients avec des concentrations circulantes de FP4 élevées, comme ceux ayant subi une chirurgie cardiaque ou prothétique, notamment orthopédique (PTH ou PTG).
Enfin, une concentration plasmatique élevée en IgG anti-FP4/H est également un facteur de risque notable de TIH car leur pathogénicité est plus importante.
Celle-ci repose en effet sur l’interaction des IgG anti-FP4/H avec les récepteurs FcγRIIA des plaquettes, qui entraine leur activation et la libération de microparticules procoagulantes (Figure 1). Cet effet des anticorps est typiquement héparine-dépendant, et n’est observé qu’à des concentrations thérapeutiques ou supra-thérapeutiques d’héparine, mais non en absence ou en excès d’héparine.
Les leucocytes contribuent également à l’hypercoagulabilité des TIH. En effet, les monocytes activés synthétisent de grandes quantités de facteur tissulaire (FT), et libèrent eux aussi des microparticules procoagulantes, favorisant une génération explosive de thrombine (2). Les polynucléaires neutrophiles (PNNs) activés libèrent le contenu de leurs granules et forment des NETs ou « Neutrophil Extracellular Traps » (3).
Ces NETs :
- activent les plaquettes,
- régulent négativement les inhibiteurs physiologiques de la coagulation,
- forment une matrice propice à la formation de fibrine,
- et sont donc aussi pro-thrombotiques.
Les anticorps de TIH activent également les cellules endothéliales, bien que celles-ci n’expriment pas de récepteurs FcγR. En effet, le FP4 libéré par les plaquettes se fixe à l’endothélium vasculaire, qui en libérant du facteur Willebrand forme aussi des complexes antigéniques avec le FP4 (4), devenant ainsi une aire privilégiée de liaison des anticorps de TIH.
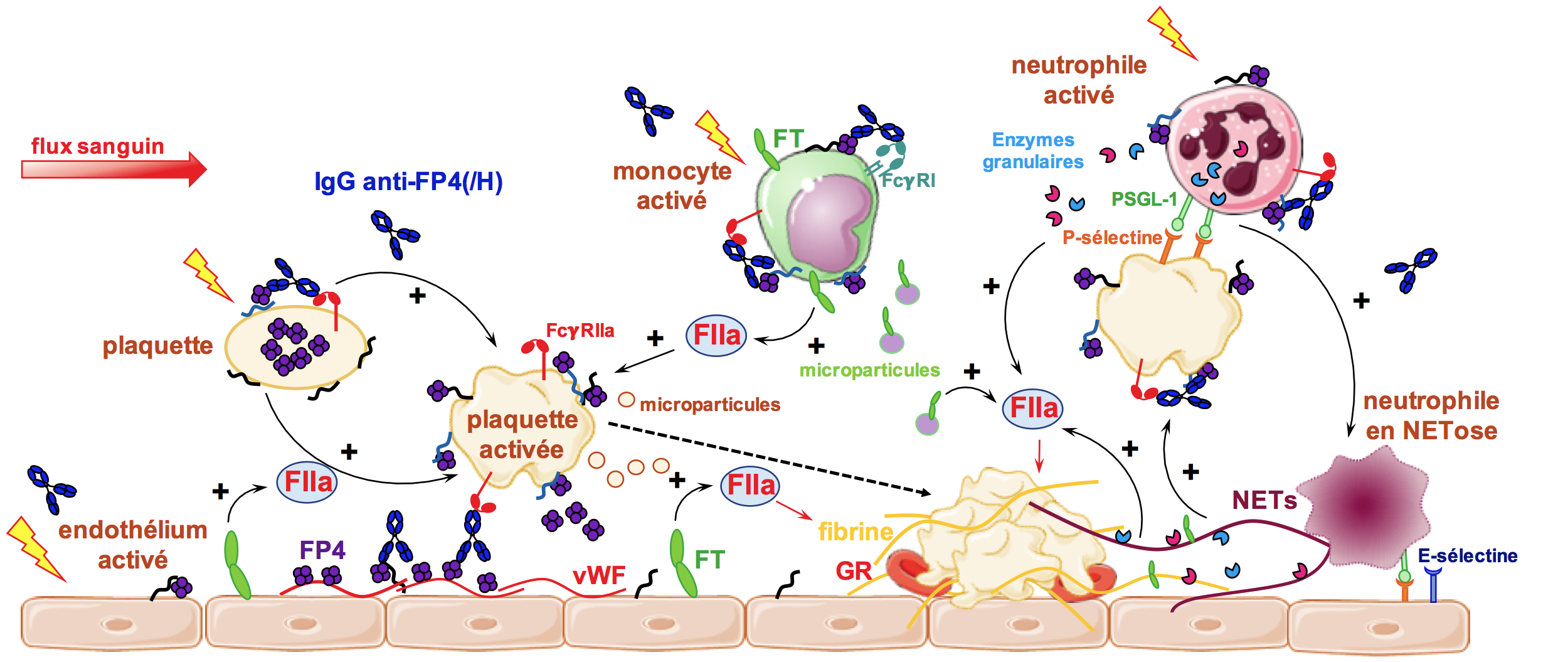
Figure 1 : Physiopathologie des thrombopénies induites par l’héparine.
Les anticorps anti-FP4(/H) induisent une activation multicellulaire, une hypercoagulabilité et des thromboses. FIIa: facteur II activé (thrombine), FP4: facteur plaquettaire 4, FT: facteur tissulaire, GR: globule rouge, NETs: neutrophil extracellular traps, PSGL-1: P-selectin ligand 1, vWF: facteur Willebrand.
- TIH auto-immunes ou atypiques
Comme évoqué précédemment, l’anneau de charges positives présent à la surface du FP4 explique son interaction avec des molécules chargées négativement, comme l’héparine. Mais, plus rarement, une immunisation anti-FP4 peut survenir sans exposition préalable à l’héparine, car d’autres molécules peuvent modifier la structure du FP4 et augmenter son immunogénicité (5).
Un syndrome inflammatoire majeur, associé à des concentrations circulantes élevées de FP4, semble jouer un rôle déterminant dans la physiopathologie des TIH auto-immunes. La libération de polyanions (ADN, GAGs) associée à des lésions tissulaires étendues au décours de certains actes traumatisants, comme une chirurgie orthopédique, pourrait aussi favoriser la formation de grandes quantités de complexes antigéniques FP4/polyanions, particulièrement immunogènes.
Les travaux d’Andreas Greinacher ont montré que le plasma des patients atteints de TIH auto-immune comportait deux types d’anticorps :
- des IgG anti-FP4/Héparine classiques
- mais aussi d’anticorps, capables de reconnaître avec une grande affinité le FP4 natif (anti-FP4) non complexé à l’héparine, et d’activer très fortement les plaquettes (6).
Particularités physiopathologiques chez l’hémodialysé
La dialyse est de fait un contexte à la fois pro-thrombotique et inflammatoire, qui associé à une exposition ré pétée à l’héparine, majore le risque d’immunisation anti-FP4 (30) et de TIH. Le contact du sang avec le circuit de dialyse active les plaquettes, avec une libération accrue de FP4, dont le taux circulant augmente, favorisant la formation des complexes FP4/héparine immunogènes, avec la synthèse d’anticorps IgG potentiellement pathogènes.
Le circuit de dialyse peut activer aussi le complément et induire une consommation plaquettaire non immunologique, masquant ou simulant une TIH et rendant l’interprétation d’une chute plaquettaire plus difficile.
Certaines comorbidités relativement fréquentes chez l’hémodialysé, comme le diabète, l’athérosclérose, ou des antécédents thrombotiques sont des facteurs de sévérité clinique lors d’une TIH.
Manifestations clinico-biologiques des TIH
- TIH classique
La TIH classique est un syndrome clinico-biologique caractérisé par une chute de plus de 50% de la numération plaquettaire (NP), survenant le plus souvent entre le 5e et 10e jour d’un traitement héparinique. La thrombopénie est généralement modérée, rarement < 50 G/L, et constitue fréquemment le premier signe d’appel.
Cette thrombopénie témoigne d’une activation multicellulaire qui conduit à des thromboses chez 30 à 50% des patients, pouvant précéder ou être contemporaines de la chute des plaquettes chez près de la moitié des patients (7).
Bien que la TIH soit souvent observée dans les 10 premiers jours d’héparinothérapie, elle peut être plus tardive sous HBPM, pouvant survenir plus de 3 semaines après la première injection (8). Exceptionnellement, elle peut apparaître précocement, dans les 24 premières heures, en lien avec une exposition antérieure à l’héparine < 3 mois, et la présence d’une immunisation anti-FP4 préexistante.
La thrombopénie est parfois absente, notamment si la NP est initialement élevée. Une TIH doit donc toujours être envisagée devant une chute relative de la NP ≥ 40% par rapport à une valeur précédente, le plus souvent mesurée avant l’héparinothérapie.
Des thromboses veineuses profondes (TVP) touchant le plus souvent les membres inférieurs ou des embolies pulmonaires (EP) sont les manifestations cliniques les plus fréquentes, mais des atteintes artérielles (ischémie aigue des membres inférieurs, accident vasculaire cérébral, infarctus du myocarde) sont possibles, et plus fréquentes après chirurgie cardiaque (9).
La présence de thromboses dans ~40 % des TIH, de localisation veineuse dans plus de ¾ des cas, justifie en cas de suspicion : un écho‑doppler veineux systématique des membres inférieurs (10).
Des manifestations dites atypiques, bien que rares, doivent être connues :
- saignements sévères (souvent en lien avec une CIVD),
- lésions cutanées au site d’injection, avec un caractère très évocateur pour les nécroses cutanées (11, 12),
- très rarement : hypotension, détresse respiratoire, état de choc dans les 30 minutes suivant une injection IV d’HNF, notamment en hémodialyse (13).
L’ensemble de ces complications contribue à la mortalité des TIH, aujourd’hui estimée à environ 5 %, en nette diminution grâce à un diagnostic plus précoce et une meilleure prise en charge au cours des 15 dernières années (9).
Particularités CLINIQUES des TIH chez L’HEMODIALYSE
Sur le plan clinique, en dehors de ces complications systémiques rares, la chute de la NP moins évidente à identifier chez ces patients. On observe également des complications thrombotiques veineuses ou plus rarement artérielles, sans particularités par rapport aux patients non dialysés.
Cependant, des évènements plus spécifiques aux hémodialysés sont possibles et parfois révélateurs d’une TIH. Il peut s’agir d’une thrombose ou de la formation anormale de caillots au niveau du circuit de dialyse, cette complication étant volontiers récidivante. Il peut aussi s’agir d’une dysfonction de la fistule artério-veineuse, témoignant de la présence de thrombi obstructifs.
Tous ces évènements inattendus doivent inciter à contrôler la numération plaquettaire et à rechercher des anticorps anti-FP4/héparine après avoir contacté le biologiste responsable des analyses spécifiques. Ces analyses peuvent nécessiter l’implication d’un centre expert.
- TIH auto-immune
En 2017, le concept de TIH auto-immune a été bien défini par A Greinacher et al. (5). Il regroupe des TIH atypiques, tant sur le plan clinique que biologique.
Ces TIH peuvent être « spontanées », survenant à distance de toute héparinothérapie, ou être induites par des flushs d’héparine. Elles peuvent également être retardées, apparaître ou persister après l’arrêt de l’héparine, et sont parfois observées sous fondaparinux (14).
Sur le plan biologique, ces TIH sont caractérisées par la présence d’anticorps anti-FP4 atypiques, capables de se fixer au FP4 natif (non modifié par l’héparine) avec une forte affinité, et d’activer puissamment les plaquettes.
Peu de cas de TIH auto-immunes spontanées ont été décrits, mais la presque totalité étaient associées à un syndrome inflammatoire majeur, souvent dans un contexte de chirurgie orthopédique (15). De très rares cas de thrombopénies sous fondaparinux - ce dernier ne formant pas de complexes antigéniques avec le FP4 in vitro - ont aussi été rapportés (16).
Enfin, le terme de TIH retardée désigne une forme rare de TIH survenant alors que l’héparine a été arrêtée depuis plusieurs jours (17).
Les caractères cliniques et biologiques de ces TIH atypiques restent peu étudiées car elles sont rares, mais elles apparaissent néanmoins associées à un tableau clinique plus sévère avec un taux de mortalité 5 fois supérieur à celui des autres formes de TIH (18). Les évènements thrombotiques des TIH auto-immunes sont de fait souvent atypiques et sévères avec une atteinte neurologique fréquente, se traduisant par des accidents vasculaires cérébraux ischémiques ou des thromboses veineuses cérébrales (TVC) (19), et compliquée dans près d’un quart des cas par une CIVD.
Tableau 1 : comparaison TIH classique / TIH auto-immune
|
|
TIH classique |
TIH auto‑immune |
|
Temporalité |
Survient entre J5 et J10 après un traitement héparinique. Peut-être plus tardive sous HBPM (> 3 semaines). Peut-être précoce (< 24 h) en cas d’exposition récente à l’héparine et d’immunisation préexistante. |
Peut-être spontanée, sans héparine. Peut survenir après des flushs d’héparine, être retardée et apparaître/persister après l’arrêt de l’héparine. Peut être observée sous fondaparinux. |
|
Nature des anticorps |
IgG anti‑FP4/héparine « classiques ». |
Anticorps anti‑FP4 atypiques capables de reconnaître le FP4 natif (non complexé à l’héparine) et d’activer puissamment les plaquettes. |
|
Contexte clinique favorisant |
Héparinothérapie (HNF ou HBPM), favorisé par un contexte inflammatoire. |
Syndrome inflammatoire majeur, souvent en lien avec une chirurgie orthopédique ou un contexte traumatique. |
|
Thrombopénie |
Fréquente, généralement modérée, rarement < 50 G/L. Peut être absente si NP initiale élevée → diagnostique basé sur une chute relative ≥ 40 %. |
Peut être présente mais parfois atypique ; dépend du contexte inflammatoire et du type d’anticorps. |
|
Thromboses |
Très fréquentes (30–50 %). Principalement veineuses : TVP, EP. Possibles thromboses artérielles : ischémie, AVC, IDM — plus fréquentes après chirurgie cardiaque. |
Souvent atypiques et sévères, avec atteinte neurologique fréquente : AVC ischémique, thrombose veineuse cérébrale (TVC). Association à une CIVD dans ~25 % des cas. |
|
Lien avec l’héparine |
Toujours lié à l’héparine (exposition en cours ou récente). |
Peut survenir sans héparine. Peut apparaître sous fondaparinux, malgré l’absence de complexes FP4/fondaparinux in vitro. |
|
Gravité / mortalité |
Mortalité environ 5 % (en baisse grâce au diagnostic précoce). |
Forme plus sévère, avec une mortalité ×5 par rapport à la TIH classique. |
DEPISTAGE ET Diagnostic d’une TIH
- TIH classiques
Le dépistage d’une TIH repose essentiellement sur la surveillance de la NP. Sous héparine, les modalités de surveillance dépendent donc du risque de TIH, stratifié en 3 niveaux (élevé, intermédiaire ou faible). Ce risque dépend du type d’héparine injectée chez le patient, du contexte clinique et de la durée du traitement. Il est le plus élevé sous HNF (≥1%), sauf en cas de traitement prophylactique prescrit dans un contexte médical ou obstétrical (risque intermédiaire entre 0,1 et 1 %).
Une héparinothérapie après chirurgie cardiaque avec circulation extra-corporelle (CEC), ou lors d’une assistance circulatoire de type extracorporeal membrane oxygenation (ECMO) ou d’une épuration extra-rénale (EER) avec administration d’HNF, est le contexte à risque le plus élevé de TIH. Les recommandations en vigueur (8) pour la surveillance de la NP dépendent donc de ces 2 éléments (type-posologie d’héparine et contexte clinique) et sont résumées dans la table 2.
Tableau 2 : Rythme de surveillance de la numération plaquettaire selon le risque de TIH
|
Patients |
Schéma |
Probabilité clinique de TIH |
Surveillance de la numération plaquettaire |
|
|
HNF |
Chirurgicaux y compris césarienne |
Prophylactique |
Élevée |
2 fois par semaine entre le 4ème et 14ème jour
puis 1 fois par semaine si le traitement est poursuivi, avec une durée totale de suivi d’un mois |
|
Curatif |
||||
|
Médicaux/ Obstétrique |
Curatif |
|||
|
CEC, EER, Assistances |
- |
|||
|
Médicaux/ Obstétrique |
Prophylactique |
Intermédiaire |
1 à 2 fois par semaine entre le 4ème et 14ème jour
puis 1 fois par semaine si le traitement est poursuivi, avec une durée totale de suivi d’un mois |
|
|
HBPM |
Chirurgicaux y compris césarienne |
Prophylactique |
||
|
Curatif |
||||
|
Cancéreux |
- |
|||
|
Médicaux/ Obstétrique |
Prophylactique |
Faible |
Aucune |
|
|
Curatif |
||||
|
Fondaparinux |
Toutes indications |
|||
Particularités relatives au risque et au dépistage de la TIH chez l’hémodialysé
Le risque de TIH sous hémodialyse est variable selon les séries publiées et le type d’héparine utilisée. Il est en pratique jugé assez faible (entre 0,1 et 1%) sous HBPM (20), mais non négligeable voire élevé avec l’HNF (>1%) et possiblement sous-estimé (29) car une thrombopénie est fréquente en dialyse et les variations de la numération plaquettaire sont parfois attribuées à la procédure d’épuration extra-rénale elle-même.
Le dépistage d’une TIH chez l’hémodialysé est plus difficile car la NP est souvent basse chez ces patients, varie assez souvent de façon significative entre les séances, et la chronologie des évènements, notamment de la diminution du nombre des plaquettes permettant de suspecter une TIH, n’est pas aussi typique que dans les autres situations médicales ou chirurgicales justifiant une héparinothérapie.
Dans certains cas, la TIH semble « tardive » et survenir bien au-delà de la 2ème semaine d’épuration extra-rénale et donc de l’exposition à l’héparine.
Dans d’autres cas, elle semble « précoce », survenant dans les heures qui suivent l’injection d’héparine associée à la dialyse, avec un délai bien plus court que les 5 jours minimums d’exposition à l’héparine nécessaires à une TIH classique.
Ces cas, très rares, sont la conséquence, le plus souvent, d’une pré-immunisation du patient vis-à-vis du FP4 après une exposition préalable à l’héparine. Elles peuvent aussi expliquer les complications systémiques graves telles qu’une détresse respiratoire aiguë, ou un collapsus cardiovasculaire, exceptionnellement décrites au décours d’une injection intraveineuse d’héparine lors d’une hémodialyse (31).
Le diagnostic de TIH est bioclinique et repose sur l’analyse évolutive de la NP et sur l’existence de complications, notamment thrombotiques, qui permettront d’établir la probabilité clinique de TIH. La surveillance des plaquettes est donc un élément clé du diagnostic. La NP peut être normale mais c’est sa diminution relative d’au moins 40 % par rapport à une valeur mesurée au début de l’héparinothérapie qui est très évocatrice.
Pour aider à évaluer la probabilité clinique de TIH, des scores sont disponibles. Le plus utilisé à ce jour reste le score des 4Ts, recommandé par la Société Américaine d’Hématologie (20), et un groupe d’experts français membres de plusieurs sociétés savantes françaises (8). Ce dernier est toutefois moins fiable et performant chez les patients ayant subi une CEC, ou ceux bénéficiant d’une ECMO ou en unités de soins. En pratique, après une CEC ou au décours d’une ECMO, la méthode la plus efficace et simple reste le suivi de la NP (21, 22), qui si elle chute brutalement 5 jours après l’initiation de l’héparinothérapie, justifie pleinement la recherche d’anticorps anti-FP4/H. Ceci est d’autant plus vrai au décours d’une ECMO en cas de caillotage du circuit et/ou de chute brutale du fibrinogène plasmatique. Dans les situations cliniques où le score des 4Ts est applicable, ce dernier permet de définir trois niveaux de probabilité de TIH (faible, modéré, ou élevé) et oriente la prescription et l’interprétation des examens biologiques ultérieurs (Figure 2). Il est donc primordial d’obtenir des informations les plus exhaustives et précises possible lors de sa réalisation. En effet, il est admis qu’un score des 4Ts faible (4Ts ≤ 3) permet d’exclure la TIH tandis qu’un score intermédiaire (4Ts = 4 ou 5) ou élevé (4Ts ≥ 6) doit inciter à la prescription de tests biologiques spécifiques.
.png)
Figure 2 : algorithme décisionnel pour le diagnostic et la prise en charge des thrombopénies induites par l’héparine
CLIA : chemiluminescent immunoassay, DO : densité optique, UA : unités arbitraires.
Deux types de tests, complémentaires, sont le plus souvent nécessaires pour diagnostiquer biologiquement une TIH :
- Les tests immunologiques détectent la présence d’anticorps dirigés contre le FP4 modifié et s’ils sont négatifs, ils ont une très bonne valeur prédictive négative en cas de probabilité clinique de TIH intermédiaire. Les principaux tests immunologiques disponibles à ce jour, leurs caractéristiques et leurs performances, ont été résumées dans deux méta-analyses (23, 24). Les tests rapides, qu’ils soient qualitatifs ou semi‑quantitatifs, sont utiles en urgence car ils ont une bonne valeur prédictive négative mais ils reflètent imparfaitement la quantité d’anticorps anti-FP4/H en circulation. Par conséquent, les méthodes ELISA sont plus fiables, mieux corrélés à la probabilité clinique de TIH, et s’ils sont fortement positifs peuvent suffire à confirmer le diagnostic de TIH en cas de probabilité clinique élevée (26). Mais, aucun test immunologique n’a une sensibilité de 100 %, et un test fonctionnel est donc indispensable en cas de probabilité clinique intermédiaire même si l’ELISA est positif, mais aussi en cas de forte suspicion de TIH (score des 4T>6 ou profil d’évolution de la NP évocateur après CEC) si le test immunologique négatif.
- Les tests fonctionnels visent à rechercher l’activation de plaquettes de sujets sains en présence du plasma (ou du sérum) du patient et d’héparine, pour confirmer (ou non) la pathogénicité des anticorps détectés par les tests immunologiques. Contrairement à ces derniers, les tests fonctionnels ne sont pas réalisables en urgence. Les plus performants, le test de libération de sérotonine (SRA) et le test d’activation plaquettaire induite par l’héparine (HIPA), sont réalisés avec des plaquettes lavées et seulement dans quelques centres experts. D’autres tests utilisent du plasma riche en plaquettes (agrégométrie ou cytométrie de flux) mais sont souvent moins sensibles (29). L’impédancemétrie sur sang total (HIMEA) moins utilisée car onéreuse est très performante (30).
Quel que soit le test fonctionnel réalisé, il convient de tester au moins deux concentrations faibles d’héparine (entre 0,01 et 1 UI/ml) et une forte comprise entre 10 à 100 UI/mL. Cette dernière est indispensable afin de vérifier que l’activation plaquettaire est alors bien inhibée. Une condition sans héparine est également intéressante à réaliser car la mise en évidence d’une activation des plaquettes pourrait être associée à une plus forte pathogénicité des anticorps, et par conséquent à un tableau clinique plus sévère (27). De même, des contrôles positifs doivent être inclus dans chaque série.
Dans certains cas douteux, l’addition de FP4 humain (10 μg/mL) à des plaquettes lavées au cours des tests fonctionnels comme le SRA, peut être pertinent pour améliorer la détection d’anticorps pathogènes sans diminuer la spécificité du test (28).
Une communication optimale entre le clinicien et le biologiste est indispensable pour confirmer le diagnostic d’une TIH. Celle-ci devra être ensuite déclarée au centre de pharmacovigilance.
- La distinction entre une TIH typique et une TIH auto-immune est essentielle au choix d’un traitement adapté
Les thrombopénies et thromboses induites par des anticorps anti-FP4 justifient dans tous la mise en place d’un traitement antithrombotique non-héparinique à doses curatives. Les anticoagulants utilisables aujourd’hui sont le danaparoïde sodique et l’argatroban. Le fondaparinux et les anti-Xa oraux directs sont utilisés hors AMM dans cette indication. Des recommandations relatives à la prescription et la surveillance ces thérapeutiques ont été émises par un groupe d’experts francophones en 2020 (8) et par la société américaine d’hématologie en 2018 (20).
Au cours d’une TIH classique, les anticoagulants précédemment cités suffisent dans la plupart des cas, avec l’arrêt de l’héparine, à contrôler le risque thrombotique.
Mais au cours des TIH auto-immunes, l’hypercoagulabilité majeure induite par les anticorps pathogènes justifie l’administration d’immunoglobulines polyvalentes par voie veineuse (1g/kg pendant 2 jours) pour dissocier des cellules les complexes pathogènes IgG/FP4, inhiber l’activation cellulaire et permettre une correction de la NP, ainsi qu’un contrôle de l’extension des thromboses (5). Des échanges plasmatiques ont également été réalisés avec succès chez quelques patients pour qui les traitements habituels s’étaient avérés inefficaces, mais leur utilisation reste très limitée.
Conclusion
Les thrombopénies et thromboses induites par l’héparine sont aujourd’hui plus rares mais toujours possibles, notamment en chirurgie cardiaque, mais aussi chez l’hémodialysé. Une meilleure connaissance de leur physiopathologie, associée aux progrès des méthodes de diagnostic et de traitement ont permis d’améliorer considérablement le pronostic vital et fonctionnel des patients atteints. Certaines situations restent cependant délicates à gérer, comme les interventions chirurgicales sous circulation extra-corporelle, ou l’assistance circulatoire. C’est la raison pour laquelle tout évènement inexpliqué chez un patient à risque doit inciter à rechercher des anticorps anti-FP4/héparine le plus vite possible afin d’éviter toute ré-exposition à un anticoagulant héparinique. Une collaboration étroite entre cliniciens et biologistes est primordiale pour garantir un diagnostic précoce, et un traitement adapté et efficace.
REFERENCES
1. Muller L, Gebicka P, Handtke S, Schonborn L, Thiele T. Advances in our understanding of anti-PF4 related immunothrombosis. Frontiers in immunology. 2025;16:1724207.
2. Pouplard C, Iochmann S, Renard B, Herault O, Colombat P, Amiral J, et al. Induction of monocyte tissue factor expression by antibodies to heparin- platelet factor 4 complexes developed in heparin-induced thrombocytopenia. Blood. 2001;97(10):3300-2.
3. Perdomo J, Leung HHL, Ahmadi Z, Yan F, Chong JJH, Passam FH, et al. Neutrophil activation and NETosis are the major drivers of thrombosis in heparin-induced thrombocytopenia. Nature communications. 2019;10(1):1322.
4. Hayes V, Johnston I, Arepally GM, McKenzie SE, Cines DB, Rauova L, et al. Endothelial antigen assembly leads to thrombotic complications in heparin-induced thrombocytopenia. The Journal of clinical investigation. 2017;127(3):1090-8.
5. Greinacher A, Selleng K, Warkentin TE. Autoimmune heparin-induced thrombocytopenia. J Thromb Haemost. 2017;15(11):2099-114.
6. Nguyen TH, Medvedev N, Delcea M, Greinacher A. Anti-platelet factor 4/polyanion antibodies mediate a new mechanism of autoimmunity. Nature communications. 2017;8:14945.
7. Warkentin TE, Kelton JG. A 14-year study of heparin-induced thrombocytopenia. The American journal of medicine. 1996;101(5):502-7.
8. Gruel Y, De Maistre E, Pouplard C, Mullier F, Susen S, Roullet S, et al. Diagnosis and management of heparin-induced thrombocytopenia. Anaesth Crit Care Pain Med. 2020;39(2):291-310.
9. Gruel Y, Vayne C, Rollin J, Weber P, Faille D, Bauters A, et al. Comparative Analysis of a French Prospective Series of 144 Patients with Heparin-Induced Thrombocytopenia (FRIGTIH) and the Literature. Thromb Haemost. 2020;120(7):1096-107.
10. Tardy B, Tardy-Poncet B, Fournel P, C V, Jospe R, Dacosta A. Lower limbs veins should be sytematically explored in patients with isolated heparin-induced thrombocytopenia. Thromb Haemostas. 1999;82(3):1199-2000.
11. Fontana P, Bodmer A, Gruel Y, Boehlen F, Janer V, Kaya G, et al. Skin necrosis is a clinical manifestation of low-molecular weight heparin-induced thrombocytopenia. Thromb Haemost. 2004;91(1):196-7.
12. Warkentin TE. Think of HIT. Hematology Am Soc Hematol Educ Program. 2006:408-
13. Matsuo T, Wanaka K, Miyasita K, Prechel M, Walenga JM. Clinical evaluation of acute systemic reaction and detection of IgG antibodies against PF4/heparin complexes in hemodialysis patients. Thrombosis Research. 2011.
14. Warkentin TE. Fondaparinux: does it cause HIT? Can it treat HIT? Expert review of hematology. 2010;3(5):567-81.
15. Poudel DR, Ghimire S, Dhital R, Forman DA, Warkentin TE. Spontaneous HIT syndrome post-knee replacement surgery with delayed recovery of thrombocytopenia: a case report and literature review. Platelets. 2017;28(6):614-20.
16. Warkentin TE, Sheppard JA, Manheim JC. HIT complicating fondaparinux prophylaxis: fondaparinux-dependent platelet activation as a marker for fondaparinux-induced HIT. Thromb Haemost. 2014;112(6):1319-22.
17. Warkentin TE, Kelton JG. Delayed-onset heparin-induced thrombocytopenia and thrombosis. Annals of internal medicine. 2001;135(7):502-6.
18. Pohl C, Kredteck A, Bastians B, Hanfland P, Klockgether T, Harbrecht U. Heparin-induced thrombocytopenia in neurologic patients treated with low-molecular-weight heparin. Neurology. 2005;64(7):1285-7.
19. Fesler MJ, Creer MH, Richart JM, Edgell R, Havlioglu N, Norfleet G, et al. Heparin-induced thrombocytopenia and cerebral venous sinus thrombosis: case report and literature review. Neurocrit Care. 2011;15(1):161-5.
20. Cuker A, Arepally GM, Chong BH, Cines DB, Greinacher A, Gruel Y, et al. American Society of Hematology 2018. Guidelines for management of venous thromboembolism: Heparin-Induced Thrombocytopenia. Blood Advances. 2018;2 (22):3360-92. .
21. Pouplard C, May MA, Regina S, Marchand M, Fusciardi J, Gruel Y. Changes in platelet count after cardiac surgery can effectively predict the development of pathogenic heparin-dependent antibodies. British journal of haematology. 2005;128(6):837-41.
22. Vayne C, May MA, Bourguignon T, Lemoine E, Guery EA, Rollin J, et al. Frequency and Clinical Impact of Platelet Factor 4-Specific Antibodies in Patients Undergoing Extracorporeal Membrane Oxygenation. Thromb Haemost. 2019;119(7):1138-46.
23. Sun L, Gimotty PA, Lakshmanan S, Cuker A. Diagnostic accuracy of rapid immunoassays for heparin-induced thrombocytopenia. A systematic review and meta-analysis. Thrombosis and Haemostasis. 2016;115(5).
24. Nagler M, Bachmann LM, ten Cate H, ten Cate-Hoek A. Diagnostic value of immunoassays for heparin-induced thrombocytopenia: a systematic review and meta-analysis. Blood. 2016;127(5):546-57.
25. Jousselme E, Guéry EA, Nougier C, Sobas F, Rollin J, Gruel Y, et al. Prospective evaluation of two specific IgG immunoassays (HemosIL(®) AcuStar HIT-IgG and HAT45G(®) ) for the diagnosis of heparin-induced thrombocytopenia: A Bayesian approach. Int J Lab Hematol. 2021;43(3):468-76.
26. Pouplard C, Amiral J, Borg JY, Laporte-Simitsidis S, Delahousse B, Gruel Y. Decision analysis for use of platelet aggregation test, carbon 14 serotonin release assay, and heparin-platelet factor 4 enzyme-linked immunosorbent assay for diagnosis of heparin-induced thrombocytopenia. American journal of clinical pathology. 1999;111(5):700-6.
27. Rollin J, Charuel N, Gruel Y, Billy S, Guery EA, May MA, et al. Variable serotonin release assay pattern and specificity of PF4-specific antibodies in HIT, and clinical relevance. J Thromb Haemost. 2022;20(11):2646-55.
28. Vayne C, Guery EA, Kizlik-Masson C, Rollin J, Bauters A, Gruel Y, et al. Beneficial effect of exogenous platelet factor 4 for detecting pathogenic heparin-induced thrombocytopenia antibodies. British journal of haematology. 2017;179(5):811-9.
29. Warkentin TE. Immunologic Effects of Heparin Associated With Hemodialysis: Focus on Heparin-Induced Thrombocytopenia. Semin Nephrol. 2023;43(6):151479.
30. Carrier M, Knoll GA, Kovacs MJ, Moore JC, Fergusson D, Rodger MA. The prevalence of antibodies to the platelet factor 4 -heparin complex and association with access thrombosis in patients on chronic hemodialysis. Thromb Res. 2007;120(2):215-20.
31. Warkentin TE. Hemodialysis-associated acute systemic reactions and heparin-induced thrombocytopenia. Thromb Res. 2012;129(4):405-6.
Rédigé le 10/04/2026
Liens d'intérêt de l’auteur : Stago, Viatris et Sanofi

Dossier thématique réalisé avec le soutien institutionnel du laboratoire Viatris

 26 minutes
26 minutes
