
Le traitement de 1re intention de la DMLA exsudative repose sur des injections intravitréennes d’un anti-VEGF, qui permet de stabiliser voire d’améliorer la vision des patients (illustration).
L'anti-VEGF à base d'aflibercept EYLEA 40 mg/mL solution injectable est désormais disponible en seringue préremplie contenant 90 µL de solution injectable prête à l'emploi.
EYLEA en seringue préremplie s'ajoute à la présentation d'EYLEA en flacon, déjà commercialisée.
En flacon ou en seringue préremplie, EYLEA est indiqué dans le traitement de :
- la forme néovasculaire (humide) de la dégénérescence maculaire liée à l'âge (DMLA) (cf. VIDAL Reco "DMLA") ;
- la baisse d'acuité visuelle due
- à l'œdème maculaire secondaire à une occlusion de branche veineuse rétinienne (OBVR) ou de la veine centrale de la rétine (OVCR) ;
- à l'œdème maculaire diabétique (OMD) ;
- à une néovascularisation choroïdienne (NVC) myopique.
La présentation en seringue préremplie et celle en flacon sont également identiques en termes de composition (dosage en aflibercept et excipients) et de posologie.
Quelle que soit l'indication, la dose d'aflibercept à injecter est de 2 mg d'aflibercept, soit 50 µL (cf. Encadré 1).
Encadré 1 - Schémas posologiques recommandés d'EYLEA, indication par indication
Forme humide de la DMLA - 2 mg d'aflibercept, correspondant à 50 µL selon le schéma suivant :
- instauration du traitement : injection 1 fois par mois pendant 3 mois consécutifs ;
- puis 1 injection tous les 2 mois. En fonction du jugement du médecin sur les résultats visuels et/ou anatomiques, l'intervalle entre 2 injections peut être maintenu à 2 mois ou davantage étendu en utilisant un protocole "Treat and Extend", au cours duquel les intervalles entre les injections augmentent par ajustements de 2 ou 4 semaines, afin de maintenir la réponse visuelle et/ou anatomique. En cas de détérioration des paramètres visuels et/ou anatomiques, l'intervalle entre 2 injections doit être réduit en conséquence, à un intervalle minimum de 2 mois au cours des 12 premiers mois de traitement.
Œdème maculaire secondaire à une occlusion veineuse rétinienne (OVCR ou OBVR) - 2 mg d'aflibercept, correspondant à 50 µL selon le schéma suivant :
- première injection ;
- puis administration mensuelle. L'intervalle entre deux injections ne doit pas être inférieur à 1 mois. Le traitement mensuel est poursuivi jusqu'à ce que l'acuité visuelle maximale soit atteinte et/ou jusqu'à l'absence de signe d'activité de la maladie. Trois injections mensuelles ou plus peuvent être nécessaires. Ensuite, le traitement peut être poursuivi selon un protocole "Treat and Extend" avec une augmentation progressive de l'intervalle entre 2 injections afin de maintenir la réponse visuelle et/ou anatomique. Cependant, les données disponibles ne permettent pas de conclure sur la durée de ces intervalles.
Œdème maculaire diabétique - 2 mg d'aflibercept, correspondant à 50 µL, selon le schéma suivant :
- instauration du traitement : 1 injection 1 fois par mois pendant 5 mois consécutifs ;
- puis 1 injection tous les 2 mois. Il n'est pas nécessaire de réaliser des visites de suivi entre les injections. Après les 12 premiers mois de traitement, et en fonction de résultats visuels et/ou anatomiques, l'intervalle entre deux injections peut être prolongé, par exemple avec un protocole « Treat and Extend » au cours duquel les intervalles entre les injections augmentent progressivement afin de maintenir la réponse visuelle et/ou anatomique. Cependant, les données disponibles ne permettent pas de conclure sur la durée de ces intervalles. En cas de détérioration des paramètres visuels et/ou anatomiques, l'intervalle entre 2 injections doit être réduit en conséquence.
Néovascularisation choroïdienne myopique :
- 1 injection intravitréenne unique de 2 mg d'aflibercept, correspondant à 50 µL. Des injections supplémentaires peuvent être administrées si les paramètres visuels et/ou anatomiques indiquent que la maladie persiste. Les récidives doivent être traitées comme des nouvelles manifestations de la maladie. Le calendrier de suivi doit être déterminé par le médecin qui administre le traitement. L'intervalle entre 2 injections ne doit pas être inférieur à un mois.
|
Une seringue préremplie est à usage unique. Elle est munie d'un bouchon-piston et d'un adaptateur Luer Lock. Elle doit être utilisée pour le traitement d'un seul œil.
- Préparation de la seringue préremplie avant l'injection
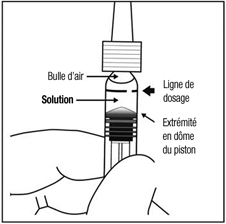
Le corps de la seringue préremplie est marquée par une ligne de dosage noire correspondant à 50 µL (2 mg d'aflibercept).
Le volume excédentaire de solution doit être éliminé avant l'injection, en appuyant lentement sur le piston pour aligner la base cylindrique de l'extrémité en dôme du piston avec la ligne de dosage noire sur la seringue (cf. Encadré 2).
- Ouvrir délicatement le blister.
- Retirer de manière aseptique la seringue du blister stérilisé.
- Retirer le capuchon de la seringue.
- Fixer fermement, de manière aseptique, l'aiguille d'injection sur l'extrémité Luer Lock de la seringue par un mouvement de rotation.
- Éliminer toutes les bulles et expulser l'excédent de médicament, en appuyant lentement sur le piston pour aligner la base cylindrique de l'extrémité en dôme du piston avec la ligne de dosage noire sur la seringue (équivalant à 50 µl).
|
- Conservation d'EYLEA en seringue préremplie
EYLEA en seringue préremplie doit être conservé au réfrigérateur (entre 2 °C et 8 °C), dans son blister et dans l'emballage extérieur, à l'abri de la lumière.
Avant l'utilisation, le blister d'EYLEA seringue préremplie non ouvert peut être conservé à température ambiante (inférieure à 25 °C) pendant 24 heures maximum.
Identité administrative
- Liste I
- Prescription réservée aux spécialistes en ophtalmologie
- Boîte de 1 seringue préremplie, CIP 3400926783501
- Remboursable à 100 % selon la procédure des médicaments d'exception (cf. Encadré 3) (Fiche d'information thérapeutique - Journal officiel du 13 décembre 2016, texte 26)
- Prix public TTC = 637,57 euros
- Agrément aux collectivités (Journal officiel du 30 octobre 2013, texte 10)
- Laboratoire Bayer Healthcare
Encadré 3 - Périmètre des indications prises en charge - EYLEA
- Traitement de la forme néovasculaire (humide) rétrofovéolaire de la dégénérescence maculaire liée à l'âge (DMLA) chez l'adulte ;
- Traitement de la baisse d'acuité visuelle due à l'œdème maculaire secondaire à une occlusion de branche veineuse rétinienne (OBVR) ou de la veine centrale de la rétine (OVCR) chez l'adulte ;
- Traitement de la baisse d'acuité visuelle due à l'œdème maculaire diabétique, en cas de forme diffuse ou de fuites proches du centre de la macula, chez les patients adultes ayant une acuité visuelle inférieure ou égale à 5/10 et chez lesquels la prise en charge du diabète a été optimisée ;
- Traitement de la baisse d'acuité visuelle due à une néovascularisation choroïdienne (NVC) myopique chez l'adulte.
|



 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.