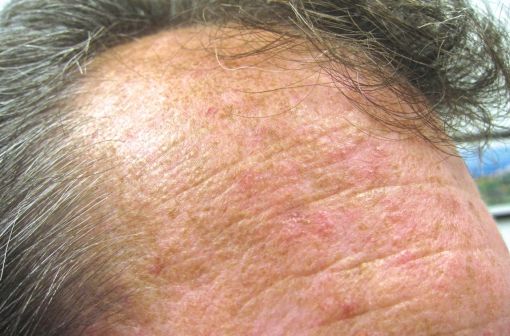
Lésions de kératose actinique sur le front d'un patient (illustration @Future FamDoc sur Wikimedia).
La Commission européenne a décidé de suspendre l'AMM (autorisation de mise sur le marché) du gel à base de mébutate d'ingénol, PICATO (cf. Encadré 1), par mesure de précaution, suivant en cela la recommandation du PRAC (Comité européen de pharmacovigilance).
Cette mesure provisoire intervient alors qu'une réévaluation européenne du rapport bénéfice/risque de PICATO, initiée en septembre 2019, est toujours en cours. Celle-ci a pour objectif d'évaluer le lien possible entre l'utilisation de PICATO et le développement d'un cancer de la peau.
La décision finale de la Commission européenne dépendra des résultats de cette réévaluation.
Encadré 1 - À propos de PICATO
|
PICATO, kératoses et risque de cancer cutané : ce que l'on sait
La mise sur le marché de PICATO en février 2014 s'est accompagnée d'une surveillance particulière sur un éventuel surrisque de certains cancers cutanés dans la zone traitée, en particuliers de carcinomes épidermoïdes.
Dans un point d'information en date du 17 janvier 2020, l'Agence de sécurité du médicament et des produits de santé (ANSM) rappelle que "En effet, les résultats de plusieurs études suggèrent une incidence plus élevée de cancers cutanés, et plus particulièrement de carcinomes épidermoïdes, chez les patients traités par mébutate d'ingénol, comparé à celle observée chez des patients traités par placebo ou par d'autres médicaments, en particulier chez des patients ayant des antécédents de cancers cutanés".
Dans un état des lieux publié le 17 janvier 2020, le PRAC précise les éléments suivants :
- résultats finaux d'une étude menée pendant 3 ans sur 484 patients versus imiquimod (ALDARA) : l'incidence de cancer cutané est de 3,3 % dans le groupe PICATO contre 0,4 % dans le groupe comparateur imiquimod ;
- résultats d'un essai contrôlé versus véhicule de 8 semaines (n = 1 262) : l'incidence des tumeurs cutanées est de 1 % dans le groupe mébutate d'ingénol contre 0,1 % dans le groupe contrôle ;
- résultats de 4 essais cliniques (n = 1 234) menés avec un autre ester, le disoxate d'ingénol, très proche du mébumate d'ingénol : l'incidence des tumeurs de la peau est de 7,7 % dans le groupe disoxate d'ingénol contre 2,9 % dans le groupe comparateur.
L'ANSM précise que les kératoses peuvent, en outre, constituer elles-mêmes un signe précurseur de cancer de la peau : "elles évoluent lentement et sont sans gravité, à condition d'être dépistées et traitées tôt grâce à une surveillance régulière". Un contrôle dermatologique régulier est par conséquent nécessaire.
Une première restriction d'utilisation en novembre 2019
En novembre 2019, soit 2 mois après l'initiation de la réévaluation européenne de PICATO, les premières recommandations ont été données aux prescripteurs, à savoir l'utilisation prudente de PICATO chez les patients ayant des antécédents de cancer cutané (notre article du 18 novembre 2019).
En pratique : quelles conséquences pour les professionnels de santé et les patients ?
Suite à la suspension de l'AMM de PICATO, il est demandé :
- aux médecins de ne plus prescrire ce gel, ni en initiation, ni en renouvellement. Des alternatives sont disponibles sur le marché pour le traitement des kératoses actiniques ;
- aux pharmaciens de ne plus délivrer PICATO. Ils doivent informer les patients de la décision provisoire de la Commission européenne, et les orienter vers leur médecin prescripteur ;
- aux patients de ne plus utiliser le gel PICATO. Le traitement par PICATO peut être arrêté sans conséquence. Les patients doivent consulter leur médecin prescripteur pour envisager une alternative. En cas d'apparition de nouvelles lésions cutanées, d'excroissance ou de symptômes inhabituels, les patients doivent consulter leur médecin.
Un rappel des lots de PICATO sera organisé prochainement et une lettre d'information sera adressée aux professionnels de santé.
EDIT du 28 janvier 2020 : ALERTE MED20/A003/B003 - Rappel de tous les lots non périmés disponibles sur le marché français de PICATO gel 150 µg/g et 500 µg/g. Ce rappel concerne les officines, les établissements de santé et le circuit de distribution pharmaceutique. Il ne s'adresse pas aux patients. /FIN EDIT
Pour aller plus loin
PICATO (mébutate d'ingénol) : suspension de l'autorisation de mise sur le marché dans l'attente des conclusions de la réévaluation du rapport bénéfice/risque (ANSM, 17 janvier 2020)
EMA suspends Picato as a precaution while review of skin cancer risk continues (EMA, 17 janvier 2020)
EDIT du 28 janvier 2020 : ALERTE MED20/A003/B003 - rappel de lots de PICATO gel (ANSM, 27 janvier 2020) / FIN EDIT
Sur VIDAL.fr
Kératose actinique : utiliser PICATO avec prudence en cas d'antécédents de cancer de la peau (18 novembre 2020)
Sources
Pour recevoir gratuitement toute lâactualitÃĐ par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.