La mitomycine C est une substance antinéoplasique et antibiotique extraite de Streptomyces caespitosus, une espèce d'actinobactéries (illustration @Wikimedia).
Face à la persistance des difficultés d'approvisionnement en mitomycine C liées à la rupture de stock prolongée des spécialités AMETYCINE, l'ANSM (Agence nationale de sécurité du médicament et des produits de santé) fait le point sur les alternatives disponibles (spécialités importées et ATU) et les recommandations d'utilisation selon les indications.
Pour rappel, cette rupture de stock fait suite à la mise en évidence de manquements aux bonnes pratiques sur le site de fabrication de la mitomycine C et au rappel des lots non périmés des spécialités concernées du laboratoire Kyowa Kirin Pharma (notre article du 14 octobre 2019).
Remplacement d'AMETYCINE à fin 2019 : 3 spécialités importées et 1 spécialité sous ATU nominative
Au total, 3 spécialités à base de mitomycine C sont importées en France, sous forme de poudre adaptée à la préparation de solution à usage intravésical/solution pour injection/perfusion :
- depuis le 4 novembre 2019 (notre article du 6 novembre 2019), MITOMYCIN MEDAC 1 mg/mL (40 mg), EDIT du 10 avril 2020 : agrément aux collectivités - Journal officiel du 31 mars 2020 texte 16 /FIN EDIT
- à partir de la semaine du 25 novembre (semaine 48) ou du 2 décembre (semaine 49) : MITOCIN 20 mg et MITOMYCIN ACCORD 20 mg.
EDIT du 30 avril 2020 : commercialisation de la spécialité MITOMYCINE SUBSTIPHARM 20 mg poudre pour solution injectable en flacon (étui unitaire) à compter de mi-avril 2020, et arrêt de l'importation de MITOCIN 20 mg SUBSTIPHARM (point d'information actualisé au 30 avril 2020 - ANSM). /FIN EDIT
Une spécialité américaine est également disponible à partir de la semaine 48, en ATU nominative (cf. Fiche ATU nominative de MITOSOL) :
- MITOSOL 0,2 mg/mL poudre et solvant pour solution à usage ophtalmique. Cette spécialité est autorisée aux États-Unis dans l'indication chirurgie du glaucome. Elle est à utiliser à la place des préparations pharmaceutiques de mitomycine C.
Dans certaines indications en oncologie et en onco-ophtalmologie, d'autres médicaments peuvent être utilisés.
Actualisation des indications prioritaires : quelles spécialités de mitomycine C utiliser en fonction de l'indication ?
Un premier point d'information avait été publié sur le site de l'ANSM fin octobre 2019, suite à l'importation d'unités de la spécialité MITOMYCIN MEDAC 1 mg/mL pulver til intravesikalopplosning/injecktions-/infusjonsvaeske, opplosning, initialement destinées au marché scandinave, afin de prioriser leur utilisation dans certaines indications (notre article du 6 novembre 2019).
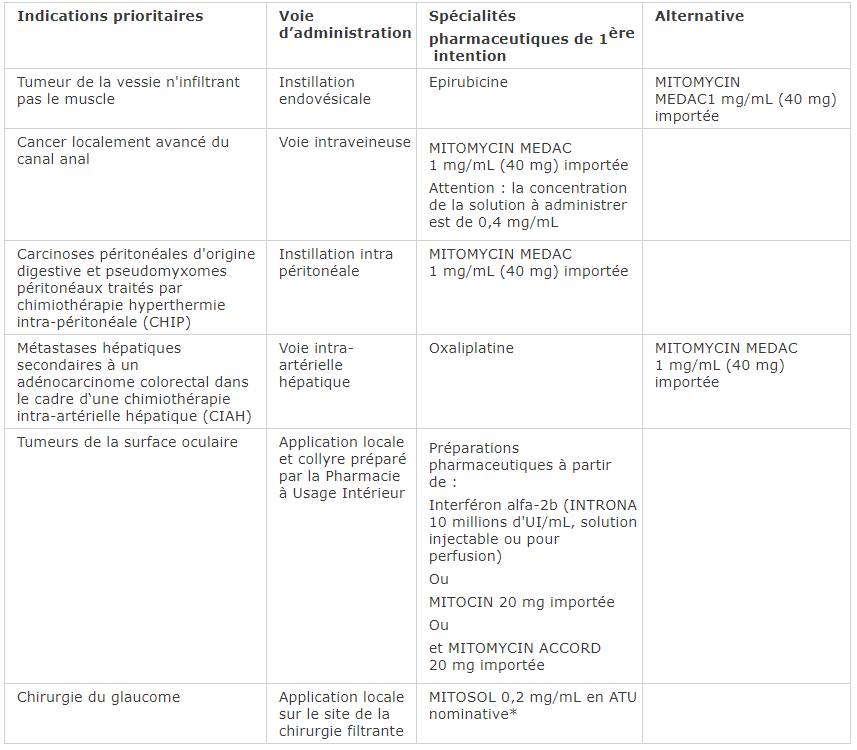
Les alternatives disponibles étant désormais différentes, l'ANSM a actualisé ses recommandations et révisé les indications prioritaires pour l'utilisation des différentes spécialités de mitomycine C mises à disposition en France d'ici à fin 2019 (cf. Tableau I).
Tableau I - Indications prioritaires : traitement de première intention et alternatives thérapeutiques recommandées

Ces nouvelles recommandations de l'ANSM ont été validées par les sociétés savantes suivantes :
- Association Française d'Urologie,
- Société Française du Glaucome,
- Société Française d'Ophtalmologie,
- Société Française de Pharmacie Clinique,
- Société Française de Pharmacie Oncologique,
- REseau NAtional de référence des tumeurs rares du PEritoine,
- Association Nationale pour les maladies péritonéales primitives et métastatiques,
- Fédération Francophone de Cancérologie Digestive.
Coexistence des différentes spécialités de mitomycine C : attention aux erreurs
Les diverses spécialités de mitomycine C (spécialités importées et spécialité sous ATU nominative) vont co-exister pendant quelques temps.
L'ANSM met en garde contre les erreurs lors de la prescription, la dispensation, la reconstitution et l'administration de ces médicaments, en raison de protocoles d'utilisation différents.
- MITOMYCINE MEDAC 1 mg/mL : pas d'administration par voie ophtalmique
La présence d'urée dans la formulation de cette spécialité est compatible avec l'injection en intraveineuse (en respectant la concentration de 0,4 mg/mL).
En l'absence de données permettant d'exclure sa toxicité par voie ophtalmique, il n'est pas recommandé d'utiliser MITOMYCINE MEDAC 1 mg/mL pour les préparations en ophtalmologie.
- MITOMYCIN MEDAC : concentration identique à AMETYCINE 40 mg, mais différente d'AMETYCINE 10 mg
Après reconstitution avec 40 mL de solvant, la concentration de la solution est de 1 mg/mL, comme avec AMETYCINE 40 mg.
Cette concentration est différente de celle d'AMETYCINE 10 mg (en flacon de 25 mL, concentration de 0,4 mg/mL après reconstitution).
Il est nécessaire de respecter la concentration de 0,4 mg/mL pour l'injection intraveineuse.
Cette spécialité a reçu une AMM française ; sa commercialisation effective est prévue pour début 2020 (notre article du 14 octobre 2019).
- MITOMYCIN MEDAC : optimiser l'utilisation
Dans la mesure du possible, il est donc demandé de regrouper les patients pour les administrations.
- MITOCIN 20 mg : même concentration qu'AMETYCINE 10 mg
La solution doit être utilisée immédiatement après reconstitution.
- MITOSOL (ATU nominative) : au bloc en extemporané
Pour aller plus loin
Mitomycine C : point sur les alternatives et les indications jugées prioritaires - Point d'Information (ANSM, 22 novembre 2019)
MITOSOL 0.2 mg/ml, poudre et solvant pour solution à usage ophtalmique- Fiche référentiel ATU nominative (RCP et notice)
EDIT du 10 avril 2020 : inscription de MITOMYCIN MEDAC sur la liste des spécialités pharmaceutiques agréées aux collectivités - Journal officiel du 31 mars 2020, texte 16 /FIN EDIT
EDIT du 30 avril 2020 : Mitomycine C : point sur les alternatives et les indications jugées prioritaires et sur le risque d'erreur médicamenteuse - Point d'Information (ANSM, actualisé le 30 avril 2020)/ FIN EDIT
Sur VIDAL.fr
Rupture de stock d'AMETYCINE : importation d'un médicament similaire et priorisation des indications (6 novembre 2019)
AMETYCINE et MITOMYCIN-C KYOWA : rappel de lots de grande envergure (14 octobre 2019)
Pour aller plus loin
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.