Lors d’une fécondation in vitro avec ICSI (IntraCytoplasmic Sperm Injection), un spermatozoïde est injecté dans le cytoplasme de chaque ovocyte fécondable (illustration).
REKOVELLE solution injectable en stylo prérempli multidose est une nouvelle spécialité indiquée dans la stimulation ovarienne contrôlée pour induire le développement de follicules multiples, chez les femmes entreprenant un programme d'Assistance Médicale à la Procréation (AMP) tel que la fécondation in vitro (FIV) ou la FIV avec injection intracytoplasmique de spermatozoïdes (ICSI).
Il n'y a pas d'expérience clinique avec REKOVELLE dans le cadre d'un protocole long avec agoniste de la GnRH.
Le principe actif de REKOVELLE est la follitropine delta. Il s'agit de la première FSH recombinante (r-hFSH) produite à partir d'une lignée cellulaire humaine, disponible sur le marché français.
Sa particularité consiste à être administrée selon une posologie individualisée pour chaque patiente, visant à obtenir un nombre suffisant d'ovocytes prélevés et à réduire le nombre d'interventions pour prévenir le syndrome d'hyperstimulation ovarienne (SHO).
REKOVELLE non inférieur à GONAL-F sur les taux de grossesses et d'implantations évolutives
Dans son avis du 5 avril 2017, la Commission de la Transparence a évalué REKOVELLE sur la base d'une étude de non infériorité en simple aveugle, ESTHER 1 (Fertil Steril. 2017), ayant comparé l'efficacité de REKOVELLE à celle de GONAL-F (follitropine alpha - recombinante) chez des patientes entreprenant un premier cycle de stimulation ovarienne contrôlée pour FIV/ICSI avec un antagoniste de la GnRH (n = 1329).
Les patientes ont reçu une dose quotidienne personnalisée de REKOVELLE, sur la base de leur taux sérique d'hormone anti-müllérienne (AMH) mesuré au cours de la visite de sélection et de leur poids au moment de la randomisation. Cette dose personnalisée restait fixe pendant tout le traitement.
La dose de GONAL-F pouvait être ajustée par paliers à partir de J6, en fonction de la réponse individuelle.
Les co-critères de jugement principaux étaient :
- le taux de grossesses évolutives (au moins un fœtus intra-utérin viable à l'échographie 10-11 semaines après le transfert) ;
- le taux d'implantations évolutives (nombre de fœtus intra-utérins viables à l'échographie 10-11 semaines après le transfert divisé par le nombre de blastocystes transférés).
La non infériorité de REKOVELLE par rapport à GONAL-F a été démontrée pour les deux co-critères de jugement principaux avec, en population perprotocole :
- un taux de grossesses évolutives de 31,8 % dans le groupe REKOVELLE (198/623) et 32,6 % dans le groupe GONAL-F (206/632) (différence : - 0,9 %, IC 95 % : [- 6,0 %; 4,3 %]),
- et un taux d'implantations évolutives respectivement de 36,2 % (200/553) et 36,9 % (206/558) (différence : - 0,9 %, IC 95 % : [- 6,5 % ; 4,7 %]).
Pour ces co-critères de jugement, la marge de non infériorité a toutefois été de - 8%, correspondant à une perte d'efficacité de 20%, cliniquement significative.
En termes de tolérance, les événements indésirables les plus fréquents (> ou = 4 %) ont été des céphalées (14,6 % versus 13,3 % dans les groupes REKOVELLE et GONAL-F respectivement), des douleurs liées aux interventions (7,4 % vs 7,9 %, principalement prélèvements d'ovocytes), des douleurs pelviennes (6,9 % vs 6,2 %).
Les hyperstimulations ovariennes ont concerné 3,5 % des patientes (n = 23) du groupe REKOVELLE et 4,8 % (n = 32) du groupe GONAL-F (différence non significative).
Parmi celles-ci, 2,6 % (n = 17) dans le groupe REKOVELLE et 3 % (n = 20) dans le groupe GONAL-F étaient des hyperstimulations précoces (survenant < ou = 9 jours après le déclenchement de la maturation finale) pour lesquelles des interventions préventives étaient prévues au protocole.
Traitement de 1re intention, SMR important, pas d'ASMR
En conclusion de son avis, la Commission de la Transparence considère que REKOVELLE est un traitement de première intention dans la stimulation de l'ovulation en vue d'une fécondation in vitro avec ou sans ICSI.
Sur la base des données disponibles, la Commission estime que le service médical rendu (SMR) par REKOVELLE est important dans son indication, sans amélioration du service médical rendu par rapport à GONAL-F (ASMR V) compte tenu :
- "de la non infériorité démontrée de REKOVELLE par rapport à GONAL-f sur les taux de grossesses et d'implantations, évolutives,
- mais avec une marge importante de non infériorité, cliniquement significative,
- du nombre inférieur d'hyperstimulations ovariennes observées avec REKOVELLE, par rapport à GONAL-f, sans différence significative,
- du besoin thérapeutique théoriquement couvert."
REKOVELLE en pratique
Le laboratoire Ferring a mis à disposition 3 dosages de REKOVELLE :
- REKOVELLE 12 µg/0,36 mL solution injectable : 1 stylo multidose prérempli délivre 12 µg de follitropine delta dans 0,36 mL de solution.
- REKOVELLE 36 µg/1,08 mL solution injectable : 1 stylo multidose prérempli délivre 36 µg de follitropine delta dans 1,08 mL de solution.
- REKOVELLE 72 µg/2,16 mL solution injectable : 1 stylo multidose prérempli délivre 72 µg de follitropine delta dans 2,16 mL de solution.
Le stylo prérempli multidose est équipé d'un sélecteur de dose et d'une fenêtre d'affichage des doses sélectionnées (Cf. Figure 1).
Figure 1 - Stylo REKOVELLE et ses composants
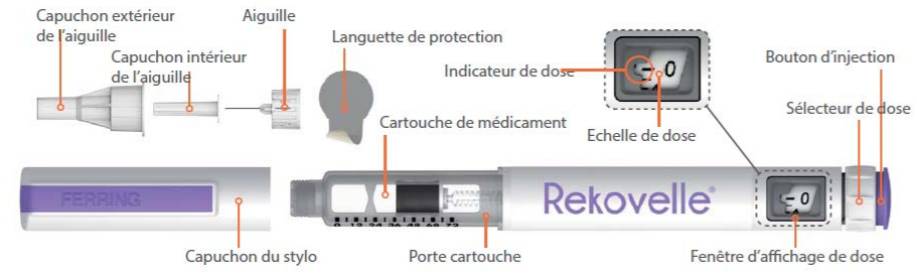 |
Le stylo peut délivrer des doses de 0,33 à 20 µg de REKOVELLE, par intervalles gradués de 0,33 µg.
Chaque nombre est séparé par deux traits, chaque trait correspond à un intervalle de 0,33 µg.
La dose est sélectionnée en tournant le bouton de réglage et délivrée en pressant sur le bouton d'injection (au bout du stylo).
Il est recommandé d'appuyer sur le bouton d'injection pendant 5 secondes, pour être sûr d'avoir injecté toute la dose.
Les aiguilles sont fournies avec le stylo. Il faut utiliser une nouvelle aiguille à chaque injection.
Le stylo est jetable au terme de son utilisation.
Une posologie individualisée pour chaque patiente
Le traitement doit être initié sous la surveillance d'un médecin ayant l'expérience du traitement des troubles de la fertilité.
La posologie de REKOVELLE est individualisée pour chaque patiente et a pour objectif d'obtenir une réponse ovarienne associée à un profil favorable de tolérance/efficacité.
REKOVELLE est dosé en microgrammes. Le schéma posologique est spécifique à REKOVELLE et la dose en microgrammes ne peut pas être appliquée à d'autres gonadotrophines.
- Calcul de la dose : fonction du taux sérique d'AMH et du poids de la patiente
- du taux sérique d'hormone anti-müllérienne (AMH) récent de la patiente (c'est-à-dire réalisé au cours des 12 derniers mois), mesuré par le test diagnostique du laboratoire Roche suivant : test immunologique ELECSYS AMH Plus (absence de standardisation des tests AMH disponibles). Ce taux est exprimé en pmol/L et arrondi au nombre entier le plus proche. Si le taux d'AMH est exprimé en ng/mL, il doit être converti en pmol/L en le multipliant par 7,14 avant utilisation (ng/mL x 7,14 = pmol/L),
- et de son poids corporel (mesuré sans chaussures ni manteau, juste avant le début de la stimulation).
Chez les femmes ayant un taux d'AMH < 15 pmol/L, la dose quotidienne est de 12 µg, indépendamment du poids corporel.
Chez les femmes ayant un taux d'AMH > ou = 15 pmol/L, la dose quotidienne décroît progressivement de 0,19 à 0,10 µg/kg en fonction de l'augmentation du taux d'AMH (Cf. Tableau I).
La dose doit être arrondie au 0,33 µg le plus proche pour correspondre à la graduation du stylo pour injection. La dose quotidienne maximale pour le premier cycle de traitement est de 12 µg.
Tableau I - Schéma d'administration de REKOVELLE
| Taux d'AMH (pmol/L) |
inférieur à 15 | 15-16 | 17 | 18 | 19-20 | 21-22 | 23-24 | 25-27 | 28-32 | 33-39 | > ou = 40 |
| Dose quotidienne fixe de REKOVELLE | 12 µg | 0,19 µg/kg | 0,18 µg/kg | 0,17 µg/kg | 0,16 µg/kg | 0,15 µg/kg | 0,14 µg/kg | 0,13 µg/kg | 0,12 µg/kg | 0,11 µg/kg | 0,10 µg/kg |
- Administration sous-cutanée sous surveillance médicale en début de traitement
La première injection doit être effectuée sous surveillance médicale directe.
Les patientes doivent être entraînées à l'utilisation du stylo pour injection REKOVELLE et à la réalisation des injections. L'auto-injection ne doit être réalisée que par des patientes très motivées, correctement formées et pouvant disposer de conseils avisés.
- Modalité de conservation
Après la première ouverture, le stylo prérempli peut être conservé 28 jours à une température ne dépassant pas 25 °C.
Avant la première utilisation, REKOVELLE peut être conservé hors du réfrigérateur, sans être réfrigéré à nouveau, à une température ne dépassant pas 25 °C pendant une durée maximale de 3 mois (cette durée maximale de 3 mois inclut la période d'utilisation après la première ouverture).
Identité administrative
- Liste I
- Surveillance particulière pendant le traitement
- Prescription réservée aux spécialistes en gynécologie médicale, en gynécologie-obstétrique ou en endocrinologie, diabétologie et nutrition
- REKOVELLE 12 µg/0,36 mL, boîte de 1 stylo prérempli + 3 aiguilles, CIP 3400930110980, prix public TTC = 83,86 euros
- REKOVELLE 36 µg/1,08 mL, boîte de 1 stylo prérempli + 6 aiguilles, CIP 3400930110997, prix public TTC = 248,42 euros
- REKOVELLE 72 µg/2,16 mL, boîte de 1 stylo prérempli + 9 aiguilles, CIP 3400930111000, prix public TTC = 495,26 euros
- Remboursable à 100 % (Journal officiel du 13 mars 2019, texte 3)
- Agrément aux collectivités (Journal officiel du 13 mars 2019, texte 3)
- Laboratoire Ferring
Pour aller plus loin
Avis de la Commission de la Transparence - REKOVELLE (HAS, 5 avril 2017)
Avis de la Commission de la Transparence - REKOVELLE en stylo prérempli (HAS, 27 septembre 2017)
Etude pivot :
Andersen et al., Individualized versus conventional ovarian stimulation for in vitro fertilization : a multicenter, randomized, controlled, assessor-blinded, phase 3 noninferiority trial, Fertility and Sterility, 2017, 107(2), 387-396 (pdf)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)
.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.