Plaque d'athérome sur la paroi d'une artère (illustration).
LOJUXTA gélule est un hypolipémiant dont le principe actif est une nouvelle substance, le lomitapide.
Il s'agit d'un inhibiteur sélectif de la protéine microsomale de transfert des triglycérides (PMT), une protéine intracellulaire de transfert de lipides qui assure la liaison et le transport de molécules individuelles de lipides entre les membranes.
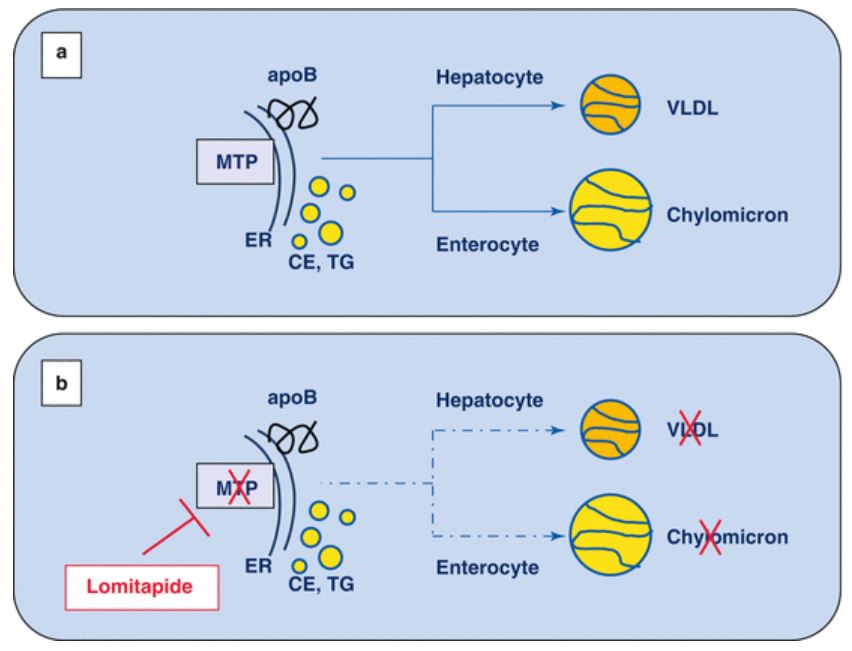
La PMT joue un rôle clé dans l'assemblage des lipoprotéines contenant de l'Apo B dans le foie et les intestins (Fig. 1a).
L'inhibition de la PMT diminue la sécrétion de lipoprotéines et les concentrations circulantes de lipides transportés par des lipoprotéines, notamment du cholestérol et des triglycérides (Fig. 1b).
Figure 1 - Rôle du MTP dans la biosynthèse des VLDL et du chylomicrons et effet de l'inhibition du MTP par le lomitapide (source : ThoracicKey.com)
LOJUXTA est indiqué, en complément d'un régime alimentaire pauvre en graisses et d'autres médicaments hypolipémiants, avec ou sans aphérèse des lipoprotéines de basse densité (LDL), chez des patients adultes présentant une hypercholestérolémie familiale homozygote (HFHo).
L'HFHo doit être confirmée par un test génétique dans la mesure du possible. D'autres formes d'hyperlipoprotéinémies primaires et les causes secondaires d'hypercholestérolémie (syndrome néphrotique, hypothyroïdisme, par exemple) doivent être exclues.
 LOJUXTA fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.
LOJUXTA fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de santé déclarent tout effet indésirable suspecté.Une baisse significative du LDLc, à interpréter avec prudence
Dans son avis du 8 janvier 2014, la Commission de la Transparence a évalué l'efficacité de LOJUXTA sur la base d'une étude de phase III (AEGR-733-012), non comparative, en ouvert, ayant évalué l'effet de l'ajout du lomitapide à un traitement hypolipémiant stable depuis au moins 6 semaines (incluant statine, ézétimibe, fibrate, cholestyramine, niacine et aphérèse), chez 29 patients avec HFHo.
Le critère principal de jugement était le pourcentage de réduction des taux de LDL-c à 26 semaines par rapport au taux à l'inclusion.
Un suivi de la tolérance jusqu'à 78 semaines était également prévu.
A l'issue de 26 semaines de suivi, une réduction significative des taux de LDL-c a été rapportée suite à l'ajout de lomitapide aux traitements hypolipémiants en cours (23 des 29 patients inclus dans l'analyse d'efficacité ont terminé l'étude) :
- taux de LDL-c moyen à l'inclusion = 3,364 g/L [1,52 ; 5,64] ;
- taux de LDL-c moyen à la fin de l'étude = 1,896 g/L [1,499 ; 2,292] ;
- soit une réduction de 40,1% [-51,9, -28,2], p < 0,001.
Tenant compte de la méthodologie de cette étude (non comparative, en ouvert, effectif faible), la Commission considère que "ces résultats sont à interpréter avec prudence".
Elle "regrette l'absence de bras comparateur dans cette étude et le choix de méthodologie en « ouvert » fait par le laboratoire qui ne permet pas d'apprécier la quantité d'effet observée d'autant qu'une étude de type croisé aurait pu être réalisée avec un faible nombre de sujets".
En termes de tolérance, les principaux effets indésirables rapportés pendant cette étude étaient d'ordre gastro-intestinal (93 %) : diarrhée (79 %), nausées (65 %), dyspepsie (38 %), vomissements (34 %), douleurs, gênes ou distensions abdominales, constipation et flatulences (20 %). Des infections ont également été rapportées avec une fréquence de 58,6 % (grippe, nasopharyngite, gastroentérite).
L'effet indésirable le plus grave observé pendant le traitement a été une élévation anormale des transaminases (ALAT) survenue chez 7 % des patients.
Les données issues de la phase de suivi à 126 semaines, qui a inclus 19/29 patients (65 %) ayant terminé les 78 semaines de suivi de l'étude pivot, montrent que l'effet du lomitapide a été maintenu avec une réduction significative des taux de LDL-c observée avec l'ajout de lomitapide aux traitements hypolipémiants en cours :
- taux de LDL-c moyen à l'inclusion de 3,364 g/L [1,52 ; 5,64],
- taux de LDL-c moyen à 126 semaines de 1,89 g/L [1,27 ; 2,50],
- réduction de 45,5 % [-61,6, -29,4], p < 0,001.
SMR important, ASMR mineure, médicament de dernière intention
Sur la base des données disponibles au moment de cette évaluation, la Commission de la Transparence estime que LOJUXTA est un médicament de dernière intention à réserver aux patients avec hypercholestérolémie familiale homozygote non contrôlée malgré un traitement hypolipémiant optimal, à dose maximale, avec ou sans aphérèse.
LOJUXTA bénéficie d'un service médical rendu (SMR) important, et d'une amélioration du service médical rendu mineure (ASMR IV).
La population cible des patients avec HFHo en France est estimée de 100 à 150 patients. La proportion de ces patients non contrôlés par les hypolipémiants disponibles sur le marché n'est pas connue. La Commission considère que "la population cible de LOJUXTA est au maximum de 100 patients".
A noter qu'il n'existe pas d'autre traitement indiqué en association aux traitements hypolipémiants à doses maximales chez des patients avec HFHo non contrôlée.
Plan de gestion des risques, notamment hépatiques
La commercialisation de LOJUXTA s'accompagne d'un plan de gestion des risques (PGR) qui prévoit la surveillance de certains risques identifiés comme importants ou potentiels et signale les données manquantes relatives à son utilisation chez certains patients (Cf. Tableau I).
A ce titre, LOJUXTA est contre-indiqué chez les patients présentant une insuffisance hépatique modérée ou sévère et les patients dont les tests de la fonction hépatique sont anormaux de façon prolongée et inexpliquée.
Si les résultats des tests hépatiques avant traitement sont anormaux, l'instauration du traitement par ce médicament ne doit être envisagée qu'après une investigation appropriée réalisée par un hépatologue et seulement lorsque les anomalies avant traitement sont expliquées ou résolues.
Un bilan hépatique doit être réalisé :
Sur la base des données disponibles au moment de cette évaluation, la Commission de la Transparence estime que LOJUXTA est un médicament de dernière intention à réserver aux patients avec hypercholestérolémie familiale homozygote non contrôlée malgré un traitement hypolipémiant optimal, à dose maximale, avec ou sans aphérèse.
LOJUXTA bénéficie d'un service médical rendu (SMR) important, et d'une amélioration du service médical rendu mineure (ASMR IV).
La population cible des patients avec HFHo en France est estimée de 100 à 150 patients. La proportion de ces patients non contrôlés par les hypolipémiants disponibles sur le marché n'est pas connue. La Commission considère que "la population cible de LOJUXTA est au maximum de 100 patients".
A noter qu'il n'existe pas d'autre traitement indiqué en association aux traitements hypolipémiants à doses maximales chez des patients avec HFHo non contrôlée.
Plan de gestion des risques, notamment hépatiques
La commercialisation de LOJUXTA s'accompagne d'un plan de gestion des risques (PGR) qui prévoit la surveillance de certains risques identifiés comme importants ou potentiels et signale les données manquantes relatives à son utilisation chez certains patients (Cf. Tableau I).
Tableau I - Risques identifiés et informations manquantes selon le PGR de JOLUXTA
| Risques importants identifiés | Effets hépatiques (élévation des ALAT, stéatoses) Troubles gastro-intestinaux (nausées, diarrhées, perte de poids, malabsorption) Interaction avec les statines |
| Risques potentiels identifiés | Fibrose hépatique Tumeur hépatique primaire Tumeurs intestinales Tumeurs pancréatiques Mésusage Grossesse |
| Données manquantes | Utilisation pendant la grossesse, chez les enfants, avec l'alcool, chez les patients non caucasiens Maladie hépatique préexistante, utilisation concomitante avec des agents hépatotoxiques, interactions avec les inhibiteurs du CYP3A4 |
A ce titre, LOJUXTA est contre-indiqué chez les patients présentant une insuffisance hépatique modérée ou sévère et les patients dont les tests de la fonction hépatique sont anormaux de façon prolongée et inexpliquée.
Si les résultats des tests hépatiques avant traitement sont anormaux, l'instauration du traitement par ce médicament ne doit être envisagée qu'après une investigation appropriée réalisée par un hépatologue et seulement lorsque les anomalies avant traitement sont expliquées ou résolues.
Un bilan hépatique doit être réalisé :
- Avant traitement : mesure des taux des enzymes ALAT, ASAT, phosphatases alcalines, de la bilirubine totale, de la gamma-glutamyl transférase (gamma-GT) et de l'albumine sérique.
- Pendant la première année de traitement : mesure des valeurs des tests hépatiques (au minimum les taux d'ALAT et d'ASAT), avant chaque augmentation de dose ou 1 fois par mois, selon l'échéance qui se présente en premier.
- Après la première année : mêmes analyses tous les 3 mois et avant toute augmentation de dose.
Dans le cadre de ce PGR, un kit de formation doit être fourni par le laboratoire à tous les médecins susceptibles de prescrire ou d'utiliser le lomitapide.
LOJUXTA en pratique
Le traitement doit être instauré et surveillé par un médecin qualifié dans la prise en charge des patients atteints de dyslipidémie.
LOJUXTA est disponible sous 3 dosages : 5 mg, 10 mg et 20 mg.
La posologie initiale recommandée est de 5 mg 1 fois par jour.
Après 2 semaines, la dose peut être augmentée, sur la base d'une sécurité et d'une tolérance acceptables, à 10 mg, puis, à des intervalles d'au moins 4 semaines, à 20 mg, 40 mg et jusqu'à la dose maximale recommandée de 60 mg.
La dose doit être augmentée progressivement, afin de minimiser l'incidence et la gravité des effets indésirables gastro-intestinaaux et l'augmentation des aminotransférases.
Les patients doivent prendre quotidiennement, et pendant toute la durée du traitement par LOJUXTA, des compléments alimentaires apportant 400 UI de vitamine E et approximativement 200 mg d'acide linoléique, 110 mg d'acide eicosapentaénoïque (AEP), 210 mg d'acide alpha-linolénique (AAL) et 80 mg d'acide docosahexaénoïque (ADH).
Cas particuliers : association avec l'atorvastatine ou les inhibiteurs du CYP3A4
Le traitement doit être instauré et surveillé par un médecin qualifié dans la prise en charge des patients atteints de dyslipidémie.
LOJUXTA est disponible sous 3 dosages : 5 mg, 10 mg et 20 mg.
La posologie initiale recommandée est de 5 mg 1 fois par jour.
Après 2 semaines, la dose peut être augmentée, sur la base d'une sécurité et d'une tolérance acceptables, à 10 mg, puis, à des intervalles d'au moins 4 semaines, à 20 mg, 40 mg et jusqu'à la dose maximale recommandée de 60 mg.
La dose doit être augmentée progressivement, afin de minimiser l'incidence et la gravité des effets indésirables gastro-intestinaaux et l'augmentation des aminotransférases.
Les patients doivent prendre quotidiennement, et pendant toute la durée du traitement par LOJUXTA, des compléments alimentaires apportant 400 UI de vitamine E et approximativement 200 mg d'acide linoléique, 110 mg d'acide eicosapentaénoïque (AEP), 210 mg d'acide alpha-linolénique (AAL) et 80 mg d'acide docosahexaénoïque (ADH).
LOJUXTA présente des interactions médicamenteuses avec les substances suivantes :
- les inhibiteurs du CYP3A4 : augmentation de l'exposition au lomitapide,
- les inducteurs du CYP3A4 : diminution de l'effet du lomitapide,
- les satines : augmentation des concentrations plasmatiques des statines et augmentation du risque d'effets indésirables (rhabdomyolyse),
- la warfarine : augmentation des concentrations plasmatiques de warfarine. L'INR doit être surveillé régulièrement.
L'ensemble de ces interactions doit être pris en compte, par exemple chez les patients traités par atorvastatine et recevant une dose d'entretien stable de LOJUXTA, il faut :
- soit réduire la dose de LOJUXTA de moitié. Les patients traités par 5 mg doivent rester à 5 mg.
La dose peut ensuite être augmentée avec prudence en fonction de la réponse en LDL-c et de la sécurité/tolérance.
Lors de l'arrêt de l'atorvastatine, la dose de LOJUXTA doit être augmentée progressivement par paliers, en fonction de la réponse en LDL-c et de la sécurité/tolérance.
Autre exemple, en cas de traitement concomitant avec un inhibiteur faible du CYP3A4, il faut espacer la prise des médicaments (LOJUXTA et l'inhibiteur faible du CYP3A4) de 12 heures.
Conseils aux patients
LOJUXTA doit être pris à jeun, au moins 2 heures après le repas du soir ; la teneur en graisses d'un repas récent peut avoir un effet défavorable sur sa tolérance gastro-intestinale.
L'administration avec des aliments peut augmenter l'exposition au lomitapide. La survenue et la gravité des effets indésirables gastro-intestinaux diminuent avec un régime alimentaire pauvre en graisses. Les patients doivent suivre un régime apportant moins de 20 % des calories sous forme de graisses avant de commencer le traitement et poursuivre ce régime pendant le traitement.
Des conseils diététiques sont recommandés.
Le jus de pamplemousse doit être supprimé du régime alimentaire pendant le traitement par LOJUXTA.
La consommation d'alcool n'est pas recommandée.
Les patients traités par LOJUXTA sont exposés à un risque de déshydratation liée aux réactions indésirables gastro-intestinales. Les patients doivent en être informés et prendre des précautions pour éviter une déplétion hydrique.
LOJUXTA et contraception
LOJUXTA peut diminuer l'efficacité des contraceptifs oraux à base d'estrogènes, en raison de diarrhées et/ou de vomissements.
Il faut en informer les patientes concernées car des mesures contraceptives supplémentaires doivent être prises, jusqu'à la disparition des symptômes.
Identité administrative
Lors de l'arrêt de l'atorvastatine, la dose de LOJUXTA doit être augmentée progressivement par paliers, en fonction de la réponse en LDL-c et de la sécurité/tolérance.
Autre exemple, en cas de traitement concomitant avec un inhibiteur faible du CYP3A4, il faut espacer la prise des médicaments (LOJUXTA et l'inhibiteur faible du CYP3A4) de 12 heures.
Conseils aux patients
LOJUXTA doit être pris à jeun, au moins 2 heures après le repas du soir ; la teneur en graisses d'un repas récent peut avoir un effet défavorable sur sa tolérance gastro-intestinale.
L'administration avec des aliments peut augmenter l'exposition au lomitapide. La survenue et la gravité des effets indésirables gastro-intestinaux diminuent avec un régime alimentaire pauvre en graisses. Les patients doivent suivre un régime apportant moins de 20 % des calories sous forme de graisses avant de commencer le traitement et poursuivre ce régime pendant le traitement.
Des conseils diététiques sont recommandés.
Le jus de pamplemousse doit être supprimé du régime alimentaire pendant le traitement par LOJUXTA.
La consommation d'alcool n'est pas recommandée.
Les patients traités par LOJUXTA sont exposés à un risque de déshydratation liée aux réactions indésirables gastro-intestinales. Les patients doivent en être informés et prendre des précautions pour éviter une déplétion hydrique.
LOJUXTA peut diminuer l'efficacité des contraceptifs oraux à base d'estrogènes, en raison de diarrhées et/ou de vomissements.
Il faut en informer les patientes concernées car des mesures contraceptives supplémentaires doivent être prises, jusqu'à la disparition des symptômes.
Identité administrative
- Liste I
- Prescription hospitalière, réservée aux spécialistes et services de cardiologie, diabétologie, endocrinologie, maladies métaboliques et médecine interne
- LOJUXTA 5 mg gélule, flacon de 28, CIP 3400927625992
- LOJUXTA 10 mg gélule, flacon de 28, CIP 3400927626074
- LOJUXTA 20 mg gélule, flacon de 28, CIP 3400927626135
- Remboursement à 65 % (Journal officiel du 15 novembre 2018 - texte 13)
- Prix public TTC = 20 607,46 euros TTC
- Agrément aux collectivités (Journal officiel du 15 novembre 2018 - texte 14)
- Laboratoire Amryt Pharmaceuticals
Pour aller plus loin
Avis de la Commission de la Transparence - LOJUXTA (1er juillet 2015)
Avis de la Commission de la Transparence - LOJUXTA (8 janvier 2014)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 8 minutes
8 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.