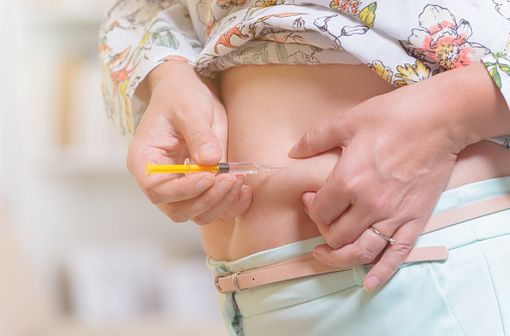
L'injection sous-cutanée de l'énoxaparine doit être réalisée dans le tissu cellulaire sous-cutané de la ceinture abdominale alternativement du côté droit et du côté gauche (illustration).
EDIT du 5 mars 2019 : Mise à disposition depuis le 1er mars 2019 :
/FIN EDIT
Tensions d'approvisionnement dues à une forte demande au niveau mondial
Dans une lettre en date du 7 décembre 2018 à destination des professionnels de santé, le laboratoire Sanofi indique être confronté à des tensions d'approvisionnement régulières en LOVENOX (énoxaparine sodique), dans un contexte de forte demande sur le marché des héparines au niveau mondial.
Cette situation a pu impacter la capacité de Sanofi à livrer les quantités commandées et occasionner des ruptures de stocks ponctuelles pour les dosages suivants : 4 000 UI (40 mg)/0,4 ml, 6 000 UI (40 mg)/0,6 ml, 8 000 UI (40 mg)/0,8 ml (Cf. Encadré 1).
Mise à disposition d'unités destinées à l'Autriche et à l'Italie
Dans l'attente de la remise à disposition normale de cette héparine de bas poids moléculaire (HBPM), prévue en janvier 2019, le laboratoire souhaite renforcer le marché français en LOVENOX afin d'éviter des ruptures de prise en charge chez les patients concernés.
A ce titre, Sanofi met à disposition de manière exceptionnelle et transitoire, en accord avec l'ANSM, des unités de LOVENOX solution injectable en seringue préremplie initialement destinées à d'autres marchés européens (Cf. Tableau I).
Ces unités sont distribuées auprès des pharmacies à usage intérieur (PUI) depuis le 10 décembre 2018. Aussi, les commandes passées lors des prochaines semaines pourront être honorées avec ces seringues.
Concernant LOVENOX 4 000 UI (40 mg)/0,4 mL (UCD 3400892669236), la pharmacie pourra recevoir des conditionnements autrichiens (LOVENOX 40 MG/0,4 mL) ou italiens (CLEXANE 4KIU/0,4 mL).
Produits similaires, conditionnements différents
Pour ces présentations initialement destinées à l'Autriche et à l'Italie, les seringues sont strictement identiques en termes de produit et issues des mêmes usines que les seringues LOVENOX destinées à la France.
Leur dispositif de sécurité diffère légèrement par le fait qu'il nécessite d'appuyer plus fort sur le piston, mais il bénéficie également d'un système de sécurité automatique.
Selon le pays de destination initial, leur conditionnement est par ailleurs rédigé en italien ou en autrichien. Ils ne comportent ni datamatrix, ni code UCD : les codes UCD habituels devront être utilisés pour les commandes.
Enfin, pour les présentations LOVENOX 4 000 UI initialement destinées à l'Autriche, les seringues sont conditionnées par boîte de 10 au lieu de 6.
En annexe de sa lettre aux professionnels de santé, le laboratoire Sanofi joint des informations pratiques concernant les commandes des boîtes de LOVENOX initialement destinées à l'Italie et à l'Autriche.
Dans le cas où les mesures mises en place ne permettraient pas de répondre à l'intégralité des besoins en LOVENOX, le laboratoire recommande de prévoir le recours aux autres HBPM disponibles.
Pour aller plus loin
LOVENOX 4 000 UI (40 mg)/0,4 ml, 6 000 UI (40 mg)/0,6 ml, 8 000 UI (40 mg)/0,8 ml, solution injectable en seringue préremplie - Tensions d'approvisionnement (ANSM, 11 décembre 2018, mise à jour le 18 février 2019, mise à jour le 1er mars 2019)
Lettre aux professionnels de santé - LOVENOX (sur le site de l'ANSM, 11 décembre 2018, mis à jour le 18 février 2019)
- d'unités de la spécialité CLEXANE 4 000 anti Xa/0,4 mL initialiement destinées au marché turc (boîte de 10 seringues),
- d'unités de la spécialité CLEXANE 6 000 anti Xa/0,6 mL et 8 000 anti Xa/0,8 mL initialement destinées au marché allemand (boîtes de 12 seringues).
- strictement identiques en termes de produit à la version LOVENOX française,
- issues des mêmes usines que les seringues de la version LOVENOX française,
- ont le même dispositif de sécurité automatique que les seringues des spécialités LOVENOX françaises.
/FIN EDIT
Tensions d'approvisionnement dues à une forte demande au niveau mondial
Dans une lettre en date du 7 décembre 2018 à destination des professionnels de santé, le laboratoire Sanofi indique être confronté à des tensions d'approvisionnement régulières en LOVENOX (énoxaparine sodique), dans un contexte de forte demande sur le marché des héparines au niveau mondial.
Cette situation a pu impacter la capacité de Sanofi à livrer les quantités commandées et occasionner des ruptures de stocks ponctuelles pour les dosages suivants : 4 000 UI (40 mg)/0,4 ml, 6 000 UI (40 mg)/0,6 ml, 8 000 UI (40 mg)/0,8 ml (Cf. Encadré 1).
Encadré 1 - Indications thérapeutiques de LOVENOX 4 000 UI (40 mg)/0,4 ml, 6 000 UI (40 mg)/0,6 ml, 8 000 UI (40 mg)/0,8 ml
|
LOVENOX est indiqué chez l'adulte dans :
|
Dans l'attente de la remise à disposition normale de cette héparine de bas poids moléculaire (HBPM), prévue en janvier 2019, le laboratoire souhaite renforcer le marché français en LOVENOX afin d'éviter des ruptures de prise en charge chez les patients concernés.
A ce titre, Sanofi met à disposition de manière exceptionnelle et transitoire, en accord avec l'ANSM, des unités de LOVENOX solution injectable en seringue préremplie initialement destinées à d'autres marchés européens (Cf. Tableau I).
Tableau I - Liste des unités de LOVENOX destinées aux autres marchés européens et mises à disposition en France
| Produits | Marché initial |
| LOVENOX 40MG/0,4ML INJ PS10 | Autriche |
| CLEXANE 4KIU/0,4ML INJ PS6 | Italie |
| LOVENOX 60MG/0,6ML INJ PS10 | Autriche |
| LOVENOX 80MG/0,8ML INJ PS10 | Autriche |
Ces unités sont distribuées auprès des pharmacies à usage intérieur (PUI) depuis le 10 décembre 2018. Aussi, les commandes passées lors des prochaines semaines pourront être honorées avec ces seringues.
Concernant LOVENOX 4 000 UI (40 mg)/0,4 mL (UCD 3400892669236), la pharmacie pourra recevoir des conditionnements autrichiens (LOVENOX 40 MG/0,4 mL) ou italiens (CLEXANE 4KIU/0,4 mL).
Produits similaires, conditionnements différents
Pour ces présentations initialement destinées à l'Autriche et à l'Italie, les seringues sont strictement identiques en termes de produit et issues des mêmes usines que les seringues LOVENOX destinées à la France.
Leur dispositif de sécurité diffère légèrement par le fait qu'il nécessite d'appuyer plus fort sur le piston, mais il bénéficie également d'un système de sécurité automatique.
Selon le pays de destination initial, leur conditionnement est par ailleurs rédigé en italien ou en autrichien. Ils ne comportent ni datamatrix, ni code UCD : les codes UCD habituels devront être utilisés pour les commandes.
Enfin, pour les présentations LOVENOX 4 000 UI initialement destinées à l'Autriche, les seringues sont conditionnées par boîte de 10 au lieu de 6.
En annexe de sa lettre aux professionnels de santé, le laboratoire Sanofi joint des informations pratiques concernant les commandes des boîtes de LOVENOX initialement destinées à l'Italie et à l'Autriche.
Dans le cas où les mesures mises en place ne permettraient pas de répondre à l'intégralité des besoins en LOVENOX, le laboratoire recommande de prévoir le recours aux autres HBPM disponibles.
Pour aller plus loin
LOVENOX 4 000 UI (40 mg)/0,4 ml, 6 000 UI (40 mg)/0,6 ml, 8 000 UI (40 mg)/0,8 ml, solution injectable en seringue préremplie - Tensions d'approvisionnement (ANSM, 11 décembre 2018, mise à jour le 18 février 2019, mise à jour le 1er mars 2019)
Lettre aux professionnels de santé - LOVENOX (sur le site de l'ANSM, 11 décembre 2018, mis à jour le 18 février 2019)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
- Embolie pulmonaire
- HBPM et fondaparinux (traitement par)
- Infarctus cérébral
- Syndrome coronarien aigu ST-
- Syndrome coronarien aigu ST+ (Infarctus du myocarde)
- Thrombose veineuse profonde : prophylaxie en milieu médical
- Thrombose veineuse profonde : prophylaxie en chirurgie
- Thrombose veineuse profonde : traitement
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)
.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.