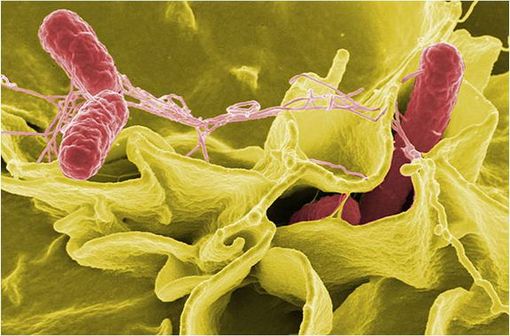
Le germe le plus souvent responsable de typhoïde est Salmonella typhi (illustration @Wikimedia).
Arrêt de commercialisation du vaccin contre la typhoïde TYPHERIX
Le laboratoire GlaxoSmithKline a arrêté la commercialisation du vaccin contre la typhoïde TYPHERIX solution injectable en seringue préremplie.
Selon les informations disponibles dans le Répertoire des spécialités pharmaceutiques de l'ANSM, l'arrêt de commercialisation a été déclaré le 30 novembre 2017.
A ce jour, TYPHERIX n'est plus disponible et son autorisation de mise sur le marché (AMM) a été abrogée le 20 mars 2018.
Quelles alternatives ?
TYPHERIX était indiqué pour l'immunisation active contre la fièvre typhoïde à la fois chez les adultes et chez les enfants âgés de deux ans et plus (Cf. VIDAL Reco "Voyage : recommandations sanitaires").
A ce jour, il reste sur le marché des vaccins 2 spécialités permettant de prévenir la fièvre typhoïde :
- le vaccin TYPHIM VI (Sanofi Pasteur), indiqué en prévention de la fièvre typhoïde chez l'adulte et l'enfant de plus de 2 ans, en particulier : voyageurs se rendant en zone d'endémie, migrants, personnel de santé, militaires.
- le vaccin TYAVAX (Sanofi Pasteur), un vaccin combiné typhoïdique et hépatite A. Il est indiqué chez les sujets âgés de 16 ans et plus.
Sur VIDAL.fr
Vaccin TYPHERIX : les lots disponibles pourront être distribués jusqu'au 30 septembre 2017 (7 septembre 2017)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 1 minute
1 minute Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.