Le microbiote intestinal d'un être humain contient environ 100 000 milliards de bactéries, toutes dotées d'un génome (illustration).
La transplantation de microbiote intestinal ("greffe fécale", ou greffe de flore intestinale, voir notre article) a déjà fait ses preuves dans le traitement de l'infection à Clostridium difficile, en administration unique à partir d'un seul donneur. Son efficacité dans le traitement de la rectocolite hémorragique (RCH) a fait l'objet de diverses études, dont certaines randomisées, sans preuves convaincantes.
Pourtant, des études semblent pointer le rôle du microbiote dans la pathogenèse de la RCH , en particulier celui des bactéries de la famille des Fusobacterium (Gastroenterology. 2014).
Greffe fécale dans la RCH : l'hypothèse du besoin d'un traitement renforcé
Parce que les études existantes sur l'efficacité de la transplantation de microbiote dans la RCH reprenaient le protocole du traitement de l'infection à clostridies (donneur unique, administration unique, au mieux hebdomadaire), des chercheurs australiens se sont interrogés sur l'éventuelle efficacité d'un traitement renforcé (donneurs multiples, administrations quasi quotidiennes) dans cette pathologie. Ils viennent de publier leurs résultats dans The Lancet.
Un essai clinique randomisé en double aveugle avec traitement intensif (lavements répétés)
Pour évaluer cette hypothèse, ils sont conçus un essai clinique randomisé en double aveugle mesurant l'efficacité clinique et endoscopique de l'administration de mélanges de microbiotes (entre 3 et 7 donneurs, issus d'une quarantaine de personnes en bonne santé).
Ce traitement, sous forme de suspension liquide, et le placebo (liquide de même couleur et même odeur que celui réalisé à partir de mélanges de microbiotes) ont d'abord été administrés par coloscopie (celle permettant de noter les lésions initiales) au niveau de l'iléon terminal ou du cæcum.
Ensuite, les patients ont été invités à s'administrer le même mélange liquide (mêmes donneurs) sous forme de lavement, 5 fois par semaine, pendant 8 semaines, soit un total de 40 administrations.
| Les lavements sont une solution simple mais, disons, peu ragoûtante, surtout 5 fois par semaine. Des expériences sont cependant actuellement en cours pour faire des "gélules de microbiote de donneur(s)". Dans cette étude par exemple, publiée dans le JAMA en 2014, les participants ont pu modifier leur microbiote pour lutter contre une infection à Clostridium difficile en ingérant des capsules gastro-résistantes (délivrant leur contenu dans le colon) et contenant du microbiote de donneur concentré, congelé puis décongelé : les matières fécales données ont été brassées, tamisées, centrifugées et mises en suspension sous forme concentrée dans une solution saline stérile avec 10 % de glycérol. La suspension a été ensuite doublement encapsulée dans des gélules d'hypromellose, puis stockée à - 80 ° C en attendant l'utilisation (stockage possible pendant 6 mois) Les gélules pesaient en moyenne 1,6 gramme et contenaient la même quantité de bactéries que 48 g de matières fécales. Elles ont été ensuite prises à température ambiante. |
Un critère d'efficacité primaire strictement défini
Cette étude a inclus 85 patients adultes atteints de RCH modérée (score de Mayo de 4 à 10) et a été menée dans trois hôpitaux australiens. Les auteurs ont choisi un critère d'efficacité primaire restrictif : amélioration clinique et endoscopique en l'absence de traitement corticostéroïde à 8 semaines (score de Mayo inférieur ou égal à 2, chaque sous-score inférieur ou égal à 1), ce qui impliquait, pour de nombreux patients, un sevrage aux corticoïdes pendant la durée de l'étude.
Des critères secondaires ont également été déterminés : réponse ou rémission clinique, réponse ou rémission endoscopique, etc.
Rémission clinique chez près d'1 patient sur 2 du groupe "microbiotes"
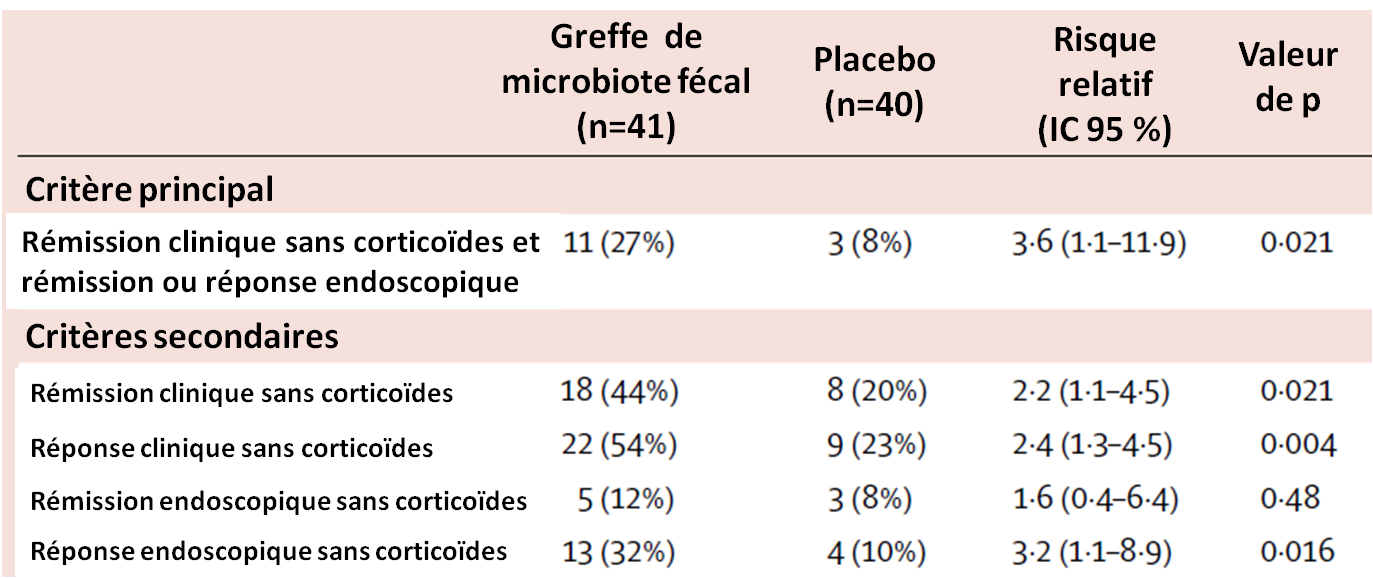
L'analyse des résultats en intention de traiter montre que le critère d'efficacité primaire a été atteint chez 27 % des patients recevant un mélange de microbiotes, contre 8 % des patients recevant le placebo (p = 0,021). De plus, lorsque ces derniers ont reçu un mélange de microbiotes en étude ouverte après les 8 semaines de traitement en double aveugle, le même pourcentage d'efficacité primaire a été observé.
Dès la 4ème semaine d'étude, une réponse clinique a été observée chez 32 % des patients traités contre 10 % du groupe placebo. À 8 semaines, une rémission clinique a été observée chez 44 % des patients traités (20 % dans le groupe placebo) et une réponse clinique chez 54 % des patients traités (23 % placebo).
Sur le plan endoscopique, les patients traités ont présenté davantage de réponse (32 % vs. 10 %), mais aucune différence significative statistiquement n'a été observée entre les deux groupes en terme de rémission endoscopique (définie par un score de Mayo = 0 sans corticothérapie) : 12 % vs 8 % :
Des rémissions parfois spectaculaires, mais des réponses plutôt moins complètes lorsque la sévérité s'accroît
La rémission a parfois été spectaculaire, comme chez ces deux femmes dont les endoscopies sont présentées ci-dessous :
- La première femme, de 37 ans, présentait des diarhhées sanglantes 6 fois par jour au début de l'étude, malgré la prise de dérivés aminosalicylés ;
- la seconde femme, de 28 ans, après plusieurs échecs thérapeutiques, subissait au démarrage de l'étude 8 épisodes de diarhhées sanglantes par jour, avec des douleurs abdominales, sous azathioprine et corticoïdes oraux.
Voici donc les résultats obtenus après 8 semaines de traitement par greffe de microbiotes mélangés, sachant que la deuxième femme a dû continuer les corticoïdes (et n'a donc pas rempli le critère principal de l'étude) :
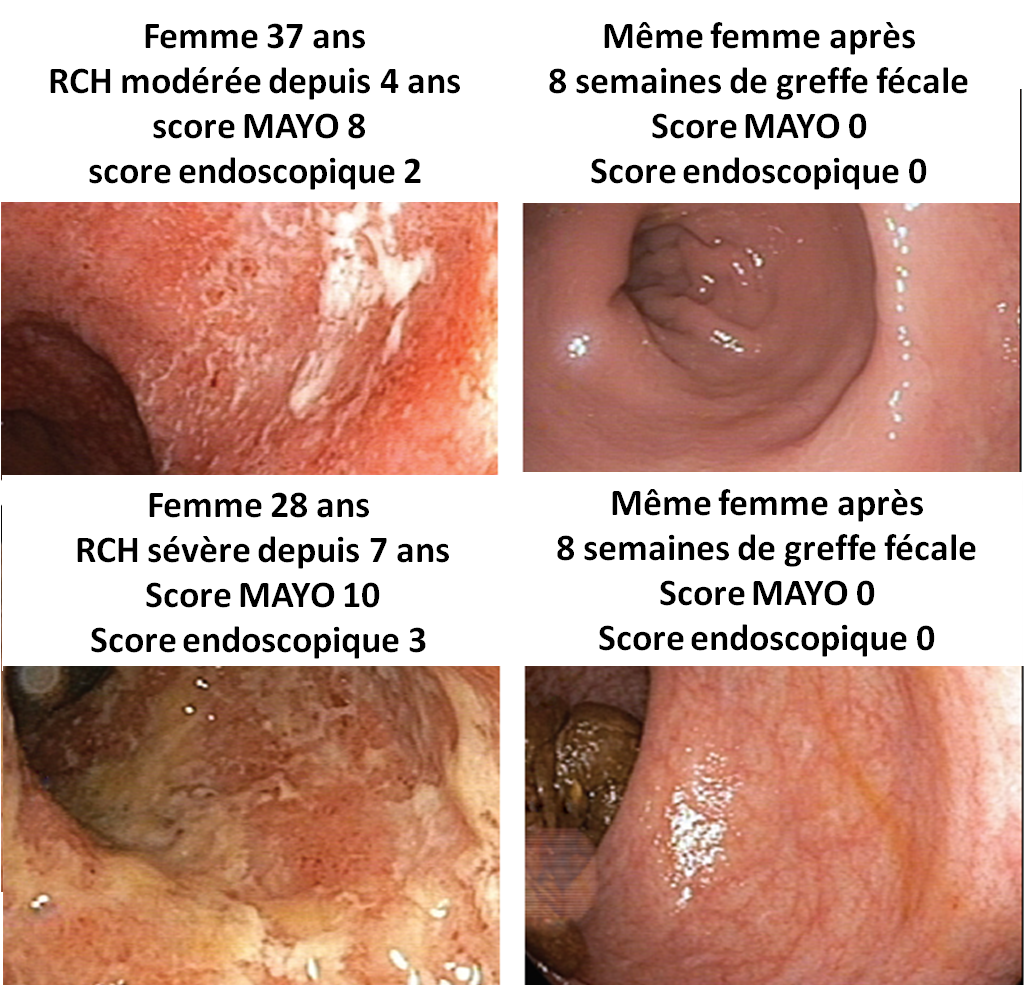
Les auteurs ont constaté que, globalement, l'efficacité du traitement semblait inversement proportionnelle à la sévérité de la RCH et à la dépendance aux corticostéroïdes au moment du recrutement.
Constat de modifications durables de la composition du microbiote
L'analyse séquencée de l'ARN ribosomique (rRNA) des microbiotes avant et après traitement montre le passage d'une dominance des Bacteroides ssp. à une dominance des Prevotella ssp. Certaines familles de bactéries ont été davantage observées chez les patients dont la clinique était améliorée : Barnesiella ssp., Parabacteroides ssp., Ruminococcus ssp., Blautia ssp., par exemple.
Une plus grande diversité du microbiote a également été observée chez les patients traités.
Ces changements ont persisté jusqu'à 8 semaines après la fin du traitement.
La présence de deux familles de bactéries associée à une moindre efficacité
Les bactéries des familles Fusobacterium ssp. et Sutterella ssp. étaient particulièrement fréquentes chez les patients n'ayant présenté aucun bénéfice.
Aucune différence d'efficacité n'a été observée par les auteurs entre les différents mélanges de microbiotes administrés (mais l'étude était de trop petite taille pour en tirer des conclusions définitives). Cependant le microbiote d'un donneur a été davantage associé à une efficacité clinique que ceux des autres donneurs.
Des effets indésirables similaires entre les groupes
Des effets indésirables digestifs légers à modérés ont été observés chez 78 % des patients traités et 83 % de ceux recevant le placebo. Néanmoins, les auteurs décrivent un cas d'aggravation rapide en début de traitement (groupe traité) ayant nécessité une colectomie partielle et s'inquiètent d'un potentiel effet aggravant de la procédure.
Les patients ayant dû quitter l'étude avant la fin étaient essentiellement des patients dont la maladie s'est aggravée lors du sevrage des corticostéroïdes, sevrage nécessaire du fait du choix du critère d'efficacité primaire.
Les auteurs concluent en insistant sur la nécessité d'études additionnelles, tant sur le rythme et la durée du traitement selon la sévérité des symptômes, que sur un éventuel choix de donneurs en fonction du microbiote initial des patients. Des incertitudes demeurent également sur la nécessité de traitements de rappel réguliers.
Rappelons que nous ne sommes qu'au début de l'étude du microbiote et de son impact sur l'inflammation, le psychisme et autres symptômes ou pathologies (voir notre article sur MetaGenopolis). Comme évoqué ci-dessus (cf. encadré), il est probable que les futures études se feront avec ingestion de gélules et non lavements itératifs, ce qui simplifiera l'observance, l'analyse des résultats et la reproductibilité. A suivre donc !
Pour aller plus loin
L'étude du Lancet sur cet essai clinique
Paramsothy S et al. « Multidonor intensive faecal microbiota transplantation for active ulcerative colitis: a randomised placebo-controlled trial. » Lancet, 2017 Feb 14.
Une revue sur le rôle du microbiote dans les maladies inflammatoires chroniques de l'intestin
Kostic AD et al. « The microbiome in inflammatory bowel disease: current status and the future ahead. » Gastroenterology 2014; 146: 1489–99.
Le score de Mayo
Mayo-score UC-DAI (Ulcerative colitis Disease Activity Index), GETAID.
L'étude publiée dans le JAMA avec des gélules de microbiote de donneur
Yougster I et al., Oral, Capsulized, Frozen Fecal Microbiota Transplantation for Relapsing Clostridium difficile Infection, JAMA, novembre 2014
Sur VIDAL.fr :
Cancérologie : la composition de la flore intestinale influencerait l'efficacité de l'immunothérapie (novembre 2015)
Greffe de flore intestinale : les recommandations de l'ANSM pour améliorer la sécurité (juin 2014)
MetaGenoPolis, une initiative pour mieux comprendre les milliards de bactéries du microbiote intestinal (août 2013)
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 7 minutes
7 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.