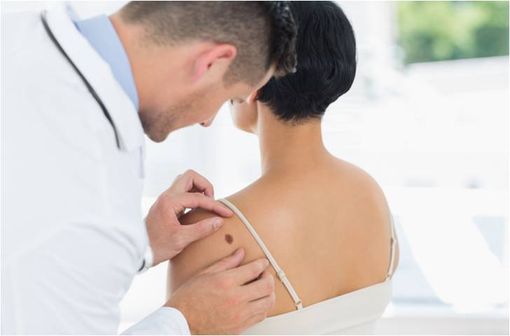
Le mélanome se forme dans environ 70 % des cas sur une peau auparavant indemne, et dans environ 30 % des cas sur un grain de beauté préexistant de type nævus (illustration).
Une analyse des événements indésirables liés à la radiothérapie rapportés lors de l'utilisation du vémurafénib a conduit les Autorités de santé à conclure que "la potentialisation de la toxicité radio-induite est un effet indésirable du vémurafénib".
L'analyse a porté sur 20 cas de lésions radio-induites, classés comme phénomène de rappel (voir Encadré 1) pour 8 cas et comme radiosensibilisation pour 12 autres cas.
La plupart des cas ont été de nature cutanée mais certains impliquaient toutefois des organes internes (voir Tableaux I et II).
| La dermite de rappel est une réactivation de la radiodermite aiguë survenant à distance (plusieurs mois à années) de l'irradiation. Une réaction inflammatoire réapparait limitée à la zone préalablement irradiée, provoquée par l'administration d'un traitement (chimiothérapie cytostatique mais aussi statines, anti tuberculeux, millepertuis, tamoxifene, antibiotiques, etc.), de façon indépendante de la dose de radiation et de l'intensité de la radiodermite lors de l'irradiation. |
"La nature et la sévérité des événements ont été évaluées dans les 20 cas comme étant majorées par rapport à ce qui est attendu au regard de la tolérance tissulaire normale à la radiothérapie", indique le laboratoire Roche dans une lettre adressée aux professionnels de santé en accord avec l'EMA (Agence européenne du médicament) et l'ANSM (Agence nationale de sécurité du médicament et des produits de santé).
Il est par ailleurs précisé dans cette lettre que, lors des essais cliniques de phase III et de phase IV sur le vémurafénib, l'incidence des lésions radio-induites observées a respectivement été de 5,2 % et 6 % (IC : [1,71-11,74] et [3,14-10,25]).
Dans la majorité des cas, les patients avaient reçu une radiothérapie à une dose supérieure ou égale à 2 Gy/jour.
Les 8 cas de phénomène de rappel ont consisté en une inflammation aiguë limitée à la zone précédemment irradiée, induite par l'administration de ZELBORAF au moins 7 jours après la fin de la radiothérapie (voir Tableau I).
| Organe affecté | Nombre de cas (n = 8) |
Manifestations cliniques | Délai moyen entre la fin de la radiothérapie et le début du traitement par ZELBORAF | Délai moyen entre l'administration de la dose initiale de ZELBORAF et l'apparition d'une réaction cutanée |
| Peau | 5 (62 %) |
Erythème Hyperkératose Lésions eczémateuses, vésiculaires et ulcératives |
31 jours (entre 21 et 42 jours) |
12 jours (entre 7 et 21 jours) |
| Poumon | 2 | Pneumopathie | 26 jours et 28 jours | 24 jours |
| Vessie | 1 | Cystite | 4 ans | 1 jour |
Les cas de "radiosensibilisation"
Douze cas de toxicité radio-induite (voir Tableau II) correspondaient à une radiosensibilisation survenue dans les circonstances suivantes :
- traitement par ZELBORAF pendant ou après la radiothérapie : à l'exception d'un cas, tous les patients avaient été traités par ZELBORAF pendant la radiothérapie ou dans les 3 jours suivant la fin de la radiothérapie ;
- survenue de la réaction après un délai moyen de 10 jours : lorsque celui-ci a été rapporté, le délai d'apparition de la réaction après initiation de la radiothérapie ou du traitement par ZELBORAF était compris entre 3 et 27 jours (moyenne = 10 jours, médiane = 8,5 jours).
| Organe affecté | Nombre de cas (n = 12) |
Manifestations cliniques | Evolution |
| Peau | 9 | Erythème Hyperkératose Lésions eczémateuses, vésiculaires et ulcératives |
Non précisée |
| Oesophage | 3 | Oesophagite radique dans 2 cas. Pour 1 des cas, aggravation d'une oesophagite de grade 1 à un grade 4 rapportée 10 jours après le début du traitement par ZELBORAF |
Fatale dans 2 cas |
| Foie | 1 | Nécrose radique 10 semaines après avoir reçu 20 Gy en exposition fractionnée sur le rachis thoracique pendant le traitement par ZELBORAF | Fatale |
| Rectum | 1 | Non précisées | Non précisée |
En conséquence
Au regard de ces données, le laboratoire Roche recommande aux professionnels de santé d'utiliser ZELBORAF avec prudence lorsqu'il est administré avant, pendant ou après une radiothérapie.
Cette précaution d'emploi ne figure pas actuellement dans le résumé des caractéristiques du produit de ZELBORAF (voir RCP de ZELBORAF sur le site de l'Agence européenne du médicament).
Pour mémoire
ZELBORAF 240 mg comprimé pelliculé (vémurafénib) est indiqué en monothérapie dans le traitement des patients adultes atteints d'un mélanome non résécable ou métastatique porteur d'une mutation BRAF V600 (Cf. Reco VIDAL Mélanome cutané).
Ce médicament est disponible en ville et à l'hôpital.
La prescription est hospitalière et réservée aux spécialistes en oncologie ou aux médecins compétents en cancérologie.
Une surveillance particulière pendant le traitement est requise.
Pour aller plus loin
Zelboraf® (vemurafenib) et risque de potentialisation de la toxicité radio-induite (ANSM, 19 octobre 2015)
Lettre aux oncologues, dermatologues, radiothérapeutes et pharmaciens hospitaliers et officinaux (sur le site de l'ANSM, 19 octobre 2015)
Review Vemurafenib-induced radiation recall dermatitis: case report and review of the literature. Dermatology. 2015 ; 230 (1) : 1-4 (abstract)

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire


Commentaires
Cliquez ici pour revenir à l'accueil.