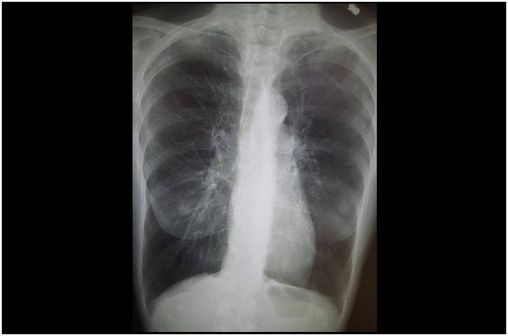
Radiographie pulmonaire montrant une BPCO sévère (illustration @Dr James Heilman, sur Wikimedia).
RELVAR ELLIPTA 92 µg/22 µg poudre pour inhalation en récipient unidose est indiqué :
- dans le traitement continu de l'asthme chez les adultes et les adolescents âgés de 12 ans et plus, dans les situations où l'utilisation d'un médicament associant un corticoïde par voie inhalée et un bronchodilatateur bêta2-agoniste de longue durée d'action est justifiée, c'est-à-dire chez des patients insuffisamment contrôlés par une corticothérapie inhalée et la prise d'un bronchodilatateur bêta2-agoniste à action rapide et de courte durée par voie inhalée « à la demande » ;
- dans le traitement symptomatique de la BPCO (bronchopneumopathie chronique obstructive) chez les adultes (18 ans et plus) dont le VEMS (volume expiratoire maximum seconde) mesuré après administration d'un bronchodilatateur est inférieur à 70 % de la valeur théorique et ayant des antécédents d'exacerbations malgré un traitement bronchodilatateur continu.
- un corticoïde, le furoate de fluticasone (92 µg par dose) ;
- un nouvel agoniste sélectif des récepteurs bêta2 adrénergiques de longue durée d'action, le vilantérol (22 µg/dose).
Place de RELVAR ELLIPTA dans la stratégie thérapeutique
- Concernant la BPCO
Dans la population conforme à l'autorisation de mise sur le marché, RELVAR ELLIPTA 92/22, administré 1 fois par jour, a permis de réduire les exacerbations modérées (aggravation des symptômes de BPCO nécessitant le recours à un corticoïde oral et/ou un antibiotique) à sévères (aggravation des symptômes de BPCO nécessitant une hospitalisation) de 21 % et de 34 % par rapport au vilantérol 22 µg 1 fois par jour seul, respectivement dans les deux études pivots de phase III de 52 semaines (études HCZ102970 et HCZ102871, de protocoles similaires).
En termes de tolérance, les effets indésirables les plus fréquemment observés au cours des études cliniques menées avec RELVAR ELIPTA ont à type de céphalée et de rhinopharyngite (>= 1/10).
Dans le cadre de cet avis, la Commission a pris en compte :
- l'absence de données spécifiques sur les seules exacerbations sévères, "critère plus pertinent en termes de bénéfice pour le patient",
- l'absence de démonstration de l'intérêt de cette association par rapport au vilantérol seul en termes de VEMS, de dyspnée ou de qualité de vie,
- l'absence de données cliniques permettant de situer la place de cette association par rapport aux autres associations inhalées corticoïde/bêta2 agoniste de longue durée d'action, en particulier l'association propionate de fluticasone/salmétérol xinafoate 500/50 µg, comparateur le plus proche par son indication.
Dans cette indication, RELVAR ELLIPTA est remboursable au taux de 30 % et agréée aux collectivités.
- Concernant l'asthme
De plus, aucune étude clinique n'a pas montré la supériorité ou la non infériorité de RELVAR ELLIPTA par rapport à une autre association corticoïde inhalé/bêta2 agoniste de longue durée d'action.
En termes de tolérance, les effets indésirables les plus fréquemment observés au cours des études cliniques menées avec RELVAR ELIPTA ont été à type de céphalée et de rhinopharyngite (>= 1/10), comme dans les études conduites dans la BPCO.
Au total, la Commission a jugé le SMR de RELVAR ELLIPTA insuffisant et a donné un avis défavorable à son remboursement par l'Assurance maladie ainsi qu'à son agrément aux collectivités, dans son indication d'AMM dans l'asthme.
RELVAR ELLIPTA en pratique
- Dans le traitement de la BPCO
Généralement, une amélioration de la fonction respiratoire est ressentie dans les 16 à 17 minutes suivant l'inhalation.
- Dans le traitement de l'asthme
Généralement, une amélioration de la fonction respiratoire est ressentie dans les 15 minutes qui suivent l'inhalation.
Si les symptômes surviennent entre les prises, un bronchodilatateur bêta2 agoniste à action rapide et de courte durée par voie inhalée doit être utilisé pour obtenir un soulagement immédiat.
Une utilisation quotidienne est nécessaire pour contrôler les symptômes de l'asthme ; il est important de rappeler aux patients que le traitement doit être poursuivi même en cas de disparition des symptômes.
RELVAR ELLIPTA : administration par voix inhalée
RELVAR ELLIPTA s'administre par voie inhalée uniquement, à l'aide du dispositif d'inhalation ELLIPTA.
Il doit être administré chaque jour au même moment de la journée.
Le dispositif ELLIPTA est muni d'un compteur de doses. Avant la première utilisation, il indique 30 doses.
A chaque ouverture du dispositif (chaque fois que le couvercle du dispositif est ouvert), une dose de médicament est préparée pour être inhalée ; le compteur de dose affiche 1 dose en moins.
Lorsqu'il reste moins de 10 doses, la moitié du compteur devient rouge.
Conseils aux patients
Avant de prendre la dose, le patient doit expirer autant que possible (à distance de l'inhalateur).
Le patient doit ensuite serrer fermement les lèvres autour de l'embout buccal (sans bloquer la grille d'aération avec les doigts) et inspirer profondément et régulièrement pendant au moins 3 à 4 secondes.
Après inhalation, le patient doit se rincer la bouche avec de l'eau (sans l'avaler) afin de réduire le risque de candidose buccale.
En cas d'oubli d'une prise, la dose suivante doit être prise à l'heure habituelle le lendemain.
Si l'inhalateur est conservé dans un réfrigérateur, il doit rester pendant au moins une heure à température ambiante avant d'être utilisé.
Identité administrative
- Liste I
- Boîte contenant 1 inhalateur de 30 doses, CIP 3400927619960
- Prix public TTC = 41,28 euros
- Remboursable à 30 % dans le traitement symptomatique de la BPCO (Journal officiel du 3 juin 2015, texte 18)
- Agrément aux collectivités dans le traitement symptomatique de la BPCO (Journal officiel du 3 juin 2015, texte 19)
- Laboratoire GlaxoSmithKline
Pour aller plus loin
Résumé EPAR pour le public (EMA, mise à jour du 5 juin 2015)
Avis de la Commission de la Transparence relatif au remboursement de RELVAR ELLIPTA dans le traitement de la BPCO (HAS, 17 décembre 2014)
Avis de la Commission de la Transparence relatif au remboursement de RELVAR ELLIPTA dans le traitement de l'asthme (HAS, 17 décembre 2014)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 5 minutes
5 minutes Ajouter un commentaire
Ajouter un commentaire.jpg)
.jpg)
.jpg)
.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.